Средняя эффективная доза (Median Effective Dose (ЭД50)) нефопама и кетопрофена для лечения послеоперационной боли
Исследование взаимодействия с помощью изоболографического анализа и последовательного определения пороговой дозы.
Доктор медицины Noemie Delage, доктор медицины Hilal Maaliki, доктор медицины Helene Beloeil,
доктор медицины Dan Benhamou, доктор медицины, к.н. Jean-Xavier Mazoit
Предпосылки: Эффективность кетопрофена была продемонстрирована при лечении послеоперационного болевого синдрома средней и тяжелой степени. Эффективность нефопама была показана при лечении послеоперационного болевого синдрома средней тяжести. Целью данного исследования было определение средней эффективной дозы каждого препарата в отдельности и выяснение того, приводит ли комбинированное применение указанных средств к взаимному усилению их анальгетической активности.
Методы: Семьдесят два пациента, включенных в план проведения хирургического лечения средней степени болезненности, были распределены в три группы исследования. Доза нефопама и кетопрофена для каждого пациента определялась на основании результатов оценки эффективности лечения предыдущего больного той же группы исследования, используя метод «вверх и вниз». Стартовая доза анальгетиков составляла 18 и 40 мг с интервалом коррекции 2 и 5 мг в группах нефопама и кетопрофена соответственно. Начальные дозы нефопама и кетопрофена в группе нефопама-кетопрофена были 8 и 20 мг соответственно, с тем же интервалом коррекции дозы. Эффективность анальгезии определялась как уменьшение боли до уровня менее 3-х баллов по числовой шкале боли в пределах значений от 0 до 10 через 45 мин после начала инфузии препарата.
Результаты: Средняя эффективная доза обезболивания (медиана и доверительный интервал 95%) для нефопама и кетопрофена была, соответственно, 28 мг (17-39 мг) и 30 мг (14-46 мг). Средняя эффективная анальгетическая доза при сочетанном введении была 1,75 мг (0,9-2,3 мг) для нефопама и 4,3 мг (2,2-6,5 мг) для кетопрофена. Заключение: Результаты изоболографического анализа показали, что сочетание двух указанных препаратов оказывает выраженное обезболивающее действие со значительным синергическим эффектом.
СБАЛАНСИРОВАННАЯ анальгезия, т. е. использование комбинации препаратов, относящихся к разным фармакологическим группам, как ожидается, может улучшить результаты обезболивающей терапии и уменьшить частоту возникновения и тяжесть побочных эффектов каждого лекарственного средства в отдельности[1]. Поскольку применение анальгетиков, традиционно используемых для лечения послеоперационного болевого синдрома (например, морфина, нестероидных противовоспалительных препаратов (НПВП) и парацетамола), связано с определенными ограничениями и с развитием ряда побочных эффектов, таких как тошнота, рвота, подавление функции тромбоцитов, нарушение работы почек или ограничение дозы лекарственных средств по причине гепатотоксичности, использование ненаркотического анальгетика нефопама может быть целесообразным. Нефопам представляет собой рацемическую смесь двух энантиомеров, имеющих лишь небольшие различия фармакокинетических и фармакодинамических свойств[2].
Нефопам имеет центральный механизм действия[3], подавляя повторный захват серотонина, дофамина, норадреналина нервными клетками мозга[4-6]. Нефопам также влияет на механизм глутаматергической передачи путем ингибирования рецепторов N-метил-D-аспартата[7,8]. Кроме того, выявлено, что нефопам уменьшает иммунореактивную экспрессию транскрипционного фактора с-Fos в задних рогах спинного мозга у крыс через 1 ч после внутриподошвенной инъекции препарата[9]. Несколько исследований показали его эффективность в лечении послеоперационного болевого синдрома [10-12]. Нефопам также увеличивал порог появления тремора в опытах с участием добровольцев[13] и доказал свою эффективность при лечении посленаркозного озноба[14]. Обычная доза препарата для внутривенного введения составляет 20 мг. В предыдущем исследовании мы определяли среднюю эффективную анальгезирующую дозу (E50 = эффективная анальгезия у 50% больных) и 95% доверительный интервал (ДИ) для нефопама, морфина и их комбинации у больных с умеренным болевым синдромом[15]. Величина E50 для нефопама и морфина была, соответственно, 17 мг (ДИ 95%: 15,4-18,6 мг) и 5 мг (ДИ 95%: 4-6 мг), для каждого препарата в отдельности, а также 13,5 мг (ДИ 95%: 9,8-17,2 мг) и 4,5 мг (ДИ 95%: 3,3-5,7 мг) соответственно, когда оба препарата применялись одновременно. Тип взаимодействия между препаратами был определен как инфрааддитивный эффект[15].
Нестероидные противовоспалительные средства являются мощными анальгетиками, которые широко применяются для лечения больных в послеоперационном периоде[16-18]. Они проявляют свою активность как через центральные, так периферические механизмы действия, в основном путем блокады синтеза простагландинов[18,19]. В исследованиях на животных комбинация морфина и различных НПВП оказывала потенцирующее действие на обезболивающую активность испытуемых средств[20,21]. Кетопрофен является НПВП, широко применяемым для лечения послеоперационной боли, обладающим сильной способностью уменьшать необходимую дозу морфина[16,22]. Однако в связи с тем, что эффект уменьшения дозы морфина сам по себе не позволяет однозначно сделать вывод о наличии синергического типа межлекарственного взаимодействия, мы решили исследовать лечебную активность комбинации препаратов нефопам (анальгетик центрального действия) и кетопрофен (агент, частично реализующий свой фармакологический потенциал через периферические эффекты). Для этой цели мы вначале использовали метод Диксона «вверх и вниз» для определения ЭД50[23,24], а затем изоболографический анализ [25-27].
Материалы и методы
Отбор участников исследования.
После одобрения этическим комитетом (больница Кочин-Порт-Рояль, Государственной системы здравоохранения Парижа, Франция) и подписания формы письменного информированного согласия в исследование были включены 72 пациента, имеющих уровень физического состояния I или II по классификации Американского общества анестезиологов. Все пациенты были включены в план проведения хирургического лечения, которое расценивалось как сопровождающееся умеренным послеоперационным болевым синдромом (например, устранение паховой грыжи или малые операции в отоларингологии). Критерии исключения из исследования: (1) противопоказания к назначению нефопама и кетопрофена, включая беременность; (2) возраст моложе 18 лет; (3) применение интраоперационной регионарной анестезии и (4) послеоперационная оценка боли меньше 3-х баллов по цифровой шкале боли (numeric pain scale (NPS)): 0 = нет боли, 10 = максимальная боль) на момент прибытия в палату посленаркозного наблюдения (postanesthesia care unit (PACU)).
Протокол проведения анестезии.
Вечером, накануне операции, пациенты были проинструктированы о том, как использовать NPS. Всем пациентам проводилась общая анестезия пропофолом или тиопенталом в сочетании десфлураном или изофлураном. Разрешалось применение следующих опиоидов: альфентанил, ремифентанил и суфентанил. В конце операции всем пациентам вводился 1 мг дроперидола внутривенно.
Протокол проведения анальгезии.
Исследование было двойным слепым рандомизированным и проспективным. Участники были распределены в три группы исследования, используя таблицу, созданную с помощью компьютерной программы. Маскирование обеспечивалось за счет использования шприцов вслепую свежеприготовленных анестезиологом, который не участвовал в какой-либо другой части исследования, включая оценку тяжести болевого синдрома. Сразу же после прибытия пациентов в PACU интенсивность боли оценивалась с помощью NPS. Адекватность обезболивания оценивалась одним из двух исследователей: N. D. или H. M. Если интенсивность боли оценивалась на уровне 3-х баллов и выше (на момент поступления в палату посленаркозного наблюдения – время 0 (time 0 (T0)), пациент включался в исследование и получал анальгезию согласно установленному протоколу. В момент T0 пациенты в группе нефопама получали нефопам в шприце 20 мл в виде непрерывной внутривенной инфузии в течение 10 мин и 125 мл изотонического раствора внутривенно, в виде короткой инфузии в течение 10 мин. Пациентам из группы кетопрофена внутривенно вводился кетопрофен в виде короткой инфузии 125 мл раствора в течение 10 мин и физиологического раствора в шприце 20 мл в виде непрерывной внутривенной инфузии в течение 20 минут. Проведение инфузий было необходимо при введении обоих препаратов для предотвращения развития побочных реакций. Доза нефопама и кетопрофена для каждого пациента определялась на основании оценки эффективности лечения предыдущего больного той же группы исследования, используя метод последовательного определения пороговой дозы «вверх и вниз»[23]. В группе нефопама, первый пациент получил 18 мг препарата. Интервал коррекции дозы составлял 2 мг. В группе кетопрофена первый пациент получил 40 мг препарата. Интервал коррекции дозы составлял 5 мг. Интервалы коррекции доз были установлены в соответствии с ожидаемой стандартной ошибкой для E5023,24. Больные из группы нефопам-кетопрофен получали нефопам внутривенно в 20-мл шприце в виде непрерывной инфузии в течение 20 минут и кетопрофен внутривенно в виде короткой инфузии 125 мл раствора препарата в течение 10 мин. Первый пациент получил 8 мг нефопама и 20 мг кетопрофена, исходя из предварительно рассчитанного соотношения эффективности препаратов 1:2.5 (примерно половина исходной дозы, использованной при испытаниях каждого компонента в отдельности). Интервал коррекции дозы составлял 2 мг для нефопама и 5 мг для кетопрофена. Эффективность исследуемого препарата оценивали с помощью NPS через 45 мин после начала инфузии препарата [10, 16]. Учитывались два типа результатов: (1) положительный: значение по шкале NPS находится в пределах 3-х баллов и ниже из 10-ти возможных на 45-ю минуту введения препарата (time 45 (T45)) (при положительном результате доза понижалась на 2 мг в группе нефопама, на 5 мг в группе кетопрофена, а также на 2 мг нефопама и 5 мг кетопрофена в группе нефопама-кетопрофен для следующего пациента) и (2) отрицательный: показатель тяжести боли по шкале NPS более 3-х баллов из 10-ти возможных на T45 (при отрицательном результате доза повышалась [в той же градации как указано выше] для следующего пациента).
На 45 минуту, участникам исследования, которые сообщили о неэффективности проводимой терапии, назначалось экстренное лечение морфином в дробных дозах по обычной схеме, предусмотренной в нашей PACU.
Побочные эффекты.
Известные побочные эффекты, развивающиеся при приеме нефопама (потливость, тошнота, рвота, головокружение, тахикардия, сухость во рту, повышение кровяного давления, локальная боль в месте инфузии) и кетопрофена (тошнота, рвота, головокружение, боль в животе, головная боль, боль по ходу сосудов при внутривенном введении, сыпь на коже или зуд), регистрировались на 30-ю, 45-ю и 60-ю мин после начала инфузии, и каждые 30 мин после завершения процедуры введения препарата до момента выписки больного из PACU.
Статистический анализ.
В исследование включались только те пациенты, у которых тяжесть боли оценивалась на уровне 3-х баллов или выше на момент прибытия в PACU. Сначала определялась средняя доза каждого препарата в отдельности (E50), которая вызывала эффективную анальгезию у 50% пациентов, включенных в исследование. Вероятность того, что тяжесть боли согласно NPS составит менее 3-х баллов после введения испытуемых анальгетиков, моделировалась с помощью метода Диксона последовательного определения пороговой дозы «вверх и вниз»23,24. Метод «вверх и вниз», применяя принцип «все или ничего», позволяет определить пороговое значение какого-либо параметра, выше которого 50% участников положительно реагируют на экспериментальный стимул и ниже которого 50% участников реагируют отрицательно. В кратком изложении, после введения исходной дозы первому пациенту, последующие дозы рассчитываются по следующему правилу: Если участник реагирует положительно на введение препарата, доза для следующего пациента снижается на одну ступень, и наоборот, если участник реагирует отрицательно на проводимую терапию, для следующего пациента доза повышается на одну ступень. После того как E50 для каждого препарата в отдельности была определена, проводились испытания их комбинации в фиксированном соотношении, которое было установлено на основании найденных ЭД50, для чего вновь применялся метод «вверх и вниз» с целью определения величины E50 для сочетанной терапии. Поскольку метод Диксон позволяет определить только среднюю дозу лекарственного средства и стандартное отклонение, и не дает возможности вывести полную кривую зависимости исходов лечения от величины использованной дозы препарата, мы исследовали межлекарственное взаимодействие испытуемых анальгетиков с помощью классического изоболографического анализа28. Изоболографический анализ — это графический метод, который позволяет проследить поведение двух (или более чем двух) лекарственных средств при использовании их в комбинации25-27. Изобола — это контур, который соединяет две экспериментально установленные дозы для пары лекарственных средств, которые вызывают определенную ответную реакцию.
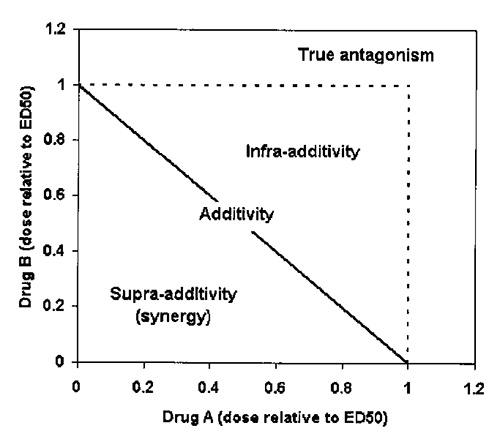
Рис. 1. Изоболограмма лекарственного взаимодействия типа «препарат-препарат». Изобола представлена в виде прямой линии, которая соединяет пары доз, которые вызывают одинаковую ответную реакцию (в данном случае средняя эффективная доза [E50]). Результат лекарственного взаимодействия двух препаратов, комбинированных в соответствии и с их дозой E50, тестируется путем нанесения на график точек с координатами доз, вызывающих ответную реакцию на уровне E50. Комбинация вызывает суммирующий эффект, если точка расположена на изоболе, потенцирующий (синергический), если точка находятся под изоболой и взаимоподавляющий (антагонистический) эффект, когда координаты точки находятся выше изоболы. Например, эффект препарата А может составлять комбинированный эффект половины дозы препарата А и половины дозы препарата А или одной трети дозы препарата А и двух третей дозы препарата А.
Изоболограммы —это диаграммы изобол, помещенные на картезианский график. Эффект воздействия считается суммированным, когда невозможно провести различие между двумя препаратами (в соотношении, соответствующем их относительной эффективности). В классическом представлении Loewe26, суммирование эффектов лекарственных средств представляется в виде прямой линии на изоболограмме. Таким образом, можно квалифицировать эффект исследуемого лекарственного взаимодействия как суммирующий, потенцирующий (синергический), или антагонистический (рис. 1). Доверительные границы на уровне девяносто пять процентов для комбинированной терапии были определены путем соединения показателей ДИ 95% на обеих осях изоболограммы. Результат лекарственного взаимодействия считался суммированным, если эти границы накладывались друг на друга. В других случаях сочетанный эффект считался синергичным или антагонистичным. Демографические данные трех групп исследования сравнивались с использованием критерия хи-квадрат или с помощью дисперсионного анализа в зависимости от конкретных условий. Развитие нежелательных явлений и побочных эффектов сравнивалось между группами с использованием точного критерия Фишера. Значения E50 представлены с указанием ДИ.
Результаты
Демографические данные участников в трех группах исследования (возраст, соотношение полов, масса тела, тип и продолжительность операции) были сопоставимы (Таблица 1). Альфентанил не вводился ни одному из пациентов. Число пациентов, получавших ремифентанил, было сопоставимым во всех трех группах исследования (Таблица 1). Ни один пациент не был исключен из исследования по причине того, что их исходное значение NPS оказалось ниже 3-х баллов. Все участники полностью выполнили программу испытаний. При поступлении в PACU, на момент времени Т0, тяжесть болевого синдрома, согласно оценкам NPS, была сопоставимой во всех трех группах исследования (Таблица 1 и рис. 2). Значения E50 для нефопама и кетопрофена были 28 мг (17-39 мг) и 30 мг (14-46 мг) соответственно. Значения E50 для сочетанной терапии составили 1,75 мг (0,9-2,3 мг) для нефопама и 4,3 мг (2,2-6,5 мг) для кетопрофена, указывая на выраженный потенцирующий эффект комбинированного лечения. Последовательность эффективных и неэффективных опытов по обезболиванию отображена на рисунке 3, изоболограммы представлены на рисунке 4. За период пребывания пациентов в РACU случаи болей в животе, кожной сыпи или зуда, брадикардии и гипотонии не наблюдались ни у одного пациента. В отношении частоты случаев потливости, тошноты, рвоты, сухости во рту, головной боли, седативной реакции, головокружения или тахикардии, существенных различий между группами исследования не наблюдалось. В группе кетопрофена жалобы на локальную боль, связанную с внутривенным введением препарата, наблюдались значительно чаще (Таблица 2).
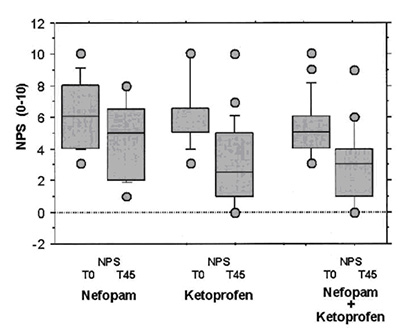
Рис. 2. Процентили значений числовой шкалы боли (NPS; от 0 до 10) в трех группах исследования перед введением препарата (T0) и через 45 мин от начала лечения (ячейки), 10-е-90-е процентили (линии) и нетипичные значения (окружности). Эффективность обезболивания на момент времени T45 была ниже (хотя и незначительно) в группе нефопама, чем в других группах, вероятно, потому что исходная доза была далека от средней эффективной дозы в этой группе, что привело к тому, что качество анальгезии первых пациентов было низким (рис. 3).
Таблица 1. Демографические данные 72-х пациентов. |
|||
|
Нефопам (n = 24) |
Кетопрофен (n = 24) |
Нефопам плюс кетопрофен (n = 24) |
Пол М/Ж |
16/8 |
11/13 |
15/9 |
Возраст (лет) |
40 ± 13 |
43 ± 13 |
47 ± 15 |
Масса тела (кг) |
73 ± 16 |
68 ± 13 |
70 ± 14 |
Продолжительность операции (мин) |
104 ± 62 |
123 ± 54 |
135 ± 85 |
Общая доза ремифентанила |
1,95 ± 0,31 |
1.84 ± 0,42 мг |
1,86 ± 0,38 мг |
Число больных |
(8) |
(9) |
(5) |
Общая доза суфентанила |
30 ± 9,4 /нг |
35± 9,8 / g |
35± 10,6 / g |
Число больных |
(12) |
(11) |
(19) |
Операция |
|
|
|
| Ортопедическая | 8 (33%) |
5 (21%) |
4 (17%) |
|
Удаление ортопедического материала (n = 6) |
Удаление ортопедического материала (n = 4)} |
Удаление ортопедического материала (n = 3) |
|
|||
|
Сшивание сухожилия (рука) |
Сшивание сухожилия (рука) |
Экзостоз пальца ноги |
|
Тенолиз |
|
|
Отоларингологическая |
8 (33%) |
9 (37%) |
6 (25%) |
|
Операция на ухе (n = 6) |
Операция на ухе (n = 7) |
Операция на ухе (n = 2) |
|
Удаление зубов (n = 2) |
Удаление зубов (n = 2) |
Удаление зубов (n = 2) удаление слюнной железы (n = 2) |
На брюшной полости и урогенитальной области |
8 (33%) |
10 (42%) |
14 (58%) |
|
Герниорафия (n = 4) |
Герниорафия (n = 7) |
Герниорафия (n = 7) |
|
Холецистэктомия* (n = 2) |
Холецистэктомия* (n=2) |
Холецистэктомия* (n =2) |
|
Закрытие колостомы |
|
Закрытие колостомы (n=2) |
|
Спленэктомия* (частичная) |
Спленэктомия* (частичная) |
Адреналэктомия* (n = 2) Аппендэктомия |
NPS |
|
|
|
T0 |
6 (4-8) |
5 (5-6,5) |
5 (4-6) |
T 45 мин |
5 (2-6) |
2,5 (1-5) |
3 (1-4) |
Числовая шкала боли (Numerical pain scale (NPS)) от 0—нет боли до 10 = максимальная боль. Данные представлены в виде среднего значения ± стандартное отклонение; количества (процента), если применимо; медианы и границ вероятности для показателей NPS. Статистически достоверных различий между тремя группами выявлено не было. * Путем лапараскопии. |
|||
Значения E50 для нефопама и кетопрофена были 28 мг (17-39 мг) и 30 мг (14-46 мг) соответственно. Значения E50 для сочетанной терапии составили 1,75 мг (0,9-2,3 мг) для нефопама и 4,3 мг (2,2-6,5 мг) для кетопрофена, указывая на выраженный потенцирующий эффект комбинированного лечения. Последовательность эффективных и неэффективных опытов по обезболиванию отображена на рисунке 3, изоболограммы представлены на рисунке 4.
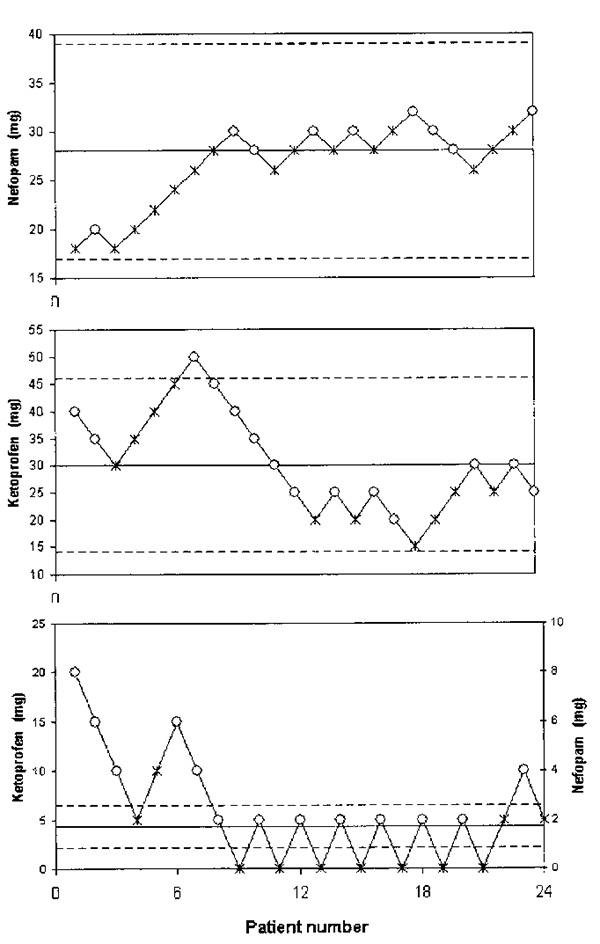
Рис. 3. Последовательность дозирования в трех группах пациентов, которым вводился нефопам, кетопрофен и сочетание нефопама и кетопрофена в соотношении 2,5 / 1. Качество обезболивания оценивали по цифровой шкале боли (от 0 до 10). Результат определялся как положительный (значение числовой шкалы боли <3 баллов) или отрицательный (значение числовой шкалы боли> 3 баллов). Звездочки обозначают отрицательный результат терапии (неэффективное обезболивание), и незакрашенные окружности обозначают положительный результат терапии (эффективное обезболивание). На каждом графике горизонтальные линии обозначают среднюю эффективную дозу (жирная линия) и ее доверительный интервал 95% (пунктирные линии).
За период пребывания пациентов в РACU случаи болей в животе, кожной сыпи или зуда, брадикардии и гипотонии не наблюдались ни у одного пациента. В отношении частоты случаев потливости, тошноты, рвоты, сухости во рту, головной боли, седативной реакции, головокружения или тахикардии, существенных различий между группами исследования не наблюдалось. В группе кетопрофена жалобы на локальную боль, связанную с внутривенным введением препарата, наблюдались значительно чаще (Таблица 2).
Таблица 2. Частота развития побочных эффектов |
|||
|
Нефопам (n = 24) |
Кетопрофен (n = 24)} |
Нефопам плюс кетопрофен (n = 24) |
Потливость |
3 (12%) |
0 |
1 (4%) |
Тошнота |
1 (4%) |
2 (8%) |
1 (4%) |
Рвота |
0 |
1 (4%) |
0 |
Головокружение |
4 (17%) |
0 |
2 (8%) |
Сухость во рту |
10 (42%) |
8 (33%) |
6 (25%) |
Боль в месте инфузии |
0 |
7 (29%)* |
2 (8%) |
Головная боль |
0 |
1 (4%) |
2 (8%) |
Боль в животе |
0 |
0 |
0 |
Зуд |
0 |
0 |
0 |
Кожная сыпь |
0 |
0 |
0 |
Гипертензия |
0 |
1 (4%) |
3 (12%) |
Тахикардия |
3 (12%) |
0 |
0 |
Побочные эффекты регистрировались каждые 30 мин в палате посленаркозного наблюдения до момента выписки (все пациенты находились в палате посленаркозного наблюдения не менее 60 мин). Любая побочная реакция была зарегистрирована, если она была отмечена в любой момент времени в течение этого периода наблюдений. Результат показан в виде числа пациентов (процент). * P < 0.05 в сравнении с группой нефопама и нефопама плюс кетопрофен. |
|||
|
|||
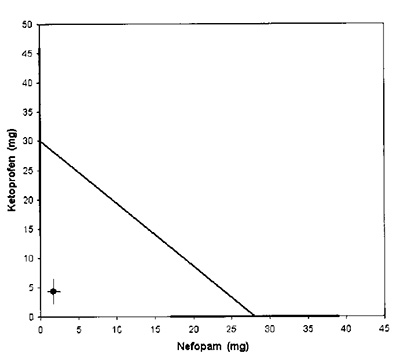
Рис. 4. Изоболограмма лекарственного взаимодействия кетопрофена и нефопама. Линия, соединяющая средние эффективные дозы (E50) каждого препарата в отдельности (нефопам на оси Х и кетопрофен на оси У), представляет собой состояние простого суммирования фармакологических эффектов. Значения ЭД50 показаны в сопровождении доверительных интервалов 95% (жирные линии). Величина E50 для комбинированной терапии (в соотношении 2,5/1) показана в черной окружности с доверительным интервалом 95%.
Обсуждение
Мы установили среднюю эффективную анальгезирующую дозу нефопама и кетопрофена при монотерапии и комбинированном лечении послеоперационного болевого синдрома средней степени тяжести. Комбинированная терапия нефопамом и кетопрофеном показала выраженный эффект потенцирования фармакологического действия испытуемых лекарственных средств. Мы использовали метод последовательного определения эффективности лечения «вверх и вниз» для установления величины E50. На втором этапе исследования был использован изоболографический анализ для оценки эффективности межлекарственного взаимодействия при совместном применении обоих препаратов. Метод Диксона «вверх и вниз» позволяет определить E50 при использовании меньшего числа пациентов, чем традиционные способы исследования. В связи с этим, данный метод широко используется для расчета минимальной концентрации местных анестетиков, применяемых для регионарной анестезии и особенно в акушерской практике[29]. На втором этапе исследования мы использовали изоболографический анализ для сравнения E50 испытуемых препаратов по отдельности и при комбинированном назначении (рис. 1). Любопытно то, что изоболографический анализ комбинации обезболивающих средств широко применяется в доклинических испытаниях, но очень редко — в клинических экспериментах. Основываясь на нескольких предшествующих исследованиях[15,20,21,3], мы хотели установить, обладает ли комбинация кетопрофена и нефопама эффектом взаимного усиления анальгетического действия.
В предыдущем исследовании[15] мы получили результат определения E50 при лечении нефопамом на уровне 17 мг (15,4-18,6 мг) на сравнимой группе больных, то есть пациентов с умеренным болевым синдромом в течение самого раннего этапа послеоперационного периода. В настоящем исследовании результат определения E50 был 28 мг (17-39 мг), что также выше, чем 20 мг по рекомендации компании-производителя. Установление более высокого показателя E50 для нефопама по результатам текущего исследования по сравнению с предыдущими испытаниями может быть объяснено тем, что в настоящем исследовании мы оценивали тяжесть болевого синдрома через 45 мин после 20-минутной инфузии лекарственных средств по сравнению с тем, что в первом исследовании эффективность анальгезии определялась через 30 мин после начала 15-минутной инфузии препарата. Тем не менее, в связи с тем, что границы ДИ относительно велики, различия в результатах этих исследований должны оцениваться с осторожностью. Если бы нефопам применялся в качестве монотерапии, нужно было бы использовать более высокие дозы препарата, для того чтобы достигнуть адекватный уровень анальгезии более чем у 90% больных.
Величина E50 для кетопрофена, лекарственного средства, которое широко используется для ведения пациентов в послеоперационном периоде, никогда не определялась. Мы определили величину E50 для кетопрофена на уровне 30 мг. Полученный результат находится в соответствии с эмпирическим опытом нашей клинической практики использования данного препарата в дозе 50 мг[31]. Это подтверждает целесообразность применения кетопрофена, как и большинства НПВП, для лечения послеоперационного болевого синдрома[32].
Значения E50 для сочетанной терапии нефопамом и кетопрофеном составили 1,75 мг (0,9-2,3 мг) для нефопама и 4,3 мг (2,2-6,5 мг) для кетопрофена, указывая на выраженный синергизм данной комбинации препаратов. Частично уменьшая местную воспалительную реакцию, кетопрофен имеет спектр анальгетической активности, который отличается от таковой других анальгетиков, таких как нефопам, действующих на центральные механизмы боли. Именно поэтому мы выбрали для исследования комбинацию кетопрофена и нефопама. Нефопам усиливает подавляющую активность нисходящих серотонинергических и норадреналиновых нисходящих нервных путей, блокируя транспорт допамина, норадреналина и серотонина через синаптические мембраны[4]. Это подтверждается данными, полученными в работе Buritova и Besson[9], в которой было показано влияние нефопама на экспрессию иммунореактивного белка с-Fos на уровне спинного мозга. Кетопрофен, как и другие НПВП, обладая частичным периферическим эффектом, уменьшая местную воспалительную реакцию[16,18,33,34], тем не менее, также влияет на центральные механизмы развития боли[18,19,34]. Таким образом, за счет того, что кетопрофен и нефопам действуют на различные эффекторы и нервно-рефлекторные пути, они проявляют свойства синергизма при их использовании в рамках комбинированной терапии. В предыдущих исследованиях мы изучали возможность синергической активности при сочетании морфина и нефопама, двух препаратов, в основном центрального действия,[15] и комбинации морфина с трамадолом[30], также препаратов центрального действия. Ни одна из этих фармакологических комбинаций не проявила синергических свойств. Сочетание нефопама и кетопрофена явилось первой комбинацией, которая демонстрирует синергический лечебный эффект в условиях клинических испытаний.
Как и ожидалось, в ходе исследования мы не наблюдали развития серьезных побочных эффектов. Низкая частота развития потливости в группе нефопама (наиболее частая побочная реакция, типичная для данного лекарственного средства) может быть объяснена низкой скоростью введения препарата (20 мг в течение 20 мин). Единственное различие между группами заключалось в том, что у пациентов, которым вводился кетопрофен, значительно чаще развивалась боль в месте внутривенного введения препарата (29% пациентов), чем у пациентов в других группах исследования. Применение двух испытуемых препаратов в комбинации не снижало частоту возникновения побочных эффектов, вероятно, из-за того, что частота их развития была относительно низкой в ходе их применения в качестве монотерапии (Таблица 2). Тем не менее, представляется благоприятной возможность использования минимальной дозы каждого препарата[35], так как комбинированная терапия потенциально может привести к снижению частоты развития и тяжести побочных эффектов.
В заключение следует отметить, что данное исследование является первым по определению средней эффективной анальгетической дозы (E50) кетопрофена (30 мг) для лечения послеоперационного болевого синдрома средней тяжести. Наряду с этим, опыты комбинированной терапии нефопамом и кетопрофеном показали выраженный эффект потенцирования фармакологического действия испытуемых лекарственных средств. Мы полагаем, что причиной данного результата является воздействие на различные механизмы развития болевого синдрома. Необходимы дальнейшие исследования по сравнению комбинированной активности опиоидов, НПВП и парацетамола с целью дальнейшего выяснения механизмов межлекарственного взаимодействия этой группы фармакологических средств, что послужит основанием для улучшения результатов клинической практики.
- Dahl JB, Rosenberg J, Dirkes WE, Mogensen T, Kehlet H: Prevention of postoperative pain by balanced analgesia. Br J Anaesth 1990; 64:518-20
- Mather GG, Labroo R, Le Guern ME, Lepage F, Gillardin JM, Levy RH: Nefopam enantiomers: Preclinical pharmacology/toxicology and pharmacokinetic characteristics in healthy subjects after intravenous administration. Chirality 2000; 12:153-9
- Guirimand F, Dupont X, Bouhassira D, Brasseur L, Chauvin M: Nefopam strongly depresses the nociceptive flexion (Rm) reflex in humans. Pain 1999; 80:399-404
- Piercey MF, Schroeder LA: Spinal and supraspinal sites for morphine and nefopam analgesia in the mouse. Eur J Pharmacol 1981; 74:135-40
- Rosland JH, Hole K: The effect of nefopam and its enantiomers on the uptake of 5-hydroxytryptamine, noradrenaline and dopamine in crude rat brain synaptosomal preparations. J Pharm Pharmacol 1990; 42:437-8
- Fuller RW, Snoddy HD: Evaluation of nefopam as a monoamine uptake inhibitor in vivo in mice. Neuropharmacology 1993; 32:995-9
- Fernandez-Sanchez MT, Diaz-Trelles R, Groppetti A, Manfredi B, Brini AT, Biella G, Sotgiu ML, Novelli A: Novel effect of nefopam preventing cGMP increase, oxygen radical formation and neuronal death induced by veratridine. Neuropharmacology 2001; 41:935-42
- Verleye M, Andre N, Heulard I, Gillardin JM: Nefopam blocks voltage-sensitive sodium channels and modulates glutamatergic transmission in rodents. Brain Res 2004; 1013:249-55
- Buritova J, Besson JM: Effects of nefopam on the spinal nociceptive processes: A c-Fos protein study in the rat. Eur J Pharmacol 2002; 441:67-74
- McLintock TTC, Kenny GNC, Howie JC, McArdle CS, Lawrie S, Aitken H: Assessment of the analgesic efficacy of nefopam hydrochloride after upper abdominal surgery: A study using patient controlled analgesia. Br J Surg 1988; 75:779-81
- Mimoz O, Incagnoli P, Josse C, Gillon M-C, Kuhlman L, Mirand A, Soilleux H, Fletcher D: Analgesic efficacy and safety of nefopam vs. propacetamol following hepatic resection. Anaesthesia 2001; 56:520-5
- Du Manoir B, Aubrun F, Langlois M, Le Guern ME, Alquier C, Chauvin M, Fletcher D: Randomized prospective study of the analgesic effect of nefopam after orthopaedic surgery. Br J Anaesth 2003; 91:836-41
- Alfonsi P, Adam F, Passard A, Guignard B, Sessler DI, ChauvinM: Nefopam, a nonsedative benzoxazocine analgesic, selectively reduces the shivering threshold in unanesthetized subjects. ANESTHESIOLOGY 2004; 100:37-43
- Piper SN, Rohm KD, Suttner SW, Maleck WH, Kranke P, Boldt J: A comparison of nefopam and clonidine for the prevention of postanaesthetic shivering: A comparative, double-blind and placebo-controlled dose-ranging study. Anaesthesia 2004; 59:559-64
- Beloeil H, Delage N, Mazoit JX, Negre I, Benhamou D: The median effective dose of nefopam and morphine administered intravenously for postoperative pain after minor surgery: A prospective randomized double blind isobolographic study of their analgesic action. Anesth Analg 2004; 98:395-400
- Dahl JB, Kehlet H: Non-steroidal antiinflammatory drugs: Rationale for use in severe post operative pain. Br J Anaesth 1991; 66:703-12
- Ochroch EA, Mardini IA, Gottschalk A: What is the role of NSAIDs in pre-emptive analgesia? Drugs 2003; 63:2709-23
- Walker JS: NSAID: An update on their analgesic effects. Clin Exp Pharmacol Physiol 1995; 22:855-60
- Yaksh TL, Dirig DM, Conway CM, Svensson C, Luo ZD, Isakson PC: The acute antihyperalgesic action of nonsteroidal, anti-inflammatory drugs and release of spinal prostaglandin E2 is mediated by the inhibition of constitutive spinal cyclooxygenase-2 (COX-2) but not COX-1. JNeurosci 2001; 21:5847-53
- Fletcher D, Benoist JM, Gautron M, Guilbaud G: Isobolographic analysis of interactions between intravenous morphine, propacetamol, and diclofenac in carrageenin-injected rats. ANESTHESIOLOGY 1997; 87:317-26
- Miranda HF, Silva E, Pinardi G: Synergy between the antinociceptive effects of morphine and NSAIDs. Can JPhysiol Pharmacol 2004; 82:331-8
- Rao AS, Cardosa M, Inbasegaran K: Morphine-sparing effect of ketoprofen after abdominal surgery. Anaesth Intensive Care 2000; 28:22- 6
- Dixon WJ, Mood AM: A method for obtaining and analyzing sensitivity data. J Am Stat Assoc 1948; 48:109-26
- Dixon WJ: Staircase bioassay: The up-and-down method. Neurosci Biobehav Rev 1991; 15:47-50
- Berenbaum MC: What is synergy? Pharmacol Rev 1989; 41:93-141
- Greco WR, Bravo G, Parsons JC: The search for synergy: A critical review from a response surface perspective. Pharmacol Rev 1995; 47:331-85
- Minto CF, Schnider TW, Short TG, Gregg KM, Gentilini A, Shafer SL: Response surface model for anesthetic drug interactions. ANESTHESIOLOGY 2000; 92:1603-16
- Talarida RJ, Porreca F, Cowan A: Statistical analysis of drug-drug and site-site interactions with isobolograms. Life Sci 1989; 45:947-61
- Polley LS, Columb Mo, Naughton NN, Wagner DS, Dorantes DM, van de Ven CJ: Effect of intravenous versus epidural fentanyl on the minimum local analgesic concentration of epidural bupivacaine in labor. ANESTHESIOLOGY 2000; 93:122-8
- Marcou TA, Marque S, Mazoit JX, Benhamou D: Median effective dose (ED50) of tramadol and morphine in postoperative patients: A study of interactions. Anesth Analg 2005; 100:469-74
- Benhamou D, Bouaziz H, Zerrouk N, Preaux N: Audit of ketoprofen prescribingafter orthopedic andgeneralsurgery. Can. J. Anesth1999; 46:109-13
- Moote C: Efficacy of nonsteroidal anti-inflammatory drugs in the management of postoperative pain. Drugs 1992; 44:14-30
- Dionne RA, Gordon SM, TaharaM, Rowan J, Troullos E: Analgesic efficacy and pharmacokinetics of ketoprofen administered into a surgical site. J Clin Pharmacol 1999; 39:131-8
- Burian M, Tegeder I, Seegel M, Geisslinger G: Peripheral and central antihyperalgesic effects of diclofenac in a model of human inflammatory pain. Clin Pharmacol Ther 2003; 74:13-20
- Carr DB, Goudas LC: Acute pain. Lancet 1999; 353:2051-8
Anesthesiology 2005; 102:1211-6

