Министерство здравоохранения и социального развития РФ
Научный Центр акушерства, гинекологии и перинатологии РАМН
Российское общество акушеров-гинекологов

БАЗОВЫЕ ПРИНЦИПЫ ПРОВЕДЕНИЯ
АНЕСТЕЗИИ И ИНТЕНСИВНОЙ ТЕРАПИИ
У БЕРЕМЕННЫХ С ГЕСТОЗОМ
Методические рекомендации
Москва, 2004
Учреждение-разработчик: Научный Центр акушерства, гинекологии и перинатологии РАМН
Авторский коллектив: Кулаков В. И., Серов В. Н., Шифман Е. М., Федорова Т. А., Мурашко Л. Е., Пырегов А. В., Аревшатян А. В., Заварзина О. О.
Рецензент: зав. кафедрой акушерства и гинекологии лечебного факультета Московского государственного стоматологического университета, д. м. н., профессор Манухин И. Б.
Методические рекомендации посвящены клинико-физиологическому обоснованию диагностики, проведения интенсивной терапии и анестезиологического пособия у больных эклампсией и составлены с учетом информационного письма Российской ассоциации акушеров-гинекологов от 14 октября 2002 г.
Адресовано акушерам-гинекологам и анестезиологам-реаниматологам.
Эклампсия * – преобладание в клинических проявлениях преэклампсии поражения головного мозга с судорожным синдромом и комой.
* От греч. ![]() – вспышка.
– вспышка.
Факторы риска развития эклампсии:
- Тяжелая преэклампсия или эклампсия при предыдущих беременностях от одного и того же партнера.
- Тяжелая преэклампсия или эклампсия у матери.
- Первородящие.
- Юный возраст.
- Многоплодная беременность.
- Артериальная гипертензия.
- Заболевания почек.
- Системная красная волчанка.
КЛИНИКА И ДИАГНОСТИКА
Основная причина эклампсии – спазм сосудов головного мозга. Тяжелый, генерализованный отек мозга при эклампсии встречается реже, чем более типичная форма для этого заболевания – очаговый отек серого вещества мозга в затылочных долях. Существуют две патофизиологические теории, которые, впрочем, не исключают друг друга:
1. Спазм сосудов головного мозга в ответ на артериальную гипертензию (АГ), который приводит к ишемии и цитотоксическому отеку головного мозга.
2. Прогрессирующая дилатация сосудов головного мозга.
Расширение сосудов головного мозга наступает в том случае, когда
АГ превышает возможности ауторегуляции кровотока в артериолах.
В результате происходит их перерастяжение, увеличение кровенаполнения и выход жидкости за пределы сосудистого русла с формирова
нием отека. В норме механизмы ауторегуляции кровотока надежно
защищают головной мозг от изменений артериального давления (АД).
Ответ систем ауторегуляции мозгового кровотока на изменения общегопериферического сопротивления сосудов (ОПСС) исчисляется несколькими секундами и устанавливает наиболее выгодные параметры в течение 15–30 сек. В родах за счет боли и сокращений матки значительно увеличивается ликворное давление, достигая во время I и II периодов родов 710ммвод. ст., что также может способствовать нарушению мозгового кровотока. Мозговой кровоток у больных, перенесших эклампсию (данные допплерографии и магнитнорезонансной томографии), полностью восстанавливается только к 12–13 неделе послеродового периода, что объясняет случаи развития
«поздней» эклампсии.
Клинические формы эклампсии:
- отдельные судорожные припадки;
- серия судорожных припадков (эклампсический статус);
- эклампсическая кома.
Классическая триада преэклампсии (артериальная гипертензия, протеинурия и отеки) у больных с эклампсией встречается только в 50% случаев, но хотя бы один из этих признаков будет присутствовать всегда. В 20% случаев эклампсия протекает без протеинурии. Перед приступом эклампсии, а нередко и задолго до него, появляются жалобы на головную боль, головокружение, общую слабость, нарушение зрения («мелькание мушек перед глазами», «пелена и туман», вплоть до потери зрения), боли в подложечной области и правом подреберье. Нередко возникают опоясывающие боли за счет кровоизлияния в корешки спинного мозга (симптом Ольсхаузена). Незадолго до судорог отмечаются гиперрефлексия и клонус.
Приступ эклампсии развивается в четыре этапа:
1. Мелкие фибриллярные подергивания мышц лица с дальнейшим распространением на верхние конечности (при эпилепсии не бывает).
2. Тонические сокращения всей скелетной мускулатуры (потеря сознания, апноэ, цианоз, прикус языка, симптом Цангмейстера (Расширение зрачков)) продолжительностью до 30 сек.
3. Клонические судороги с распространением на нижние конечности.
4. Глубокий вдох, восстановление дыхания и сознания, амнезия.
Судороги при эклампсии носят тонико-клонический характер и, следовательно, представляют собой генерализованные, ритмичные мышечные сокращения. Таким образом, во время приступа эклампсии возникает прямая угроза остановки сердца и дыхания, аспирации желудочного содержимого, гипоксии и ацидоза. Ацидоз, который развивается после судорог, носит смешанный характер (респираторный и метаболический), вызывает спазм сосудов, увеличение общего периферического сопротивления сосудов и рост артериального давления (АД). Следствием ацидоза является увеличение внутричерепного объема крови и давления. При повторяющихся приступах эклампсии может наблюдаться гиперпирексия, что является проявлением нарушений терморегуляции вследствие повышения внутричерепного давления. Во время судорог и в ближайшее время после эклампсического припадка отмечается брадикардия плода, которая, как правило, быстро восстанавливается (если не происходит отслойки плаценты).
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Наиболее частые причины судорожного синдрома во время беременности, родов или после родоразрешения:
- эпилепсия;
- эклампсия;
- венозный тромбоз;
- медикаментозное отравление и действие лекарственных препаратов;
- гипогликемия;
- опухоль головного мозга;
- черепно-мозговая травма.
Осложнения эклампсии:
- гипертоническая энцефалопатия;
- геморрагический инсульт;
- субарахноидальные кровоизлияния;
- преждевременная отслойка плаценты;
- РВС-синдром;
- внутриутробная гибель плода;
- отек легких;
- синдром острого легочного повреждения;
- аспирационный синдром;
- нарушения зрения;
- острая печеночно-почечная недостаточность;
- послеродовые психозы.
ИНТЕНСИВНАЯ ТЕРАПИЯ ЭКЛАМПСИИ
Радикальное лечение эклампсии – это родоразрешение. Но в тех случаях, когда не проведена подготовка, роды (через естественные родовые пути или операция кесарева сечения) могут привести к жизненно опасным осложнениям матери и плода. Экстренное родоразрешение, предпринимаемое сразу же после приступа судорог без предварительной подготовки значительно увеличивает риск акушерских и анестезиологических осложнений. Подготовка к родоразрешению должна занимать около двух часов, за исключением тех осложнений эклампсии, которые требуют экстренного родоразрешения.
Необходимый объем обследования:
- Клинический анализ крови, включая тромбоциты и гематокрит.
- Биохимический анализ крови:
– общий белок, альбумин;
– креатинин, мочевина;
– билирубин (прямой, непрямой);
– АлАТ, АсАТ, ЩФ, ЛДГ;
– свободный гемоглобин крови;
– глюкоза крови;
– электролиты. - Анализ мочи на белок (в однократно взятой порции).
- Анализ суточной мочи на белок (повторно).
- Свободный гемоглобин мочи.
- Исследование глазного дна.
Подготовка к родоразрешению обычно совпадает по времени с началом интенсивной терапии.
Главные цели интенсивной терапии:
- прекратить судороги;
- восстановить проходимость дыхательных путей;
- обеспечить безопасность матери и плода.
Задачи интенсивной терапии:
- предотвратить повторные судороги;
- устранить гипоксию и ацидоз (дыхательный и метаболический);
- обеспечить профилактику аспирационного синдрома.
Наиболее важно в этот момент тесное взаимодействие между акушерской и анестезиологической бригадами. Ближайшая цель – прекращение судорог и поддержание проходимости дыхательных путей. Как можно раньше необходимо начинать оксигенотерапию.
Начало одинаково для всех неотложных ситуаций, то есть поддержание проходимости дыхательных путей, вентиляция и нормализация кровообращения. Если судороги продолжаются более 30 мин, необходимо подумать об эпилептическом статусе.
Препаратом выбора при лечении эклампсии является сульфат магния.
Первоначальное действие: внутривенно медленно в течение 15–20 мин вводится 6 г сульфата магния. Затем поддерживающая доза составляет 2 г/ч.
Если судорожный синдром купировать не удалось, то вводится от 2 до 4 г магнезии в течение 5 мин.
При повторении судорожных припадков вводят 450 мг барбитуратов в течение 3 мин.
Если это не помогает, то вводят мышечные релаксанты и переводят больную на ИВЛ. Нельзя отменять постоянную внутривенную инфузию сульфата магния во время операции или родов. Окситоцин в достаточной степени нивелирует релаксирующее действие магнезии на матку даже в тех единичных случаях, когда оно может возникнуть.
К дополнительной антигипертензивной терапии прибегают в случае увеличения диастолического АД до 110ммрт. ст. и более. При контролируемом снижении артериальной гипертензии следует снижать диастолическое АД не ниже 90мм рт. ст., так как это помогает поддерживать нормальный уровень ауторегуляции мозгового кровообращения. Для этих целей используют ганглиоблокаторы короткого действия или нитропруссид натрия.
При проведении инфузионной терапии у больных с эклампсией следует поступать крайне осторожно. У большинства из этих больных отмечается гиповолемия при высокой степени постнагрузки миокарда левого желудочка. В то же время у тех из них, у кого имеется выраженная интерстициальная легочная гипергидратация или отек легких, наблюдается увеличение преднагрузки. У небольшой части больных с эклампсией наблюдается левожелудочковая недостаточность вследствие систолической или диастолической дисфункции. Определить тактику интенсивной терапии (увеличение преднагрузки, снижение пред- или постнагрузки, инотропная терапия и т. д.) позволяет мониторинг центральной и периферической гемодинамики с помощью эхокардиографии или катетеризации легочной артерии. Эклампсия – это прежде всего генерализованное повреждение эндотелия с резким увеличением его проницаемости и интерстициальной гипергидратацией. Увеличение проницаемости капилляров приводит к отеку периваскулярных и перилимфатических пространств, который затрудняет отток альбумина, декстранов и воды из интерстициального пространства. Резко увеличивается онкотическое давление в интерстиции и во внесосудистых пространствах, что приводит к увеличению внесосудистой гипергидратации вообще и интерстициальному отеку легких в частности. В связи с этим представляется крайне опасной инфузия растворов альбумина (отек легких), низко- и среднемолекулярных декстранов и растворов желатина (фибринолиз, изменение активности фактора VIII, декстраниндуцированная ангиопатия и т. д.). Единственным показанием для трансфузии плазмы является необходимость борьбы с нарушениями свертываемости крови.
Для проведения инфузионной терапии необходимо использовать растворы кристаллоидов и гидроксиэтилированного крахмала (Рефортан®). При эффективных значениях онкотического давления эти растворы обладают высокой молекулярной массой, что в условиях повышенной проницаемости эндотелия предопределяет преимущества их использования перед альбумином, плазмой и декстранами. Растворы гидроксиэтилированного крахмала (ГЭК) способны «запечатывать» поры в эндотелии, появляющиеся при разных формах его повреждения. Исходя из этого препаратами выбора при проведении инфузионной терапии у беременных с крайне низкими показателями онкотического давления являются растворы ГЭК с высокой молекулярной массой 450 000 Д и степенью замещения 0,7, относящиеся к фармакологической группе «Hetastarch» (Стабизол®).
АНЕСТЕЗИЯ
Эклампсия – это не синоним кесарева сечения. Если судороги не повторяются, состояние больной стабилизировалось, родовые пути готовы – возможно родоразрешение через естественные родовые пути. В этих условиях эпидуральная аналгезия (ЭАн) является методом выбора, так как позволяет стабилизировать состояние сердечно-сосудистой системы матери и уменьшает степень нарушений микроциркуляции, что в свою очередь улучшает маточно-плацентарный кровоток.
Условия для проведения эпидуральной и спинальной анестезии и аналгезии при тяжелой преэклампсии и эклампсии:
- Надежный контроль судорожной активности.
- Нормальное внутричерепное давление.
- Отсутствие симптомов неврологического дефицита.
- Контролируемое артериальное давление.
- Нормальные показатели свертывающей системы (тромбоциты
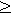 100 ? 106/ л).
100 ? 106/ л). - Отсутствие признаков острого нарушения состояния плода.
Наличие эклампсии не может рассматриваться как противопоказание к проведению ЭАн. Тем не менее ЭАн в этих условиях опасна развитием артериальной гипотонии. Артериальная гипотония может привести к гипоперфузии в области маточно-плацентарного кровотока и ухудшить состояние плода. В связи с этим ЭАн в родах должна обязательно сопровождаться кардиотокографией. Для проведения эпидуральной аналгезии используются растворы местных анестетиков (см. табл.) с добавлением разрешенных наркотических анальгетиков (морфин, фентанил).
Местные анестетики при эпидуральной аналгезии в родах: фракционное введение и постоянная инфузия

Риск развития отека легких (в особенности в послеродовом периоде) заставляет крайне осторожно относиться к стандартному болюсу введения жидкости перед проведением процедуры. Наиболее целесообразно в каждом конкретном случае решать вопрос об объеме инфузионной терапии на основании эхокардиографического исследования конечно-диастолического объема и показателя гематокрита. В случае необходимости проведения терапевтической гемодилюции перед выполнением эпидуральных или спинальных методов обезболивания у больных эклампсией также наиболее эффективно и безопасно использование 250–500 мл растворов ГЭК крупной молекулярной массы (Стабизол®). Не следует игнорировать и такие меры профилактики, как тугое бинтование нижних конечностей эластичными бинтами и устранение аортокавальной компрессии. Назначение вазопрессоров с профилактической или лечебной целью нежелательно, поскольку у больных преэклампсией имеется повышенная чувствительность к симпатомиметическим аминам.
Инструментальное и оперативное родоразрешение – нередкий результат попыток провести у этих женщин роды консервативно. Следовательно, возможность расширения уже существующего эпидурального блока является в этих ситуациях идеальным методом обезболивания.
На устройство для дозированного введения медикаментов должна быть обязательно наклеена бирка с указанием того, что лекарства вводятся в эпидуральное пространство, и точно обозначена скорость введения. Персонал родильного зала может спутать магистрали для эпидурального введения с теми, через которые проводится внутривенная инфузия, что особенно опасно в тех учреждениях, где дозирующие устройства используются для инфузии окситоцина.
При общей анестезии в дополнение к общепринятым мерам безопасности (ликвидация аортокавальной компрессии, неприемлемость гипервентиляции, профилактика аспирационных осложнений) нужно помнить и о специфических опасностях, которые присущи больным с эклампсией:
- отек верхних дыхательных путей;
- АГ при ларингоскопии;
- взаимодействие сульфата магния с препаратами, используемыми
при наркозе.
У больных эклампсией кривая диссоциации оксигемоглобина смещается влево. Это создает условия, предрасполагающие к развитию гипоксии. В связи с этим в родах, во время родоразрешения и в послеродовом периоде необходимо проводить оксигенотерапию. Перед интубацией трахеи обязательно проводить преоксигенацию. Интубацию трахеи затрудняет отек голосовых связок и ротоглотки. Из-за отека могут быть уменьшены размеры входа в трахею, поэтому всегда следует иметь наготове интубационные трубки меньшего размера. Трудности увеличиваются в особенности после травматизации вследствие предыдущих безуспешных попыток или рваной раны языка после судорог. Необходимо иметь наготове все для выполнения коникотомии или трахеостомии. Назотрахеальная интубация в этих случаях опасна развитием носового кровотечения.
Очень важно на этапе интубации трахеи контролировать уровень АД. Резкое увеличение артериального давления при интубации трахеи может спровоцировать внутримозговое и субарахноидальное кровоизлияния, увеличение давления в легочной артерии, отслойку плаценты. Для профилактики и борьбы с этими нарушениями используют b-адреноблокаторы, лидокаин (100 мг за 3–5 мин до вводного наркоза), фентанил (6 мкг/кг). В то же время чрезмерно активное рвение в снижении АД может спровоцировать гипоперфузию в области маточно-плацентарного кровотока с развитием гипоксии плода, а также приступы эклампсии в послеоперационном периоде.
Вводный наркоз должен обеспечить стабилизацию гемодинамики матери и плода. Поддержание анестезии можно обеспечить смесью 50% закиси азота с кислородом. Концентрация закиси азота в смеси с кислородом после извлечения плода может быть увеличена до 70%. После извлечения плода используют диазепам и опиоиды. Сульфат магния увеличивает действие производных сукцинилхолина. В связи с этим необходимо уменьшать дозу сукцинилхолина до 1–1,5 мг/кг.
Коагулопатия в сочетании с нарушением сократительных свойств матки может привести к кровотечению. Для профилактики и борьбы с атоническими маточными кровотечениями можно использовать окситоцин. Тем не менее метилэргометрин у этих больных внутривенно лучше не вводить, так как он может провоцировать АГ, отек легких, нарушения зрения и судороги в послеродовом периоде. Безопасность применения простогландина F2a и его дериватов у больных с тяжелой формой
преэклампсии и эклампсии пока изучена недостаточно.
ПОСЛЕОПЕРАЦИОННЫЙ ПЕРИОД
После операции кесарева сечения, произведенной на фоне эклампсии, ИВЛ необходимо продолжить не менее 24 часов. В этот период, так же как и в начале проведения интенсивной терапии, необходимо использовать принудительный режим вентиляции, а не вспомогательные режимы (ВВЛ), увеличивающие работу дыхания. Режим вентиляции должен обеспечить напряжение углекислоты в конечной пробе выдыхаемого воздуха ![]() в пределах 28–32ммрт. ст. Преждевременный перевод на ВВЛ
или самостоятельное дыхание часто является причиной возникновения
повторных судорожных припадков и осложнений. В большинстве случаев
при эклампсии удается добиться перевода на спонтанное дыхание в тече
ние 12–24 часов. Если ИВЛ проводили более 6–7 суток, прекращать респираторную поддержку можно только при отсутствии судорожных припадков и судорожной готовности без применения противосудорожныхпрепаратов (ПСП) в течение 3 суток. Основные критерии для перевода на самостоятельное дыхание и экстубации больных с эклампсией:
в пределах 28–32ммрт. ст. Преждевременный перевод на ВВЛ
или самостоятельное дыхание часто является причиной возникновения
повторных судорожных припадков и осложнений. В большинстве случаев
при эклампсии удается добиться перевода на спонтанное дыхание в тече
ние 12–24 часов. Если ИВЛ проводили более 6–7 суток, прекращать респираторную поддержку можно только при отсутствии судорожных припадков и судорожной готовности без применения противосудорожныхпрепаратов (ПСП) в течение 3 суток. Основные критерии для перевода на самостоятельное дыхание и экстубации больных с эклампсией:
- полное восстановление сознания;
- отсутствие судорожных припадков и судорожной готовности без применения ПСП;
- прекращение действия препаратов, угнетающих дыхание (миорелаксанты, наркотические аналгетики, гипнотики и т. д.);
- возможность самостоятельно удерживать голову над подушкой не менее 5 сек;
- стабильное и легко управляемое состояние гемодинамики;
- концентрация гемоглобина не менее 80 г/л;
- SaO2
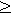 95%, PaO2
95%, PaO2 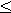 80ммрт. ст. при FiO2
80ммрт. ст. при FiO2 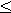 0,4 (PaO2/FiO2
0,4 (PaO2/FiO2 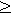 200);
200); - восстановление кашлевого рефлекса.
В послеоперационном и послеродовом периоде у больных с эклампсией необходим тщательный мониторинг. Сохраняется риск развития отека легких вследствие прогрессирующего снижения онкотического давления плазмы (КОДп). Максимальное снижение КОДп приходится на период между 6 и 16 часами послеродового (послеоперационного) периода. В этот период в программу инфузионной терапии необходимо включать препараты, обеспечивающие поддержание нормальных параметров онкотического давления плазмы. Учитывая сохраняющееся генерализованное повреждение эндотелия, препаратами выбора являются растворы кристаллоидов и ГЭК высокой молекулярной массы (Стабизол®). Единственными показаниями к назначению растворов глюкозы являются необходимость проведения парентерального питания и риск гипогликемии. Как можно раньше необходимо стремиться к переводу больных на энтеральное питание. Оптимальным является использование препаратов, адаптированных для питания беременных женщин и кормящих матерей (Берламин® Модуляр и другие).
Критерии отмены магнезиальной терапии:
- Прекращение судорог.
- Отсутствие признаков повышенной возбудимости ЦНС (гиперрефлексия, гипертонус, судорожная готовность).
- Нормализация артериального давления (ДАД
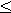 90ммрт. ст.).
90ммрт. ст.). - Нормализация диуреза (
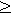 50 мл/ч).
50 мл/ч).
Выбор метода послеоперационного обезболивания должен основываться на конкретной клинической ситуации. Нет противопоказаний практически для всех методов послеоперационной аналгезии (эпидуральное введение опиоидов и местных анестетиков). Время пребывания в палате интенсивной терапии зависит от сроков разрешения критической ситуации.
НАИБОЛЕЕ РАСПРОСТРАНЕННЫЕ ОШИБКИ В ПРОВЕДЕНИИ ИНТЕНСИВНОЙ ТЕРАПИИ
И АНЕСТЕЗИОЛОГИЧЕСКОГО ПОСОБИЯ
Диагностика
- Толкование любого судорожного синдрома как проявление эклампсии.
- Недооценка тяжести больных с тяжелой формой преэклампсии в послеоперационном и послеродовом периоде.
- Несвоевременная диагностика HELLP-синдрома.
- Нераспознанные симптомы преждевременной отслойки плаценты и внутреннего кровотечения.
- Недооценка объема кровопотери.
- Неправильно принятое решение о транспортировке.
Интенсивная терапия
- Неполноценный венозный доступ (работа с «иглой в вене»).
- Начало интенсивной терапии с катетеризации центральной вены на фоне продолжающихся судорожных припадков.
- Чрезмерное рвение в снижении АД (ятрогенная эклампсия).
- Акцент на антигипертензивной и седативной терапии при недостаточном введении сульфата магния.
- Попытка справиться с судорожным синдромом введением больших доз оксибутирата натрия.
- Использование для управляемой гипотонии нитроглицерина.
- Применение осмотических диуретиков.
- Введение гепарина на фоне тяжелой артериальной гипертензии и тромбоцитопении.
Магнезиальная терапия
- Неправильный выбор насыщающей дозы.
- Передозировка сульфата магния (чаще при олигоанурии).
- Внутримышечные инъекции сульфата магния на фоне развившегося судорожного припадка.
- Преждевременный переход от постоянного внутривенного введения сульфата магния на внутримышечные инъекции.
Инфузионная терапия
- Инфузия альбумина и низкомолекулярных декстранов до родоразрешения (может провоцировать отек легких).
- Быстрая и массивная инфузионная терапия.
- Избыточное введение инфузионных сред в послеоперационном периоде.
- Включение в состав инфузионной терапии растворов глюкозы.
Искусственная вентиляция легких
- Преждевременный перевод на спонтанную вентиляцию.
- Отек гортани.
- Аспирация и регургитация желудочного содержимого.
- Использование режимов избыточной гипервентиляции в периоперационном периоде.
- Баро- и волотравма.
- Неадекватная санация трахеобронхиального дерева.
- Отсоединение больной от аппарата.
Анестезия
- Неустраненный синдром аортокавальной компрессии перед операцией кесарева сечения или во время родоразрешения.
- Недостаточная профилактика аспирационных осложнений.
- Поверхностный уровень анестезии до извлечения плода.
- Недостаточная защита от гемодинамических эффектов, возникающих при ларингоскопии.
- Неэффективное обезболивание родов у больных тяжелой формой преэклампсии и эклампсии.
- Небрежное ведение медицинской документации.

