Миорелаксанты при интубации трахеи во время индукции общей анестезии для кесарева сечения: расслабляться пока рано! Десять вопросов и ответов
Neuromuscular blockers for intubation during the induction of general anesthesia for caesarean section: relax is too early! Ten questions and answers
Резюме
Статья посвящена вопросам выбора миорелаксантов для интубации трахеи при индукции общей анестезии при кесарева сечении, особенностям их применения, препаратам для реверсии нервно-мышечной блокады и осложнениям при их использовании.
Ключевые слова: миорелаксанты, кесарево сечение, общая анестезия
Подходит к концу 2020 год, многим он запомнится пандемией новой коронавирусной инфекции COVID-19, которая внесла в наш размеренный уклад жизни заметные изменения как в социальной сфере, так и в медицинской помощи, проверив ее на прочность. На мой взгляд, мы (Россия) прошли эту проверку, нашли слабые места в системе здравоохранения и выработали планы по их устранению. Вместе с тем, ранее подписанный указ Президента РФ был опубликован на сайте Министерства здравоохранения РФ, который сделал обязательной цифровую маркировку лекарств с 1 июля 2020 года [1]. Однако не все производители лекарственных препаратов успели подготовиться к новым правилам производства, а некоторые и вовсе решили уйти с рынка лекарственных препаратов РФ.
В сегодняшней статье мы хотим уделить внимание группе лекарственных препаратов, без которых не может пройти ни одна операция под общей анестезией, - это миорелаксанты. Они используются как при интубации трахеи во время индукции общей анестезии, так и в палате интенсивной терапии в случае перевода пациента на искусственную вентиляцию легких (ИВЛ). Практические аспекты их применения относятся не только к акушерской анестезиологии, но именно в работе с беременными пациентками имеются свои уникальные особенности.
Вопрос 1. Какие миорелаксанты есть в нашем арсенале для интубации трахеи во время индукции общей анестезии при операции кесарева сечения (КС)?
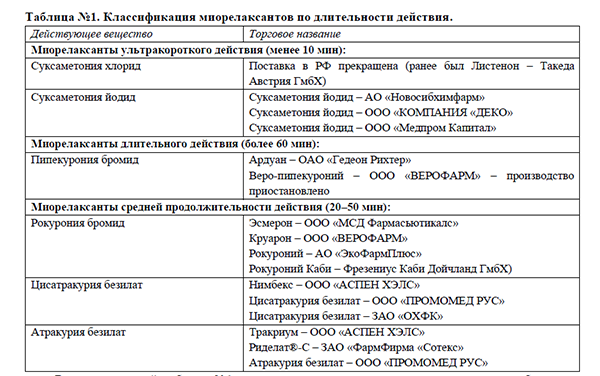
На территории РФ имеются различные виды миорелаксантов, в зависимости от механизма и длительности их действия (таблица №1).
В представленной таблице №1 мы указали все препараты, которые можно приобрести на территории РФ в декабре 2020 года. Возможно, в 2021 году появятся новые компании, которые будут поставлять миорелаксанты.
Вопрос 2. В чем основные отличия между этими миорелаксантами?
Деполяризующие миорелаксанты обладают быстрым началом действия (30 сек) и короткой продолжительностью. Недеполяризующие миорелаксанты в стандартной индукционной дозе обладают более длительным началом действия (90 сек) и большей продолжительностью.
Идеальный миорелаксант и его доза для интубации при операции кесарева сечения должны соответствовать следующим критериям:
- вызывать миоплегию для интубации в максимально короткое время после введения;
- обладать быстрым периодом полувыведения или иметь антидот для реверсии нервно-мышечного блока.
Еще одним методом ускорения наступления миоплегии для интубации трахеи при использовании рокурония бромида (недеполяризующего миорелаксанта), является прайминг - введение 10% от расчетной интубационной дозы до анестетика, а остальное после окончания индукции, что, в среднем, сокращает время действия препарата на 20 с [2].
Вопрос 3. Какие миорелаксанты чаще применяются для интубации трахеи во время индукции общей анестезии при операции КС?
Долгое время препаратом выбора был деполяризующий миорелаксант - суксаметония хлорид (в РФ часто использовался Листенон), но после прекращения его поставок на территорию РФ заменить его стало невозможно. Таким образом, на сегодняшний день остается для использования деполяризующий миорелаксант суксаметония йодид
В основном деполяризующие миорелаксанты применяются не для интубации трахеи при общей анестезии, а для ее поддержания. Современные тенденции в выборе миорелаксантов все чаще обращают внимание на применение препаратов средней продолжительности действия в акушерской анестезиологии, в основном, применяя при миоплегии для интубации рокурония бромид [3-5]. Конечно, есть статьи о применении цисатракурия безилата, атракурия безилата, но их мало [6, 7], и опубликованные практики разных стран показывают, что рутинно для миоплегии при индукции общей анестезии применяют рокурония бромид. Вместе с этим, каждый препарат имеет свою уникальную инструкцию с показаниями и противопоказаниями к применению, поэтому при использовании любого препарата необходимо сначала ознакомиться с инструкцией.
Вопрос 4. В чем основные особенности применения миорелаксантов для интубации трахеи во время индукции общей анестезии при операции КС?
Инструкции к большинству недеполяризующих миорелаксантов указывают необходимую дозу препарата для интубации у небеременных пациентов, когда не требуется быстрая последовательная индукция (RSI), то есть интубация может быть проведена в течение 2-3 минут после введения релаксанта и вентиляции с помощью лицевой маски до достижения хорошей миорелаксации. Дозы для RSI, необходимые в акушерстве, то есть интубация пациентки в течении 30-60 секунд после введения препарата с минимальной масочной вентиляцией, несколько больше обычно используемых у неакушерских пациентов.
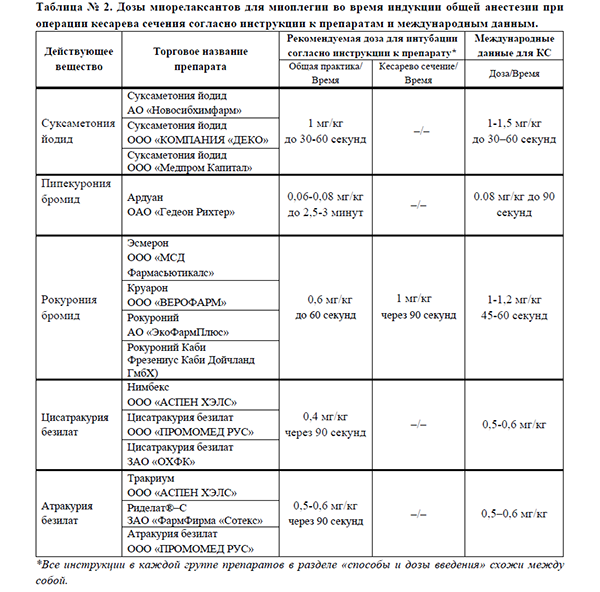
В таблице № 2 мы отразили рекомендуемые инструкцией к препаратам дозы миорелаксантов при интубации для максимально быстрой миоплегии и для миоплегии при операции кесарева сечения, а также дозы миорелаксантов, используемые в международной практике (опубликованных исследованиях и обзорах).
Вопрос 5. Почему необходимо максимально быстро интубировать беременную?
Существуют две основные особенности, почему необходимо быстро интубировать беременную пациентку.
Первая особенность связана с анатомо-физиологическими изменениями дыхательной системы беременной в доношенном сроке. Потребность в кислороде и продукция углекислого газа увеличивается до 60% во время беременности. Анатомические и физиологические изменения происходят для удовлетворения метаболических потребностей матери и плода. Происходит раннее увеличение дыхательного объема, что приводит к максимальному увеличению минутной вентиляции на 45% ко второму триместру, при этом частота дыхание увеличивается незначительно. Движущей силой этих изменений является прогестерон, который снижает порог чувствительности дыхательного центра к углекислому газу. Поскольку матка увеличивается, происходит смещение диафрагмы в краниальном направлении. Функциональная остаточная емкость легких (ФОЕЛ) уменьшается на 20% в вертикальном положении и до 30% в положении лежа на спине. Увеличение потребления кислорода и снижение ФОЕЛ означают, что у беременной может очень быстро развиться гипоксемия во время эпизода апноэ, несмотря на адекватную преоксигенацию. Увеличение минутной вентиляции и снижение ФОЕЛ способствует газообмену на уровне альвеол, что приводит к увеличению скорости поглощения ингаляционных анестетиков и более быстрым изменениям в глубине анестезии. При вентиляции беременной необходимо помнить о более низких уровнях, а также эквивалентах градиента между концом выдоха CO2 и РаСО2. Отсутствие градиента объясняется сокращением альвеолярного мертвого пространства (увеличение перфузии крови с увеличением материнского сердечного выброса). Чрезмерная гипервентиляция может привести к серьезному алкалозу и сдвигом диссоциации кривой кислорода влево, что приведет к снижению доставки кислорода к плоду [8].
Вторая особенность - это «полный желудок». Беременная с доношенным сроком должна рассматриваться, как пациент с полным желудком, а следовательно, ей необходимо провести RSI при интубации трахеи и максимально снизить риск аспирации и регургитации желудочным содержимым. Учитывая, что масочная вентиляция увеличивает риск аспирации у пациентов с «полным желудком», необходимо вводить миорелаксант в той дозе, которая вызовет максимально быструю миоплегию и снизит время проведения масочной вентиляции. Интересно, что ни в одних рекомендациях ни РФ, ни DAS/OAA (Общество трудных дыхательных путей и Общество акушерских анестезиологов Великобритании) не указывается на ограничение времени масочной вентиляции при индукции. Есть только упоминание об ограничении давления до 25 см вод. ст. [9] и минимальной по времени масочной вентиляции [10], целью которого является снижение риска регургитации и аспирации.
Вопрос 6. Какие существуют препараты и их дозы для реверсии нервно-мышечного блока?
Существует две фармакологические группы препаратов: селективный антидот миорелаксантов - сугаммадекс (Брайдан - ООО «МСД Фармасьютикалс») и ингибитор холинастеразы - неостигмина метилсульфат (Прозерин - АО «Новосибхимфарм», ОАО «ДАЛЬХИМФАРМ», ООО «АЛВИЛС»).
Сугаммадекс или Брайдан® (на данный момент на территории РФ нет аналогов этому препарату) был специально разработан для реверсии нервно-мышечного блока, вызванного рокуронием бромида. Согласно инструкции к препарату, стандартная доза сугаммадекса для реверсии нервно-мышечного блока в случае глубокой миорелаксации составляет 4 мг/кг, медиана времени для восстановления 4,7 мин (межквартильный интервал 1,2 - 16,1 мин); в случае средней нервно-мышечной блокады составляет 2 мг/кг, медиана времени для восстановления 1,4 мин (межквартильный интервал 0,9- 5,4 мин).
Высокая скорость восстановления при нервно-мышечном блоке любой глубины позволяет эффективно использовать сугаммадекс при необходимости быстрого устранения нейромышечной блокады сразу после введения рокурония [10]. Согласно инструкции к сугаммадексу для немедленной реверсии нервно-мышечного блока индуцированного рокуронием бромида 1,2 мг/кг необходимо ввести Брайдан® в дозе 16 мг/кг, медиана времени для восстановления 4,2 мин (межквартильный интервал 3,5 - 7,7 мин).
Неостигмина метилсульфат (Прозерин) выпускается различными компаниями на территории РФ, инструкции к препаратам, в основном, схожи между собой. Согласно инструкции к препаратам, предварительно вводят атропина сульфат 0,5 - 0,7 мг, затем неостигмина метилсульфат 1,5 мг (3 мл), если эффект от введения оказался недостаточным, можно повторить введение в той же дозе.
Вопрос 7. Возможна ли аллергическая реакция (анафилактический шок) на миорелаксанты?
В конце 2020 года были опубликованы данные популяционного многонационального европейского исследования по частоте и причинах анафилактического шока у беременных и рожениц [11]. Анализ был проведен в пяти европейских странах (Великобритания, Франция, Финляндия, Нидерланды, Бельгия). Основными причинами анафилаксии были антибиотики и анестетики, редко -миорелаксанты. Интересно отметить, что суксаметоний (был единственным миорелаксантом, используемым в популяционном многонациональном европейском исследовании, тогда как рокуроний был наиболее распространенным препаратом в NAP6). Результаты этого исследования были аналогичны результатам VI Национального аудиторского проекта Великобритании (NAP6); в частности, антибиотики и миорелаксанты были основными причинами анафилактического шока. Частота анафилаксии на суксаметония йодид была самой большой - 11,1/100 000 введений, затем на рокурония бромид - 5,88/100 000 и атракурия безилат - 4,15/100 000 введений [12]. Более того, в одном из ранее опубликованных исследований во Франции сообщалось, что миорелаксанты являлись основной причиной материнской смерти от анафилаксии [13].
В Новозеландском исследовании частота анафилаксии, вызванная суксаметонием, рокуронием и атракурия безилатом, составила 1:2079, 1:2498 и 1:7680-109 000 соответственно [14]. В Австралийском исследовании, оценивающем анафилаксию на миорелаксанты с 2002 по 2011 годы, наиболее частой причиной был суксаметоний. Однако, если рассматривать анафилаксию на недеполяризующие миорелаксанты, на первом месте был рокурония бромид с частотой 8,0/100 000 введений за 10-летний период (95% ДИ 5,8-11/100 000). Следующий по частоте был атракурия безилат - 4,01/100 000 (95% ДИ 1,6-8,3/100 000) [15]. Случаев анафилаксии на цисатракурия безилат не было диагностировано, как и в исследовании NAP6.
В любом случае, выбор миорелаксанта для интубации должен основываться не столько на риске развития анафилаксии, сколько на его механизме действия и противопоказаниях, с одновременным соблюдением клинических рекомендаций Министерство здравоохранения «Анафилактический шок в акушерстве» [10] и ФАР «Анафилактический шок» [16] для своевременной диагностики и лечения анафилактического шока.
Вопрос 8. Возможна ли аллергическая реакция (анафилактический шок) на препараты для реверсии нервно-мышечного блока?
В литературных данных встречаются крайне редкие сообщения об анафилактических реакциях, напрямую связанных с неостигмином. В основном, это клинические случаи или серии из них. Напротив, опубликовано много исследований и статистических данных об анафилактических реакциях на сугаммадекс [17 - 19]. Однако количество сообщений об анафилаксии, вызванной сугаммадексом, намного меньше, чем от миорелаксантов [20].
В феврале 2020 года была опубликована большая работа японских специалистов [21], в которой проводился анализ 49 532 пациентов из четырех больниц третьего уровня с целью оценить и сравнить частоту анафилаксии между сугаммадексом и неостигмином. Сугаммадекс широко применяется в Японии: было выявлено 18 случаев анафилаксии, шесть из которых связаны с сугаммадексом (0,02%; 95% доверительный интервал [ДИ], 0,007-0,044%) и ни одного с неостигмином. Авторы предполагают, что неостигмин с гораздо меньшей вероятностью вызывает анафилаксию и что в японской практике следует пересмотреть выбор препарата для реверсии нервно-мышечного блока.
Стоит отметить, что точный механизм анафилаксии от одного сугаммадекса или комплекса сугаммадекс - рокуроний до сих пор не совсем ясен [22]. Необходимо всеми возможными способами снизить потенциальный риск анафилаксии от любого препарата. Использование препарата должно основываться на тщательной оценке показаний, и сугаммадекс не является исключением.
Единственный способ оправдать введение сугаммадекса и, в частности, его дозу - это объективный мониторинг уровня нервно-мышечной блокады (часто в практике применяется TOF-мониторинг). Существует мало данных, но некоторые исследования с добровольцами свидетельствуют о том, что риск анафилактической реакции на сугаммадекс увеличивается с увеличением дозы [23]. Это является еще одной причиной проводить мониторинг нервно-мышечной блокады во время операции при планируемом введении сугаммадекса.
Вопрос 9. Какой препарат лучше использовать для реверсии нервно-мышечного блока?
Недавний Кокрановский обзор показал, что, по сравнению с неостигмином, сугаммадекс способен быстрее реверсировать нервно-мышечную блокаду, вызванную рокуронием, независимо от глубины блока [24]. Этот эффект - быстрая реверсия в конце операции - довольно часто используется при большом потоке плановых оперативных вмешательств, для увеличения числа проводимых операций, что имеет выраженную экономическую эффективность [25]. Мультицентровое исследование STRONGER, данные которого были опубликованы в Июне 2020 года, включало 2856 пациентов, получивших сугаммадекс, и столько же Прозерин. Результаты исследования достоверно показали, что использование сугаммадекса снижает частоту послеоперационных легочных осложнений [26].
В любом случае Прозерин не может адекватно противодействовать глубокому нейромышечному блоку. Самое опасное, что уровень остаточного нейромышечного блока может быть недооценен или не распознан врачом, что приведет к преждевременной экстубации трахеи и создаст риск нарушения дыхания и неспособность пациента полностью контролировать секрецию верхних дыхательных путей. Введение сугаммадекса практически устраняет проблему остаточного нейромышечного блока [27, 28].
Учитывая частоту анафилаксии на сугаммадекс, необходимо тщательно взвешивать риск и пользу. Однако риск анафилаксии сам по себе не должен быть решающим фактором при выборе препарата для реверсии нервно-мышечного блока, и следует также учитывать многие другие преимущества сугаммадекса по сравнению с неостигмином, в основном, это время. Пока, Брайдан® - это единственный препарат для целенаправленной реверсии нервно-мышечного блока, вызванного рокуронием.
Вопрос 10. Особенности применения сугаммадекса в случае неудачной интубации трахеи?
В случае трудной интубации и развития сценария CICO («не могу интубировать, не могу оксигенировать/вентилировать») Прозерин не способен вызвать реверсию глубокого нейромышечного блока, вызванного высокими дозами недеполяризующих миорелаксантов (например, рокурония бромид). Напротив, высокие дозы сугаммадекса (в большинстве исследований использовалась доза 16 мг/кг) быстро и эффективно вызывают реверсию глубокого нейромышечного блока [29 - 31].
Опубликованные в 2015 году рекомендации Общества трудных дыхательных путей и Общества акушерских анестезиологов Великобритании, посвященные вопросам интубации трахеи в акушерстве [9], рекомендуют высокие дозы рокурония (1,0-1,2 мг/кг) в качестве альтернативы суксаметонию для RSI и интубация трахеи. В случае неудачной интубации и необходимости восстановления спонтанной вентиляции в рекомендациях указывается на преимущество более быстрого восстановления при полной реверсии нейромышечного блока после введения высоких доз сугаммадекса (16 мг/кг) по сравнению со спонтанным восстановлением дыхания после введения суксаметония. Возможность быстрого введения и наличие нескольких флаконов сугаммадекса во время этой экстренной ситуации, а также высокая стоимость препарата признаны его недостатками [9].
Следует отметить, что эта тактика при сценарии CICO у беременных рекомендуется в связи с отсутствием каких-либо больших опубликованных исследований на сегодняшний день. Кроме того, в рекомендациях не рассматриваются изменения в анатомии дыхательных путей из-за отека после нескольких попыток при трудной интубации, объемно инфузионной терапии при развитии послеродового кровотечения или при преэклампсии, что ставит под сомнение выбор высоких доз рокурония для быстрой последовательной индукции при экстренной интубации [32]. Еще один вопрос, на который нет ответа, касается потенциального трансплацентарного проникновения сугаммадекса и его эффектов на плод после введения беременной. Следует отметить, что введение сугаммадекса младенцам и новорожденным не рекомендуется в настоящее время [33, 34]. Таким образом, потенциальные эффекты сугаммадекса на развивающийся плод в настоящее время полностью не изучены, поэтому говорить о безопасности применения сугаммадекса во время беременности пока еще рано.
Однако, принимая во внимание риск и пользу использования сугаммадекса в случае развития сценария CICO, его введение перед выполнением хирургического доступа с передней поверхности шеи для обеспечения проходимости верхних дыхательных путей может быть эффективным.
Литература
- Сайт Минздрава РФ, интернет-ресурс: minzdrav.gov.ru/news/2020/07/01/14336-s-1-iyulya-tsifrovaya-markirovka-lekarstv-stala-obyazatelnoy
- Dong J, Gao L, Lu W, Xu Z, Zheng J. Pharmacological Interventions for Acceleration of the Onset Time of Rocuronium: A Meta-Analysis. PLoS ONE. 2014; 9(12): e114231.
- Desai N, Wicker J, Sajayan A, Mendonca C. A survey of practice of rapid sequence induction for caesarean section in England. Int J Obstet Anesth. 2018; 36: 3-10.
- Ikeda, T., Kato, A., Bougaki, M. et al. A retrospective review of 10-year trends in general anesthesia for cesarean delivery at a university hospital: the impact of a newly launched team on obstetric anesthesia practice. BMC Health Serv Res. 2020; 20: 421.
- Kosinova M.; Stourac P.; Seidlova D.; Adamus M.; Krikava I.; Pavlik T. RocSugIO Study Group. Effect of rapid sequence induction for caesarean section in general anaesthesia with rocuronium versus succinylcholine on neonatal outcome: prospective randomised interventional multicentric trial, European Journal of Anaesthesiology (EJA). 2014; 31: 190.
- Fang, X., Xiao, Q., Xie, Q. et al. General Anesthesia with the Use of SUPREME Laryngeal Mask Airway for Emergency Cesarean delivery: A Retrospective Analysis of 1039 Parturients. Sci Rep, 2018; 8: 13098.
- Hany Mohamed Mohamed El Zahaby, Abeer Mohammad Abdel Aziz El Deek. Reham Mostafa Hashim Kotb, Rabie Ahmed Sayed Rayan. Comparison between Intubating and Recovery Characteristics of Succinylcholine, Rocuronium and Atracurium in Parturients Undergoing Cesarean Sections. Nat Sci 2020; 18(2): 40-51.
- Ruth Bedson, Anna Riccoboni. Physiology of pregnancy: clinical anaesthetic implications, Continuing Education in Anaesthesia Critical Care & Pain. 2014; 14 (2): 69-72.
- Mushambi MC, Kinsella SM, Popat M, et al; Obstetric Anaesthetists’ Association; Difficult Airway Society. Obstetric Anaesthetists’ Association and Difficult Airway Society guidelines for the management of difficult and failed tracheal intubation in obstetrics. Anaesthesia. 2015; 70: 1286-1306.
- Анестезия, интенсивная терапия и реанимация в акушерстве и гинекологии. Клинические рекомендации. Протоколы лечения. Издание четвертое, дополненное и переработанное. Под редакцией А.В. Куликова, Е.М. Шифмана. - М.: Издательство «Буки Веди», 2019. - 928 с.
- McCall, S.J., Bonnet, M.P., Ayras, O., Vandenberghe, G., Gissler, M., Zhang, W.H., Van Leeuw, V., DeneuxTharaux, C., Kurinczuk, J.J., Knight, M., Anaphylaxis in pregnancy: a populationbased multinational European study. Anaesthesia, 2020; 75: 1469-1475.
- NAP6: Anaesthesia, Surgery and Life-Threatening Allergic Reactions
- Tacquard C, Chassard D, Malinovsky J-M, SaucedoM, Deneux - Tharaux C, Mertes PM. Anaphylaxis-related mortality in the obstetrical setting: analysis of the French National Confidential Enquiry into Maternal Deaths from 2001 to 2012. British Journal of Anaesthesia. 2019; 125: e151-3.
- Reddy JI, Cooke PJ, van Schalkwyk JM, Hannam JA, Fitzharris P, Mitchell SJ. Anaphylaxis is more common with rocuronium and succinylcholine than with atracurium. Anesthesiology. 2015;122(1):39-45.
- P. H. M. Sadleir, R. C. Clarke, D. L. Bunning, P. R. Platt, Anaphylaxis to neuromuscular blocking drugs: incidence and cross-reactivity in Western Australia from 2002 to 2011. BJA: British Journal of Anaesthesia. 2013; 110 (6): 981-987
- Н.И. Ильина, И.Б. Заболотских, Н.Г. Астафьева, А.Ж. Баялиева, А.В. Куликов, Т.В. Латышева, К.М. Лебединский, Т.С. Мусаева, Т.Н. Мясникова, А.Н. Пампура, Р.С. Фассахов, Л.Г. Хлудова, Е.М. Шифман. Анафилактический шок. Клинические рекомендации Российской ассоциации аллергологов и клинических иммунологов и Общероссийской общественной организации «Федерация анестезиологов и реаниматологов». Вестник интенсивной терапии им. А.И. Салтанова. 2020; 3: 15-26.
- Tsur A, Kalansky A. Hypersensitivity associated with sugammadex administration: a systematic review. Anaesthesia. 2014; 69(11): 1251-7.
- Miyazaki Y, Sunaga H, Kida K, Hobo S, Inoue N, Muto M, Uezono S. Incidence of Anaphylaxis Associated With Sugammadex. Anesth Analg. 2018 May;126(5):1505-1508.
- Gregory R.J., Woehlck H. & Lien C.A. Sugammadex and Hypersensitivity-Related Reactions: a Review. Curr Anesthesiol Rep. 2020; 10: 123-130.
- Baldo BA, McDonnell NJ. Sugammadex and anaphylaxis in the operating theater. Rev Esp Anestesiol Reanim. 2014; 61(5): 239-45.
- Orihara M, Takazawa T, Horiuchi T, Sakamoto S, Nagumo K, Tomita Y, Tomioka A, Yoshida N, Yokohama A, Saito S. Comparison of incidence of anaphylaxis between sugammadex and neostigmine: a retrospective multicentre observational study. Br J Anaesth. 2020; 124(2): 154-163.
- Honing G, Martini CH, Bom A, van Velzen M, Niesters M, Aarts L, Dahan A, Boon M. Safety of sugammadex for reversal of neuromuscular block. Expert Opin Drug Saf. 2019; 18(10): 883-891.
- de Kam PJ, Nolte H, Good S, Yunan M, Williams-Herman DE, Burggraaf J, Kluft C, Adkinson NF, Cullen C, Skov PS, Levy JH, van den Dobbelsteen DJ, van Heumen ELGM, van Meel FCM, Glassner D, Woo T, Min KC, Peeters PAM. Sugammadex hypersensitivity and underlying mechanisms: a randomised study of healthy non-anaesthetised volunteers. Br J Anaesth. 2018; 121(4): 758-767.
- Hristovska AM, Duch P, Allingstrup M, Afshari A. Efficacy and safety of sugammadex versus neostigmine in reversing neuromuscular blockade in adults. Cochrane Database Syst Rev. 2017; 8(8): CD012763.
- Деркач Е. В., Авксентьева М. В., Реброва О. Ю., Шифман Е. М., Игнатьева В. И. & Николаенко Э. М. Клинико-экономическая оценка использования сугаммадекса (Брайдан) для реверсии нейромышечного блока при проведении оперативных вмешательств. Медицинские технологии. Оценка и выбор. 2013; 3(13): 44-55.
- Kheterpal S, Vaughn MT, Dubovoy TZ, Shah NJ, Bash LD, Colquhoun DA, Shanks AM, Mathis MR, Soto RG, Bardia A, Bartels K, McCormick PJ, Schonberger RB, Saager L. Sugammadex versus Neostigmine for Reversal of Neuromuscular Blockade and Postoperative Pulmonary Complications (STRONGER): A Multicenter Matched Cohort Analysis. Anesthesiology. 2020; 132(6): 1371-1381.
- Partownavid P, Romito BT, Ching W, et al. Sugammadex: a comprehensive review of the published human science, including renal studies. Am J Ther. 2015; 22: 298-317.
- Abad-Gurumeta A, Ripollés-Melchor J, Casans-Francés R, et al; Evidence Anaesthesia Review Group. A systematic review of sugammadex vs neostigmine for reversal of neuromuscular blockade. Anaesthesia. 2015; 70: 1441-1452.
- Pühringer FK, Rex C, Sielenkämper AW, et al. Reversal of profound, high-dose rocuronium-induced neuromuscular blockade by sugammadex at two different time points: an international, multicenter, randomized, dose-finding, safety assessor-blinded, phase II trial. Anesthesiology. 2008; 109: 188-197.
- de Boer HD, Driessen JJ, Marcus MA, Kerkkamp H, Heeringa M, Klimek M. Reversal of rocuronium-induced (1.2 mg/ kg) profound neuromuscular block by sugammadex: a multicenter, dose-finding and safety study. Anesthesiology. 2007; 107: 239-244.
- Lee C, Jahr JS, Candiotti KA, Warriner B, Zornow MH, Naguib M. Reversal of profound neuromuscular block by sugammadex administered three minutes after rocuronium: a comparison with spontaneous recovery from succinylcholine. Anesthesiology. 2009; 110: 1020-1025.
- Richardson MG, Raymond BL. Sugammadex Administration in Pregnant Women and in Women of Reproductive Potential: A Narrative Review. Anesth Analg. 2020; 130(6): 1628-1637.
- Plaud B, Meretoja O, Hofmockel R, et al. Reversal of rocuronium-induced neuromuscular blockade with sugammadex in pediatric and adult surgical patients. Anesthesiology. 2009; 110: 284-294.
- Инструкция к препарату Брайдан. Сайт Государственный реестр лекарственных средств https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=9f03e82a-ac9b-49e7-b33a-765c3d8c704b&t=