Acta Anaesthesiol Scand 2005; 49: 1041—1047
E. SOREIDE1, L. I. ERIKSSON2, G. HIRLEKAR3, H. ERIKSSON4,
S. W. HENNEBERG 5, R. SANDIN 6, J. RAEDER 7
(Task Force on Scandinavian Pre-operative Fasting Guidelines,
Clinical Practice Committee Scandinavian Society of Anaesthesiology and Intensive Care Medicine)
1Department of Anaesthesia and Intensive Care, Stavanger University Hospital, Stavanger, Norway,
2Department of Anaesthesiology and Intensive Care, Karolinska University Hospital, Stockholm, Sweden,
3Department of Anaesthesia and Intensive Care, Akureyri Hospital, Akureyri, Iceland,
4Department of Anaesthesia and Intensive Care, Helsinki University Hospital, Helsinki, Finland,
5Department of Anaesthesia, Rigshospitalet, Copenhagen, Denmark,
6Department of Anaesthesiology and Intensive Care, Regional Hospital, Kalmar, Sweden
and 7Department of Anaesthesia, Ulleval University Hospital, Oslo, Norway
Правила предоперационной подготовки натощак: новые данные
Либеральные правила предоперационной подготовки натощак применяются в большинстве стран. В общем, чистую жидкость разрешено принимать не менее, чем за 2 часа до наркоза, а лёгкую пищу за 6 часов. Те же рекомендации применимы для детей и беременных, не рожающих женщин. Большинстве рекомендаций для детей младше 6 месяцев сейчас позволяют кормление грудью или молочной смесью не менее, чем за 4 часа до обезболивания. Недавно получила поддержку концепция предоперационного приёма пищи, состоящая в использовании специального богатого углеводами напитка, который, как было показано, не увеличивал объём и кислотность желудочного сока. Основываясь на доступной литературе, наша рабочая группа создала новые общепринятые Скандинавские правила предоперационной подготовки натощак. До сих пор не ясно, до какой степени возможно применение новых либеральных правил голодания для пациентов с функциональной диспепсией и такими системными заболеваниями как сахарный диабет. Другие всё ещё спорные вопросы касаются необходимости и влияния голодания на пациентов в неотложных случаях, на женщин в родах и на пациентов, подвергающимся различным процедурам под «глубокой седацией». Нам кажется, что необходимо глубже исследовать влияния различных режимов голодания на различные подгруппы пациентов, перед тем, как продвинуться на один шаг вперёд к полностью доказательным правилам предоперационной подготовки.
Принято к публикации 16 марта, 2005г.
Ключевые слова: анестезия; общая; содержимое желудка; опорожнение желудка; предоперационное голодание; осложнения лёгочной аспирации
Связанная с наркозом лёгочная аспирация, приводящая к дыхательной недостаточности (аспирационный пневмонит, синдром Мендельсона) была описана у хирургических пациентов и в плановых, и в неотложных случаях (1 – 7). Перед хирургическими операциями пациентов заставляли соблюдать жёсткие правила подготовки натощак с надеждой уменьшить риск этого осложнения (8). Однако научная база для этих жёстких правил подготовки натощак пациентов в плановых случаях была оспорена и признана несуществующей (9 – 11). Основываясь на этих новых данных, некоторые национальные общества анестезиологов приняли более свободные правила, касающиеся проведения подготовки натощак, для чистых жидкостей (вода, прозрачные соки, кофе, чай) (12 – 17). Приём твёрдой пищи утром перед альтернативным хирургическим вмешательством всё ещё не рекомендуется.
В клинической практике всё ещё является предметом сомнения и колебания, до каких пределов предоперационная подготовка натощак в неотложных случаях имеет значение. Кроме того, также не ясно, в каких случаях необходимо сделать исключение из новых правил подготовки натощак для специфических групп пациентов с предполагаемым или подтверждённым поздним опорожнением желудка (16,17). Недавно был представлен новый метод предоперационной оптимизации в плановых случаях – приём углеводов (16, 18,19), но пока он не широко не введён в клиническую практику.
Цель этого обзора предоставить новые сведения о предоперационной подготовке натощак и желудочном содержимом как факторе риска лёгочной аспирации. Мы сделаем акцент на развитии и использовании новых и более свободных правил в клинической практике, но также осветим спорные вопросы, достойные дальнейшего изучения.
Факторы риска лёгочной аспирации, связанной с наркозом
Опорожнение желудка
Объём желудка взрослого человека приблизительно равен 1,5 л. Желудок можно разделить на две функциональные части, например проксимальную и дистальную (20). Проксимальная часть состоит из дна, кардии и верхней части тела желудка и является резервуаром проглоченной пищи, регулируя внутрижелудочное давление (адаптивная релаксация) и скорость опорожнения желудка. Дистальная часть (рис.1) желудка состоит из нижней части тела, привратника и прилежащей части. Сокращения дистальной части желудка смешивают более крупные частички твёрдой пищи с желудочным соком. Только достаточно маленькие частички (например, менее 1 мм в диаметре) могут попасть через привратник в двенадцатиперстную кишку.
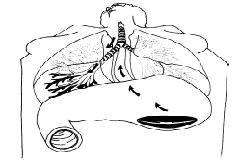 |
Рис. 1. Анатомические взаимоотношения между гастро-эзофагеальной частью пищеварительной системы и верхними дыхательными путями и лёгкими способствуют возникновению лёгочной аспирации вследствие регургитации или рвоты, когда пациент находится под наркозом. Ранее опубликовано в докторской диссертации Eldar Soreide «Анестезия и желудочное содержимое. Новые методы и направления» (1995г). Разрешение получено.
|
В нормальной ситуации на опорожнение желудка от жидкостей оказывают влияние градиент давления между желудком и двенадцатиперстной кишкой, а также объём, теплоёмкость, рН и осмолярность желудочного сока (20, 21). У так или иначе здоровых пациентов содержание желудочного сока не увеличивается сразу в предоперационном периоде, несмотря на теоретически негативное влияние беспокойства на опорожнение желудка (22, 23). Опорожнение желудка от воды или другой инертной, не термообразующей жидкости соответствует неимоверно крутой экспоненте со средним полупериодом равным 10 мин. (20, 21) (рис. 2). Первоначально, обогащённые глюкозой жидкости выходят несколько медленнее, но через 90 минут эта разница становится не значительной (20, 21, 23).
|
Рис. 2. Опорожнение желудка от твёрдой пищи (широкая пунктирная линия) и от чистой жидкости (тонкая линия). Ранее опубликовано в докторской диссертации Eldar Soreide «Анестезия и желудочное содержимое. Новые методы и направления» (1995г). Разрешение получено. |
Первоначально, обогащённые глюкозой жидкости выходят несколько медленнее, но через 90 минут эта разница становится не значительной (20, 21, 23). В противоположность этому, освобождение желудка от твёрдых частиц имеет линейную кривую (20, 21) (рис. 2 ). Опорожнение желудка от твёрдой пищи начинается приблизительно через час после еды. В течение 2 часов примерно 50 % проглоченной твёрдой пищи попадает в двенадцатиперстную кишку. Опорожнение желудка от твёрдой пищи не зависит от количества съеденной пищи, но зависит от её теплоёмкости. У женщин и пожилых опорожнение желудка происходит медленнее, чем у мужчин. Для того, чтобы желудок опорожнился от твёрдой пищи, необходимо более длительное голодание (24).
У новорождённых и младенцев прозрачные жидкости также выходят из желудка в первую очередь, а опорожнение от твёрдых частиц соответствует линейной кривой (25). Для опорожнения желудка от женского молока у доношенных новорождённых и младенцев недостаточно 2 часа, для этого требуется по крайней мере 3 часа (26). Оптимальный период голодания после приёма женского молока не установлен, но он составляет от 2 до 5 часов. У недоношенных детей более медленная скорость опорожнения желудка, а коровье молоко переваривается медленнее, чем женское (26). Время опорожнения желудка от молочных смесей зависит от состава смеси. Необходимо знать, что существуют довольно большие различия между разными регионами и странами в составе молочных смесей. Большинство детских анестезиологов сейчас используют тот же 2-часовой лимит для чистых жидкостей, как и у взрослых, и рекомендуют от 4 до 6 часов голодания после кормления грудью или молочной смесью с меньшими ограничениями у детей младше 6 месяцев (25).
Позднее опорожнение желудка бывает в многочисленных случаях, которые могут быть разделены по этиологии на нарушения в нормальной физиологии, стадия болезни и приём внешних агентов, либо лекарств либо препаратов, допускающих злоупотребление. Хорошо известно, что боль и опиоидные препараты вызывают задержку опорожнения желудка (20, 24). Также известно, что некоторые системные заболевания способствуют замедлению опорожнения желудка: из них в особенности сахарный диабет (27). Диабет действительно влияет на опорожнение желудка, больше от твёрдых частиц, чем от жидкостей (20, 27). Местный гастроинтестинальный стаз (опухоль или обструкция ) могут оказывать тот же эффект.
Время опорожнения желудка от твёрдых частиц удлиняется у курильщиков и не меняется у использующих никотиновые пластыри (28, 29). У злостных курильщиков, даже воздерживающихся от курения, имеется маленькое, но статистически значимое увеличение объёма желудочного сока по сравнению с не курящими людьми (30). Вопрос о том, до какого предела курение влияет на опорожнение желудочного сока и его объём, ещё спорный, но в общем кажется есть важные аргументы в пользу прекращения курения прямо перед наркозом (24,30,31). Злоупотребление каннабиноидами (32) для развлечения и высокие дозы алкоголя (33) также угнетают опорожнение желудка. Функциональная диспепсия (34 – 36) также ассоциирована с задержкой опорожнения желудка. У пациентов с ожирением опорожнение желудка кажется не отличается от такового у пациентов без ожирения, и предоперационный приём жидкости не увеличивает объёма содержимого желудка (37). Исследования влияния женских гормонов на опорожнение желудка имели различные результаты (20, 24). У беременных женщин скорость опорожнения желудка казалась нормальной, за исключением первого триместра, когда замедление предположительно происходит по гормональным причинам(38). В родах опорожнение желудка замедляется и остаётся замедленным, по крайней мере, ещё 2 часа после родов (39).
Метоклопрамид может улучшить опорожнение желудка у этих пациентов, но не может гарантировать опорожнение от желудочного содержимого (24, 40). То же самое касается пациентов с болью и находящихся под обезболиванием опиодными препаратами.
Содержимое желудка и гастро-эзофагеальный рефлюкс
Объём и кислотность желудочного содержимого определяются желудочной секрецией, оральным приёмом веществ и опорожнением желудка (20,24). Для того, чтобы во время наркоза произошла пассивная регургитация и лёгочная аспирация, необходимо наличие определённого объёма желудочного содержимого. Исследования (41) показывают, что для взрослого пациента это составляет 200 мл. В других случаях у здоровых пациентов определяются намного меньшие объёмы (в диапазоне 10 – 30 мл) желудочного сока (9 – 11, 42). У нескольких пациентов могут быть обнаружены большие объёмы, до 200 мл, вне зависимости от приёма жидкости. Эти крайности, возможно представляют пациентов с не выявленным нарушением пищеварения, таким как функциональная диспепсия (34 – 36). У пациентов с гастро-эзофагеальным рефлюксом или в случаях рвоты даже меньший объём желудочного содержимого может подняться верх и попасть в трахею (2, 7, 43) (рис.1)
Факторы, зависящие от пациента и анестезиолога
Проблемы с проведением вентиляции часто ускоряют лёгочную аспирацию (3 – 7). Воздух, попадающий в желудок, сопротивление и кашель в связи с лёгкой анестезией могут быть причинами возникновения эпизодов гастро-эзофагеального рефлюкса. Пациенты с ожирением, пациенты с подтверждённой гастро-эзофагеально-рефлюксной болезнью и пациенты со сложными дыхательными путями особенно подвержены лёгочной аспирации, вне зависимости от содержимого их желудка. Kruger и др. (7) считали, что такие человеческие факторы в совокупности с недальновидным суждением по поводу выбора и выполнения анестезиологической методики являются наиболее важными предрасполагающими факторами для клинически-значимой лёгочной аспирации, а не нарушение предосторожностей по поводу подготовки натощак. Это, конечно, делает перспективным наш исторически чрезмерный акцент на содержимое желудка. Важно дифференцировать то, что происходит, когда вентиляционные манипуляции во время лёгкой стадии наркоза вызывают рвоту и эпизоды гастро-эзофагеального рефлюкса независимо от объёма содержимого желудка, и когда наркоз в ситуациях с заполненным желудком способствует расслаблению пищеводных сфинктеров и пассивному току (регургитации) желудочного содержимого в верхние дыхательные пути и лёгочной аспирации (2). Анестезиолог, вероятно, является таким же важным фактором, как и желудочное содержимое.
Новые правила предоперационной подготовки натощак
Клинически контролируемые исследования и мета- анализ
Многочисленные контролируемые исследования и мета-анализ привели к заключению, что у здоровых пациентов, которым планируется провести плановые оперативные вмешательства, пероральный приём воды или других чистых жидкостей (чай, кофе, содовая, яблочный и апельсиновый сок без мякоти) более чем за 2 часа перед введением в наркоз не увеличивает объём желудочного сока и кислотность (9 – 11, 15, 44). Исследования проводились на взрослых мужчинах и женщинах (совершеннолетних) и в разных странах (44). Поэтому, согласно принципам доказательной медицины (45), настоящее научное доказательство позволяет использовать рекомендацию 1 Уровня для более либеральных правил подготовки натощак, разрешающих приём прозрачных чистых жидкостей.
Правила национального анестезиологического общества
Основываясь на новых данных, большинство анестезиологических обществ теперь рекомендуют не более, чем 2-часовое голодание после приёма чистых жидкостей (вода, чай, кофе, фруктовые соки без мякоти) в альтернативных случаях, включающих и взрослых и детей и беременных, не рожающих женщин (12 – 17). Важно, что это не применимо для молока, любых других жиросодержащих жидкостей или твёрдых частиц. Не сообщается об осложнениях, связанных с новыми и более либеральными правилами подготовки натощак (44, 46). Период голодания после приёма твёрдой пищи должен быть не менее 6 часов для обеспечения существенной безопасности (47, 48). Кроме того, не все правила национальных обществ содержат информацию об использовании жевательной резинки, табака и лекарственных препаратов прямо в предоперационном периоде, хотя говорится об их влиянии на содержимое желудка. Использование и жевательной резинки и табака увеличивают объём содержимого желудка, но пока не ясно до каких пределов это увеличение является клинически значимым (30). В настоящий момент мы считаем, что их использование следует прекратить прямо в предоперационном периоде.
Новые Скандинавские правила
Наша рабочая группа стремилась к созданию единого, но не слишком детального практического руководства для предоперационной подготовки натощак для всех скандинавских стран. Мы заключили, что подходят основанные на настоящих знаниях, общие рекомендации по поводу 2-часового голодания после приёма жидкости и 6-часового после приёма твёрдой пищи для так или иначе здоровых пациентов в несрочных случаях (табл. 1).
Таблица 1. Скандинавские правила предоперационной подготовки пациентов
натощак в несрочных случаях
- Пациенты ( как взрослые, так и дети) могут принимать чистую жидкость не менее, чем за 2 часа до общей или местной анестезии. - Пациенту не следует принимать твёрдую пищу за 6 часов перед введением в наркоз - Кормление грудью следует прекратить за 4 часа перед введением в наркоз. То же самое касается молочных смесей - Взрослые могут принять до 150 мл воды с пероральной премедикацией не менее, чем за 1 час до введения в наркоз, дети – до 75 мл - Использование жевательной резинки или табака в любой форме следует отменить в течение последних 2 часов перед введением в наркоз. |
Эти правила также применимы для плановых операций кесарева сечения. К чистым жидкостям относятся неструктурные жидкости без жира, например, вода, прозрачный фруктовый сок, чай или кофе. И коровье и сухое молоко относятся к твёрдой пище К пациентам с известной или предполагаемой задержкой опорожнения желудка (сахарный диабет, патология верхних отделов желудочно-кишечного тракта и её симптомы) необходим индивидуальный подход. |
Эти правила не противоречат и являются обоснованными для детей старше 1 года, взрослых и беременных, не рожающих женщин. Также как и остальные, к чистым жидкостям мы относим воду, чай, кофе, сок без мякоти и безалкогольные напитки, а также мы включаем углеводный напиток для предоперационного питания ( Nutricia Preop , Numico , The Netherlands ) (16, 19, 23). Ограничения касаются твёрдой пищи, включающей супы, йогурты, кефир и молочные продукты. Мы чувствовали, что с нашими Скандинавскими, выработанными общими усилиями правилами клинической практики не стоит вдаваться в детали, а оставить это национальным обществам. Вместо этого мы решили включить всё ещё спорные вопросы или темы, которые необходимо исследовать глубже.
Спорные вопросы темы будущих исследований
Группы пациентов, исключённые из либеральных правил подготовки натощак
В то время как новые, либеральные правила подготовки натощак можно безопасно использовать в большинстве плановых случаев, важно обратить внимание, что предоперационное голодание строго рекомендуется для всех неотложных случаев. Задержка опорожнения желудка в неотложных случаях может быть связана с влиянием боли само по себе, дачей опиоидов или желудочно-кишечной обструкцией (2, 24). Поэтому, запрет приёма пищи для этих пациентов никогда сделает их подготовленными «натощак и плановыми». То же самое касается беременных женщин в родах (50).
Существуют также плановые пациенты, у которых необходимо предполагать задержку опорожнения желудка. К ним относятся пациенты с желудочно-кишечной обструкцией в любом виде или раком в верхних отделах желудочно-кишечного тракта. Для пациентов с пищеводной грыжей существует высокий риск регургитации, и когда доходит дело до выбора анестезиологического пособия, их надо расценивать как «подверженных риску регургитации». Однако, нет явных доказательств более медленного опорожнения или больших остаточных объёмов желудка у этих пациентов (16, 17).
У пациентов с симптомами нарушений в верхних отделах желудочно-кишечного тракта при отсутствии органической патологии сильно превалируют задержка опорожнения желудка и гастропарез (34, 36). Поэтому, такие пациенты должны голодать после приёма твёрдой пищи больше, чем 6 часов. Однако, неизвестно, как долго. Хотя влияние опорожнения желудка от жидкости вероятно, намного меньше, для этих пациентов необходимы более контролируемые испытания (44).
У пациентов с системной патологией продолжительность опорожнения желудка высоко вариабельна и зависит от тяжести болезни (20, 27). Большинство исследований проводилось в отношении сахарного диабета, когда замедление опорожнения объяснялось полинейропатией с нарушением иннервации желудочно-кишечного тракта и основным заболеванием. До сих пор неизвестно, как долго пациентов с диабетом следует не кормить после полуночи, чтобы обеспечить безопасные колебания содержимого желудка. Диабет и другая медицинская патология больше влияют на опорожнение желудка от твёрдых частиц, чем от жидкостей (20, 24, 27). Возможно, для пациентов с системными заболеваниями также достаточно 2-часовго периода голодания после приёма чистой жидкости. Однако, необходимо провести больше исследований перед тем, как дать научно обоснованный ответ. В то же время , мы считаем, что мудро подстраховаться и принять консервативную позицию, когда дело касается голодания после приёма твёрдой пищи у этих пациентов.
У рожающих женщин очень удлиняется время опорожнения желудка (39) и повышается частота лёгочной аспирации по сравнению с другими группами пациентов (6). Несмотря на это, большинство родовых палат поощряют пероральный приём во время родов(50). Нам, как анестезиологам, может показаться, что это приведёт к обратным результатам, но для врачей-акушеров, акушерок и самих женщин небольшой риск проведения неотложного кесарева сечения под общим наркозом может не быть существенным аргументом в пользу не физиологичного голодания во время естественного процесса с огромными затратами энергии (50). Единственная уступка, на которую акушеры могут пойти, это позволить приём жидкости, а не твёрдой пищи во время родов. Решения, касающиеся правил подготовки натощак женщин в родах, принимаются без участия анестезиолога. Перед тем, как двигаться дальше в этом вопросе, нам нужно больше данных о действительной работе и возможных неблагоприятных эффектах Скандинавских методов родовспоможения.
Седативные препараты и необходимость голодания перед их применением.
Увеличивающееся число хирургических манипуляций выполняются с использованием «лёгкой, оставляющей в сознании и глубокой седации» в различных комбинациях с местной или региональной анестезией. Необходимо ли этим пациентам следовать правилам предоперационной подготовки натощак? Седативные и обезболивающие препараты имеют тенденцию к ослаблению рефлексов дыхательных путей в зависимости от степени достигнутой седации/анестезии (51,52). Доступная литература не обеспечивает достаточных доказательств того, что в результате голодания перед проведением процедур уменьшается частота неблагоприятных исходов у пациентов, подвергнутых либо умеренной, либо глубокой седации. Однако, Американское Общество Анестезиологов рекомендует пациентам, подвергающимся седации/обезболиванию во время плановых процедур, соблюдать те же предписания, которые соблюдаются пациентами в случае общего наркоза (52). Эти правила произвольны и основываются на единодушном мнении.
В неотложных ситуациях необходимо учитывать возможность лёгочной аспирации желудочного содержимого. Green и др. (51) обнаружили, что в медицинской литературе не описаны случаи лёгочной аспирации во время процедурной седации в неотложных отделениях. Однако существует мало доказательств для поддержки особых режимов подготовки натощак.
Steeds и Mather (53) изучили принципы предоперационной подготовки в глазной хирургии, производимой под местной анестезией. Пятьдесят процентов респондентов посчитали, что воздержание от приёма пищи не было необходимым, и упомянули гипогликемию, слабость, жажду, тошноту, головную боль и головокружение как осложнения длительного голодания. Maltby и Hamilton (54) не обнаружили ни одного случая лёгочной аспирации у 30000 пациентов, подвергнутых операциям на хрусталике под местной анестезией. Только в 1% случаев потребовалось применений седативных препаратов. С 1984г перед этой манипуляцией позволялось съесть завтрак. В то же время они предостерегали от глубокой седации и от перехода от местной блокады к общему наркозу. Большинство операций на глазах можно выполнить только под местной анестезией. Кажется, что предоперационная подготовка натощак обеспечивает пациенту за счёт его комфорта очень мало дополнительной безопасности. Послеоперационную рвоту, нежелательную после офтальмологических операций можно уменьшить укорочением предоперационного голодания. Кажется, что основными пунктами являются осведомление офтальмологов об опасностях глубокой седации после приёма пищи и создание частных правил, которые учитывают вид хирургии, вариант местной и региональной анестезии, необходимость седации и возможность перехода к общему обезболиванию при неудачном использовании местной анестезии. Мы чувствуем, что нужно больше данных по поводу настоящей практики использования седативных препаратов в плановых и неотложных случаях в Скандинавии перед тем, как мы сможем выработать специфические рекомендации предоперационной подготовки натощак в этих ситуациях.
Предоперационное голодание в противоположность приёму пищи
Также важны метаболические изменения при длительном голодании в противоположность коротким периодам воздержания от приёма пищи (18). Исследования указывают на то, что доступность углеводов и метаболическое состояние сытости являются важными факторами, ускоряющими выздоровление после операции (16). Главной целью предоперационного приёма углеводов является вызвать изменение обмена веществ, происходящее обычно после приёма завтрака. Это вызывает эндогенное высвобождение инсулина, что отключает в обмене веществ состояние голода, приобретённое за ночь. Исследовался богатый углеводами (12,5%) прозрачный напиток, содержащий в основном полимерные углеводы, который минимизировал осмотическую нагрузку и , таким образом, укорачивал время опорожнения желудка (23). 400 мл напитка проходило желудок через 90 мин и у здоровых добровольцев и у пациентов перед операцией. Исследования, проведённые более, чем на 250 пациентах, показали, что средний остаточный объём желудочного содержимого составляет всего лишь приблизительно 20 мл (16, 18). У маленькой группы пациентов этот объём составлял 120 мл, при самом высоком 200 мл. Когда 400-мл дозу разделили на 2 *200-мл с последним приёмом за 2 часа до гастроскопии, самый большой объём составлял 120 мл, при среднем объёме примерно 35 мл.
В исследованиях было обнаружено, что этот богатый углеводами предоперационный напиток и улучшает субъективное самочувствие по сравнению с применением плацебо (воды) и может положительно влиять на выздоровление после операции (16, 19). С точки зрения безопасности пациента важно заметить, что приём до 400 мл напитка не вызывает негативного влияния на содержимое желудка по сравнению с таким же приёмом воды ( 16, 24). Влияние перорального приёма жидкости на интраоперационное выделение мочи также следует включить в будущие исследования (42).
Выводы
Свободный приём чистой жидкости, включая специально созданный напиток, содержащий углеводы, не менее, чем за 2 часа перед наркозом в плановой хирургии, является безопасным и улучшает субъективное самочувствие. Новые Скандинавские правила делают акцент на то, что минимальное время голодания после приёма твёрдой пищи должно оставаться 6 часов. Воздержание от приёма пищи у неотложных пациентов не может обеспечить опорожнение желудка и не должно откладывать хирургические вмешательства. Нужно больше изучать предоперационную подготовку натощак и содержимое желудка у пациентов с системными заболеваниями, таких как сахарный диабет, и у пациентов с нарушениями в верхних отделах желудочно-кишечного тракта. В общем, выбор анестезиологического пособия и способа вентиляции лёгких оказывается таким же важным, как и строгое соблюдение любых правил голодания, когда дело касается уменьшения риска лёгочной аспирации.
Использованная литература
- Edwards G , Morton HJV , Pask EA , Wylie WD . Deaths associated with anaesthesia . A report on 1000 cases. Anaesthesia 1956; 11: 194—220.
- Bannister WK, Sattilaro AJ. Vomiting and aspiration during anesthesia. Anesthesiology 1962; 23: 251—64.
- Olsson GL, Hallen B, Hambraeus-Jonzon K. Aspiration during anaesthesia: computer-aided study of 185,358 anaesthetics. Acta Anaesthesiol Scand 1986; 30: 84—92.
- Mellin-Olsen J, Fasting S, Gisvold SE. Routine preoperative gastric emptying is seldom indicated. A study of 85,594 а naesthetics with special focus on aspiration pneumonia. Acta Anaesthesiol Scand 1996; 40: 1184—8.
- Warner MA, Warner ME, Weber JG. Clinical significance of pulmonary aspiration in the perioperative period. Anesthesiology 1993; 78: 56—62.
- Soreide E, Bjornestad E, Steen PA. An audit of Aspiration Pneumonitis in gynaecological and obstetric patients. Acta Anaesthesiol Scand 1996; 40: 14—9.
- Kluger MT, Short TG. Aspiration during anaesthesia: a review of 133 cases from the Australian Anaesthesia IncidentMonitoring Study (AIMS). Anaesthesia 1999; 54: 19—26.
- McIntyre JW. Evolution of 20th century attitudes to prophylaxis of pulmonary aspiration during anaesthesia. Can J Anaesth 1998; 45: 1024—30.
- Maltby JR, Sutherland AD, Sale JP, Shaffer EA. Preoperative oral fluids: is a five-hour fast justified prior to elective surgery? Anesth Analg 1986; 65: 1112—6.
- Philips S, Hutchinson S, Davidson T. Preoperative drinking does not affect gastric contents. Br J Anaesth 1993; 70: 6—9.
- Soreide E, Stromskag KE, Steen PA. Statistical aspects in studies of preoperative fluid intake and gastric content. Acta Anaesthesiol Scand 1995; 39: 738—43.
- Strunin L. How long should patients fast before surgery? Time for new guidelines (Editorial). Br J Anaesth 1993; 70: 1—3.
- Erikson LI, Sandin R. Fasting guidelines in different countries. Acta Anaesthesiol Scand 1996; 40: 971—4.
- Soreide E, Fasting S, R?der J. New preoperative fasting guidelines. Acta Anaesthesiol Scand 1997; 41: 799.
- American Task Force on Preoperative Fasting. Practice guidelines for preoperative fasting and the use of pharmacological agents to reduce the risk of pulmonary aspiration: application to healthy patients undergoing elective procedures. A report by the American Task Force on Preoperative Fasting. Anesthesiology 1999; 90: 896—905.
- Ljungqvist O, Soreide E. Preoperative fasting. Br J Surg 2003; 90: 400—6.
- Spies CD, Breuer JP, Wichmann M, Adolph M, Senkal M, Kampa U et al. Preoperative fasting. An update. Anaesthesist 2003; 52: 1039—45.
- Soop M, Nygren J, Myrenfors Thorell A, Ljungqvist O. Preoperative carbohydrate treatment attenuates immediate postoperative insulin resistance. Am J Physiol 2001; 280: E576—E583.
- Hausel J, Nygren J, Lagerkranser M, Hellstro?m PM, Hammarqvist F, Lindh A et al. A carbohydrate rich drink reduces preoperative discomfort in elective surgery patients. Anesth Analg 2001; 93: 1344—50.
- Read NW, Houghton LA. Physiology of gastric emptying and pathophysiology of gastroparesis. Gastroenterol Clin North Am 1989; 18: 359—73.
- Brener W, Hendrix TR, McHugh R. Regulation of the gastric emptying of glucose. Gastroenterology 1983; 85: 76—82.
- Haavik P, Soreide E, Hofstad P, Steen PA. Does preoperative anxiety influence gastric fluid volume and acidity? Anesth Analg 1992; 75: 91—4.
- Nygren J, Thorell A, Jacobsson H, Schnell PO, Ljungqvist O. Preoperative gastric emptying: the effects of anxiety and carbohydrate administration. Ann Surg 1995; 222: 728—34.
- Petring OU, Blake DW. Gastric emptying in adults: an overview related to anaesthesia. Anaesth Intensive Care 1993; 21: 774—81.
- Cote CJ. Preoperative preparation and premedication. Br J Anaesth 1999; 83: 16—28.
- Litman RS, Wu CL, Quinlivan JK. Gastric volume and pH in infants fed clear liquids and breast milk prior to surgery. Anesth Analg 1994; 79: 407—9.
- Horowitz M, O'Donovan D, Jones KL, Feinle C, Rayner CK, Samsom M. Gastric emptying in diabetes: clinical significance and treatment. Diabet Med 2002; 19: 177—94.
- Scott AM, Kellow JE, Shuter B, Nolan JM, Hoschl R, Jones MP. Effects of cigarette smoking on solid and liquid intragastric distribution and gastric emptying. Gastroenterology 1993; 104: 410—6.
- Wong PW, Kadakia SC, McBiles M. Acute effect of nicotine patch on gastric emptying of liquid and solid contents in healthy subjects. Dig Dis Sci 1999; 44: 2165—71. E. Soreide et al. 1046
- Soreide E, Veel T, Holst-Larsen H, Steen PA. The effects of chewing gum on gastric content р rior to induction of anesthesia. Anesth Analg 1995; 80: 985—9.
- Schumacher A, Vagts DA, Noldge-Schomburg GF. Smoking and preoperative fasting — are there evidence-based guidelines? Anaesthesiol Reanim 2003; 28: 88—96.
- Pertwee RG. Cannabinoids and the gastrointestinal tract. Gut 2001; 48: 859—67.
- Bujanda L. The effects of alcohol consumption upon the gastrointestinal tract. Am J Gastroenterol 2000; 95: 3374—82.
- Brock-Utne JG, Moshal MG, Downing JW, Spitaels JM, Stiebel R. Fasting Volume and acidity of stomach contents associated with gastrointestinal symptoms. Anaesthesia 1977; 32: 749—52.
- Hveem K, Hausken T, Berstad A. Ultrasonographic assessment of fasting liquid content in the human stomach. Scan J Gastroenterol 1994; 29: 786—9.
- Stanghellini V, Tosetti C,Horowitz M, De Giorgio R, Barbara G, Cogliandro R et al. Predictors of gastroparesis in outpatients with secondary and idiopathic upper gastrointestinal symptoms. Dig Liver Dis 2003; 35: 389—96.
- Maltby JR, Pytka S, Watson NC, Cowan RA, Fick GH. Drinking 300 mL of clear fluid two hours before surgery has no effect on gastric fluid Volume and pH in fasting and non-fasting obese patients. Can J Anaesth 2004; 51: 111—5.
- Levy DM, Williams OA, Magides AD, Reilly CS. Gastric emptying is delayed at 8—12 weeks' gestation. Br J Anaesth 1994; 73: 237—8.
- Whitehead EM, Smith M, Dean Y, O'Sullivan G. An evaluation of gastric emptying times in pregnancy and the puerperium. Anaesthesia 1993; 48: 53—7.
- Olsson GL, Hallen B. Pharmacological evacuation of the stomach with metoclopramide. Acta Anaesthesiol Scand 1982; 26: 417—20.
- Tryba M, Zenz M, Mlasowsky B, Huchzermeyer H. Does a stomach tube enhance regurgitation during general anaesthesia. Anaesthesist 1983; 32: 407—9.
- Soreide E, Holst Larsen H, Reite K, Mikkelsen H, Soreide JA, Steen PA. The effects of giving 25—450 ml of water with diazepam premedication 1—2 hours before general anesthesia. Br J Anaesth 1993; 71: 503—6.
- Vanner RG, Goodman NW. Gastro-oesophagal reflux in pregnancy at term and after delivery. Anaesthesia 1989; 44: 808—11.
- Brady M, Kinn S, Stuart P. Preoperative fasting for adults to prevent perioperative complications. In. Cochrane Database Syst Rev 2003;(4). Hoboken: John Wiley & Sons, 2003.
- Sackett DL, Straus SE, Richardson WS, Rosenberg W, Haynes RB. Evidence-Based Medicine. How to Practice and Teach EBM. New York: Churchill Livingstone, 2000.
- Fasting S, Soreide E, R?der J. Changing preoperative fasting policies. Does national consensus help? Acta Anaesthesiol Scand 1998; 42: 1188—92.
- Soreide E, Hausken T, Soreide JA, Steen PA. Gastric emptying of a light hospital breakfast. A study using ultrasonography. Acta Anaesthesiol Scand 1996; 40: 549—53.
- Brock-Utne JG. Clear fluids, not breakfast, before surgery. Acta Anaesthesiol Scand 1996; 40: 507—8.
- Maltby JR, Koehli N, Ewen A, Shaffer EA. Gastric fluid volume, pH, and gastric emptying in elective inpatients. Influences of narcotic-atropine premedication, oral fluid, and ranitidine. Can J Anaesth 1988; 35: 562—6.
- Scrutton MJ, Metcalfe GA, Lowy C, Seed PT, O'Sullivan G. Eating in labour. A randomised controlled trial assessing the risks and benefits. Anaesthesia 1999; 54: 1017—9.
- Green SM, Krauss B. Pulmonary aspiration risk during emergency department procedural sedation — an examination of the role of fasting and sedation depth. Acad Emerg Med 2002; 9: 35—42.
- The American society of Anesthesiologists-Task Force on Sedation and Analgesia by Non-Anesthesiologists. Practice Guidelines for Sedation and Analgesia by Non-Anesthesiologists (Approved by the House of Delegates on October 17, 2001)
- [www.document]. URL http://www.asahq.org. [accessed on 20 February 2005].
- Steeds C, Mather SJ. Fasting regimens for regional ophthalmic anaesthesia. A survey of members of the British Ophthalmic Anaesthesia Society. Anesthesia 2001; 56: 638—42.
- Maltby JR, Hamilton RC. Preoperative fasting guidelines for cataract surgery under regional anaesthesia. Br J Anaesth 1993; 71: 167.
Address:
Professor Eldar Soreide
Department of Anaesthesia and Intensive Care
Division of Acute Care Medicine
Stavanger University Hospital
PO Box 8100
N-4068 Stavanger
Norway
e-mail: soed@sir.no


