Опыт использования 6% ГЭК 130/0,4 Волювена
в практике скорой медицинской помощи
К одним из наиболее опасных гиповолемических состояний, несущих непосредственную угрозу жизни больных уже на догоспитальном этапе (ДГЭ), относятся тяжелые травматические повреждения, а также кровотечения нетравматического генеза. При травматическом и/или геморрагическом шоке быстрое возмещение интравазальных потерь жидкости является важнейшей, патогенетически обусловленной задачей интенсивной терапии. При этом своевременность и полноценность инфузионно-трансфузионной терапии, проводимой на всех этапах оказания медицинской помощи, является основным фактором, определяющим развитие ранних, отсроченных и поздних осложнений у данного контингента больных. Учитывая интенсивность кровопотери, восполнение внутрисосудистого объема на ДГЭ должно обеспечиваться большим объемом инфузионной терапии, осуществляемой с высокой линейной скоростью.
Стандартная схема догоспитальной инфузионной терапии при травматических или нетравматических кровотечениях включает использование кристаллоидных и синтетических коллоидных препаратов, последовательность введения и соотношение которых зависит от величины предполагаемой кровопотери. Традиционно применявшиеся в практике отечественной службы скорой медицинской помощи (СМП) декстраны, в настоящее время, уступают свои позиции гидроксиэтилкрахмалам (ГЭК) (рис. 1), что обусловлено большей клинической безопасностью последних при сходной эффективности по возмещению внутрисосудистого дефицита и стабилизации гемодинамики [7]. Многочисленные публикации отмечают значительно более низкую частоту развития аллергических реакций и меньшее влияние на свертывающую функцию крови при использовании ГЭК по сравнению с декстранами [2, 19, 21].
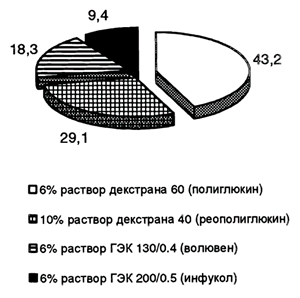 |
| Рисунок 1. Доля (в %) различных инфузионных коллоидных растворов, примененных на станции скорой и неотложной медицинской помощи г. Москвы в 2005 г. |
Однако и внутри класса ГЭК существует немалое количество препаратов, неравнозначных между собой по фармакологическому действию и клиническому эффекту [8]. Поэтому актуальным остается поиск «максимально универсального» коллоидного препарата для ДГЭ, наиболее оптимизированного по критерию «эффект / безопасность».
Согласно исследованиям, наименьшее модифицирующее действие на систему гемостаза оказывают ГЭК третьего поколения (6% Волювен, производство Фрезениус Каби, Германия) с уменьшенными средним молекулярным весом (до 130000 дальтон) и степенью замещения (до 0.4) [1,15].
Цель исследования - оценка эффективности и безопасности 6% ГЭК 130/0,4 Волювена в комплексе интенсивной терапии критических состояний на догоспитальном этапе.
Материал и методы
В исследование было включено 42 больных (37 мужчин и 5 женщин) в возрасте от 21 до 62 лет.
У 38 из них были диагностированы тяжелые травматические поражения, сопровождающиеся шоком различной степени тяжести (табл. 1), причем у 24 больных имелась сочетанная черепно-мозговая травма (63%), а у 12 - травма живота с признаками внутрибрюшного кровотечения (32%).
Таблица 1.
Распределение больных с травматическими повреждениями по степени тяжести шока
| Степень тяжести травматического шока | Число больных |
| I | 12 (32%) |
| II | 20 (53%) |
| III | 6 (15%) |
| Всего | 38 |
В исследование не были включены пострадавшие с травмой грудной клетки, требовавшие перевода на искусственную или вспомогательную вентиляцию легких.
У 4 больных были выявлены желудочно-кишечные кровотечения нетравматического генеза, осложненные геморрагическим шоком I-II степени тяжести.
Всем больным на ДГЭ проводился комплекс интенсивной терапии, предусмотренный Стандартами оказания скорой и неотложной медицинской помощи в г. Москве.
Для анализа эффективности Волювена у всех больных неинвазивно измерялись параметры гемодинамики - артериальное давление (АД) и частота пульса (ЧП), сатурация крови (SO2), по данным пульсоксиметрии, и частота дыхания (ЧД). У больных с сопутствующей черепно-мозговой травмой дополнительно определялся уровень сознания по шкале ком Глазго.
Для анализа безопасности применения Волювена у 22 больных (16 из них с признаками внутрибрюшного или желудочно-кишечного кровотечения) исследовались показатели системы гемостаза, доступные на ДГЭ [3]. У этих больных нестероидные противовоспалительные препараты с целью анальгезии не применялись.
Тромбоцитарно-сосудистый гемостаз определялся путем измерения времени кровотечения по модифицированному методу Дьюка.
Коагуляционный гемостаз определялся путем измерения времени свертывания крови по упрощенному методу Ли-Уайта.
Также в статус безопасности препарата входил контроль за возникновением побочных эффектов, связанных с его применением - развитие аллергических реакций, тошноты, рвоты и др.
Исследование вышеназванных показателей эффективности и безопасности препарата Волювен проводилось на следующих этапах:
- Исходно при первичном осмотре;
- Перед началом введения Волювена (если сначала вводился 0,9% раствор Натрия хлорида);
- После инфузии одной дозы (250 мл) Волювена;
- При поступлении больного в стационар.
Также фиксировался объем перелитых на ДГЭ инфузионных растворов и рассчитывалась средняя скорость их введения.
Все исследуемые параметры заносились в специально разработанный протокол для последующего статистического анализа.
Результаты исследования
Динамика исследуемых показателей у больных и пострадавших с шоком I степени тяжести представлена в табл.2. Объем инфузии в этой группе составил 820±50 мл (0,9% раствор Натрия хлорида 590±40 мл, Волювен 250±20 мл), причем инфузионная терапия начиналась с введения кристаллоидных препаратов и проводилась со средней скоростью 35±8 мл/мин. Все пациенты этой группы были доставлены в стационар со стабильными показателями гемодинамики (АДсист 106±8 мм рт.ст.) и положительной динамикой параметров периферического кровотока (SO2 увеличилась на 7±2% по сравнению с 1 этапом исследования).
Таблица 2.
Динамика показателей гемодинамики и дыхания у больных и пострадавших
с шоком I степени тяжести (n =12), M ± m
| Показатель | Этапы исследования | |||
| 1 | 2 | 3 | 4 | |
| АДсист (мм рт.ст.) | 90±9 | 91±10 | 102±3 *, ** | 106±8** |
| АДдиаст (мм рт.ст.) | 62±5 | 62±8 | 70±6 *, ** | 71±5** |
| ЧП (уд/мин) | 90±4 | 84±6* | 82±6 ** | 79±7 ** |
| ЧД (дых/мин) | 19±3 | 19±2 | 18±2 | 18±2 |
| SO2 (%) | 90±3 | 94±3* | 97±2 *, ** | 97±2 ** |
* - р < 0,05 по сравнению с предыдущим этапом исследования,
** - р < 0,05 по сравнению с 1 этапом исследования
Изменения гемодинамических параметров и других исследуемых показателей у больных и пострадавших с шоком II степени тяжести представлены в табл. 3. Объем инфузии в этой группе составил 1330±120 мл (0,9% раствор Натрия хлорида 910±40 мл, Волювен 490±10 мл). Инфузионная терапия, как и в предыдущей группе, начиналась с введения кристаллоидных препаратов и проводилась со средней скоростью 75±14 мл/мин.
Все пациенты этой группы были доставлены в стационар с положительной динамикой параметров центральной и периферической гемодинамики (увеличение АДсист и SO2 по сравнению с 1 этапом исследования, соответственно, на 39±9% и 9±2%).
Таблица 3.
Динамика показателей гемодинамики и дыхания у больных
и пострадавших с шоком II степени тяжести (n = 20), M ± m
| Показатель | Этапы исследования | |||
| 1 | 2 | 3 | 4 | |
| АДсист (мм рт.ст.) | 70±12 | 78±7 * | 84±5 *,** | 98±9 *,** |
| АДдиаст (мм рт.ст.) | 51±7 | 53±7 | 56±6 ** | 61±7 ** |
| ЧП (уд/мин) | 111±8 | 94±6 * | 90±5 ** | 85±8 ** |
| ЧД (дых/мин) | 22±6 | 18±2 * | 18±2 ** | 18±3 ** |
| SO2 (%) | 89±5 | 92±2 * | 96±2 *,** | 97±2 ** |
* р<0,05 по сравнению с предыдущим этапом исследования,
** р<0,05 по сравнению с 1 этапом исследования
Таблица 4.
Динамика показателей гемодинамики и дыхания у больных и пострадавших
с шоком III степени тяжести (n =6), M ±m
| Показатель | Этапы исследования | ||
| 1 | 2-3 | 4 | |
| АДсист (мм рт.ст.) | 50±9 | 54±7 | 74±7 *,** |
| АДдиаст (мм рт.ст.) | 48±4 *,** | ||
| ЧП (уд/мин) | 124±12 | 120±7 | 107±7 *,** |
| ЧД (дых/мин) | 22±10 | 20±6 | 20±3 |
| SO 2 (%) | 70±7 | 70±6 | 86±6 *,** |
* р<0,05 по сравнению с предыдущим этапом исследования,
** р<0,05 по сравнению с 1 этапом исследования
Таблица 5.
Динамика показателей системы гемостаза у больных и пострадавших
с шоком I - III степени тяжести (n =22), M ± m
| Показатель | Норма | Этапы исследования | ||
| 1 | 2-3 | 4 | ||
| Время кровотечения (мин) | 2-5 | 4,0±1,5 | 4,5±2,0 | 4,5±2,0 |
| Время свертывания крови (мин) | 5-10 | 9,5±0,5 | 9,5±1,5 | 10,0±2,0 |
* р<0,05 по сравнению с предыдущим этапом исследования,
** р<0,05 по сравнению с 1 этапом исследования
Таблица 6.
Динамика показателей неврологического статуса
у пострадавших с сочетанной тяжелой черепно-мозговой травмой (n =24), M ± m
| Показатель | Этапы исследования | |||
| 1 | 2 | 3 | 4 | |
| Баллы по шкале ком Глазго | 7±3 | 7±3 | 8±4 | 9±2 |
* р<0,05 по сравнению с предыдущим этапом исследования,
** р<0,05 по сравнению с 1 этапом исследования
Данные, полученные на этапах исследования у пострадавших с шоком III степени тяжести, отражены в табл. 4. Инфузионная терапия в этой группе начиналась с введения коллоидных препаратов и проводилась со средней скоростью 136±22 мл/мин. У 4 пострадавших с массивной кровопотерей и критической артериальной гипотензией, рефрактерной к струйному введению 2 доз Волювена (500 мл), в схему инфузионной терапии были включены коллоидные растворы с исходным гиперволемическим эффектом (10% ГЭК 200/0,5 - Хаес-стерил или 6% декстран-60-полиглюкин). Общий объем инфузии в этой группе составил 2400±300 мл, причем инфузия проводилась через 2 периферических венозных катетера. Вазопрессоры в комплексе противошоковой терапии не применялись. Все пациенты этой группы также были доставлены в стационар с положительной динамикой параметров центральной гемодинамики (увеличение АДсист на 47±9% по сравнению с 1 этапом исследования).
Данные, отражающие догоспитальное влияние Волювена на систему гемостаза, в том числе у пострадавших с признаками внутрибрюшного кровотечения и больных с желудочно-кишечными кровотечениями, представлены в табл. 5.
Динамика показателей неврологического статуса у пострадавших с сопутствующей тяжелой черепно-мозговой травмой различной степени тяжести отражена в табл. 6.
Обсуждение полученных результатов
При планировании схемы инфузионной терапии травматического шока на ДГЭ необходимо учитывать фазность данного патологического процесса [4]. В фазе компенсированного шока одним из механизмов заполнения внутрисосудистого сектора и поддержания системной гемодинамики является интравазальное поступление жидкости из интерстициального пространства с неизбежным развитием интерстициальной, а значит, и клеточной дегидратации. Начало инфузионной терапии в этот период с введения растворов с исходным гиперволемическим эффектом чревато прогрессированием внесосудистой дегидратации и развитием отсроченных осложнений шока в виде полиорганной недостаточности [8]. Поэтому в этой фазе шока патогенетически более обосновано начальное введение кристаллоидных препаратов с последующей стабилизацией внутрисосудистого объема инфузией изоволемических коллоидных растворов, каким и является Волювен. В нашем исследовании подобная схема инфузионной терапии позволила эффективно восстановить и поддерживать параметры центральной гемодинамики у больных и пострадавших с шоком I-II степени тяжести на ДГЭ. Отмечено также положительное влияние инфузии на периферический кровоток, проявляющееся характерными клиническими признаками и улучшением показателей пульсоксиметрии. Это может быть обусловлено как нормализацией системной гемодинамики, так и оптимизацией реологии крови при использовании препаратов ГЭК третьего поколения с уменьшенным молекулярным весом (130000 Дальтон).
При декомпенсации шока, наоборот, тканевой метаболический ацидоз способствует увеличению проницаемости сосудистой стенки и усиленному оттоку жидкости из сосудистого русла в интерстициальное пространство. Поэтому в этот период целесообразно начинать инфузионную терапию с введения растворов с исходным гиперволемическим эффектом, которые дополнительно привлекают внутрь сосудов жидкость из интерстициального пространства и быстрее корригируют критическую депрессию гемодинамики [5,8]. Подобная тактика допустима и в случаях массивных кровотечений.
Наше исследование продемонстрировало недостаточную эффективность изоволемических коллоидных растворов для быстрой стабилизации системной гемодинамики у пострадавших с травматическим шоком III степени тяжести на ДГЭ, что можно объяснить и ограничением по времени догоспитальной противошоковой терапии. В качестве эспандерных инфузионных сред применимы 10% растворы ГЭК, декстраны (хотя они имеют значимое количество побочных эффектов, описанных выше) и гипертонические растворы, например, ГиперХАЕС (производство Фрезениус Каби, Германия), состоящий из 7,2% раствора Натрия хлорида и 6% ГЭК 200/0.5. Последующая инфузия на ДГЭ должна проводиться изоволемическими коллоидными растворами и кристаллоидными препаратами [22].
Немаловажным фактором адекватной противошоковой терапии является соблюдение принципа преемственности между этапами оказания медицинской помощи. С одной стороны, структурные особенности отечественного стационарного этапа предполагают целесообразность создания догоспитальной терапией некоторого запаса времени на первичные сортировочные и диагностические мероприятия. С другой стороны, препараты, вводимые на ДГЭ, не должны дополнительно ухудшать функции органов и систем, и так находящихся в шоковом режиме гипоперфузии. Формат нашего исследования не предполагал детальное изучение данного аспекта безопасности ГЭК 130/0.4.
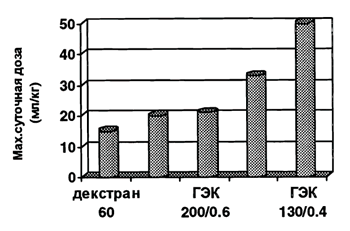 |
| Рисунок 2. Максимальная суточная доза (мл/кг) различных 6% растворов декстрана и ГЭК |
Однако, по данным литературы, Волювен оказывает минимальное отрицательное влияние на функцию почек, легких и печени [12,16,17], что обусловлено уменьшением молекулярного веса до 130 kDa и степени замещения до 0,4, а также сырьем, из которого препарат производится (кукурузный крахмал). Безопасность Волювена подтверждается тем, что его разрешенная максимальная суточная доза значительно превышает таковую для других синтетических коллоидов (рис. 2). В то же время изменение характера замещения гидроксиэтиловых групп в положении С2:С6 на 9:1 вместо 5:1 обеспечило препарату более стабильный (длительный) волемический эффект при схожем размере молекул и одинаковой степени замещения [13]. Поэтому по длительности волемического действия и по гемодинамической эффективности 6% ГЭК 130/0.4 (Волювен) идентичен 6% ГЭК 200/0,5 [11, 18], его объемный коэффициент составляет 100%, а плато эффект - 4 часа [23].
При выборе инфузионного препарата для терапии травматического шока на ДГЭ важным является влияние его на систему гемостаза. При сочетанной травме почти в 40% случаев встречается и повреждение органов брюшной полости с возможным внутренним кровотечением [6]. Данная патология не всегда легко диагностируется на ДГЭ и рутинное использование растворов, провоцирующих кровоточивость, может иметь фатальные последствия для пациентов. По данным литературы, растворы ГЭК безопаснее декстранов в плане воздействия на систему гемостаза [2], а Волювен является единственным из 6% растворов ГЭК, не влияющим на функцию тромбоцитов [14], и рассматривается, как препарат выбора в ситуациях, когда влияние инфузионной терапии на систему гемостаза должно быть строго ограниченно [2]. Из всех механизмов воздействия на гемостаз для ГЭК 130/0,4 отмечено только влияние на гемодилюцию [9,10]. Наше исследование на ДГЭ полностью подтвердило эти положения, не выявив значимого влияния Волювена ни на тромбоцитарно-сосудистый, ни на коагуляционный гемостаз. Хочется также отметить, что при инфузии препарата во время выполнения хирургической операции (5 собственных наблюдений, формально не входящих в данное исследование) визуально не было отмечено увеличение кровоточивости операционного поля.
В нашем исследовании не была выявлена отрицательная динамика неврологического статуса у пострадавших с тяжелой сочетанной черепно-мозговой травмой и шоком на фоне инфузии Волювена на ДГЭ. По данным литературы, даже длительное его введение в больших дозах (до 70 мл/кг/сут в течение 28 дней) больным с тяжелой черепно-мозговой травмой было безопасно [20]. Мы наблюдали даже некоторый положительный догоспитальный эффект, объяснимый, по нашему мнению, комплексным лечением, включавшим респираторную поддержку, инфузионную стабилизацию системной, а значит, и церебральной гемодинамики, нейропротекторную терапию.
Также необходимо отметить, что при инфузии Волювена мы не отметили возникновения тошноты, рвоты и случаев анафилаксии. Эти наблюдения соответствуют литературным данным, относящим растворы ГЭК к наиболее безопасным среди синтетических коллоидов в плане развития аллергических реакций [19,21].
Выводы
- 6% ГЭК 130/0.4 (Волювен) является эффективным и безопасным инфузионным раствором, применимым на ДГЭ при травматическом шоке I-II степени тяжести в качестве базового препарата в комплексе с кристаллоидными растворами.
- При травматическом шоке III степени тяжести на ДГЭ Волювен применим в качестве поддерживающего препарата вместе с кристаллоидными растворами после первичного введения инфузионных сред с исходным гиперволемическим эффектом.
- Профиль безопасности препарата Волювен позволяет считать его препаратом выбора при желудочно-кишечных кровотечениях или при травме, сопровождающейся внутренним кровотечением.
Литература
- Буланов А.Ю. и др. Волювен - препарат нового поколения в терапии критических состояний. //Вестник службы крови. 2002, N4, с.4-9.
- Буланов А.Ю. и др. Влияние различных типов коллоидных объемозамещающих растворов на измененную систему гемостаза. //Анестезиология и реаниматология. 2004, N2, с.25-30.
- Лабораторные методы исследования в клинике. Справочник под ред. Меньшикова В.В. М., 1987.
- Леонова Н.М. и др. Травматический шок. Учебно-методическое пособие. М., 2004.
- Марусанов В.Е. и др. Тактика инфузионной поддержки плазмозамещающими растворами при травматическом шоке на догоспитальном этапе. //Современные направления и пути развития анестезиологии-реаниматологии в Российской Федерации. М., 2006, с.248-9.
- Цыбуляк Г. И. Лечение тяжелых и сочетанных повреждений. СПб, 1995.
- Ярмагомедов А.А. Перспективы применения препаратов гидроксиэтилкрахмалов на догоспитальном этапе. //Скорая медицинская помощь. 2005, N3,c.47-50.
- Ярмагомедов А.А. и др. Выбор растворов гидроксиэтилкрахмалов на догоспитальном этапе. //Скорая медицинская помощь. 2006, N 4, с.32-38.
- Asskali F et al. Thrombelastographic coagulation analysis following in vitro and in vivo haemodilution with hydroxyethyl starch (HES). //Anasthesiol Intensivmed Not-fallmed Schmerzther. 2002; 37:258-66.
- Baron JF. //Kidney Blood Press Res. 2001; 24: 213-44.
- Boldt J et al. Volume therapy with a new hy-droxyethyl starch solution in cardiac surgical patients before cardiopulmonary bypass //J Cardiothor and Vascul Anesth. 2000; 14(3): 264-8.
- Dehne MG et al. Hydroxyethyl starch (HES) does not directly affect renal function in patients with no prior renal impairment. //J Clin Anesth. 2001; 13(2): 103-11.
- Entholzner EK et al. Coagulation effects of a recently developed hydroxyethyl starch (HES 130/0.4) compared to hydroxyethyl starches with higher molecular weight. //Acta Anaesth Scand. 2000; 44(9): 1116-21.
- Franz A et al. The effects of hydroxyethyl starches of varying molecular weights on platelet function. //Anesth Analg.2001;92: 1402-7
- Gallandat Huet RC et al. A novel hydroxyethyl starch (Voluven) for effective perioperative plasma volume substitution in cardiac surgeryJ/Can J Anaesth. 2000; 47(12): 1207-15.
- Jamnicki M et al. The effect of potato starch derived and corn starch derived hydroxyethyl starch on in vitro blood coagulation. //Anaesthesia. 1998; 53(7): 638-44.
- Jungheinrich С et al. The pharmacokinetics and tolerability of an intravenous infusion of the new hydroxyethyl starch 130/0.4 (6%, 500 mL) in mild-to-severe renal impairment. //Anesth Analg. 2002; 95(3): 544-51.
- Kasper SM et al. Evaluation of a new hydroxyethyl starch solution (HES 130/0.4) in patients undergoing pre-operath/e autologous blood donation. //J Clin Anesth. 2001; 13: 486-90.
- Laxenaire VC et al. Anaphylactoid reactions to colloid plasma substitutes: incidence, risk factors, mechanisms. A French multicenter prospective study //Ann Fr Anesth Reanim. 1994. 13:301-10.
- Neff ТА et al. // Вестник службы крови России. 2003. 4, 41-8.
- Ring J et al. Incidence and severity of anaphylactoid reactions to colloid volume substitutes. //Lancet. 1977; 1: 466-9.
- Soreide E et al. Pre-hospital fluid therapy in the critically injured patient-a clinical update. //Injury. 2005; 36(9):1001-10.
- Wahzinger J et al. //Clin Drug Invest 1998; 16: 151-60.

