Постуральные реакции мозгового кровотока у беременных с тяжелой преэклампсией
А. А. Ившин, Е. М. Шифман, Е. Г. Гуменюк
Кафедра акушерства и гинекологии медицинского факультета
Петрозаводского государственного университета;
МУЗ «Родильный дом им. Гуткина К.А;
ГУЗ «Республиканский перинатальный центр МЗСР РК»,
Петрозаводск, Карелия, Россия
Преэклампсию отличает крайняя вариабельность форм клинических проявлений [2, 4]. Даже известная классическая триада симптомов не является достоверным прогностическим критерием [6]. Таким образом, продолжает оставаться актуальным поиск неинвазивных методов диагностики, обладающих достаточной воспроизводимостью, для их выполнения в условиях скрининговых исследований, и позволяющих установить критерии тяжести преэклампсии [1, 5]. Определенное диагностическое значение для доклинической диагностики преэклампсии имеет постуральный тест: повышение диастолического АД более чем на 20 мм рт.ст. при повороте женщины с левого бока на спину указывает на риск развития преэклампсии («roll-over test» или «тест с поворотом») [3, 6].
В предыдущих работах, основанных на результатах транскраниальной допплерографии (ТДГ), нами показано, что у беременных с преэклампсией изменяется мозговой кровоток, и нарушения носят характер ишемически-реперфузионного повреждения вследствие несостоятельности системы цереброваскулярной ауторегуляции [7, 8].
Цель настоящего исследования: сравнить ауторегуляторные сосудистые реакции мозгового кровотока во время постурального теста с поворотом у здоровых беременных и беременных с тяжелой преэклампсией.
Материал и методы исследования. Исследование проводилось на базе Республиканского перинатального центра МЗСР РК. Под наблюдением находились 73 женщины в возрасте от 17 до 35 лет (средний возраст 25,5±4,3 года) с диагнозом тяжелой преэклампсии. Группу сравнения составили 90 условно здоровых беременных женщин в возрасте от 19 до 34 лет (средний возраст 25,9±4,2 года) в III триместре беременности, состоявших на диспансерном учете в консультативном отделении Республиканского Перинатального центра МЗСР РК. Алгоритм распределения в исследуемых группах представлен на рисунке 1. Средний гестационный возраст в обеих группах 34±3 недели. В клинически тяжелых случаях детальное обследование осуществлялось после начала терапии.
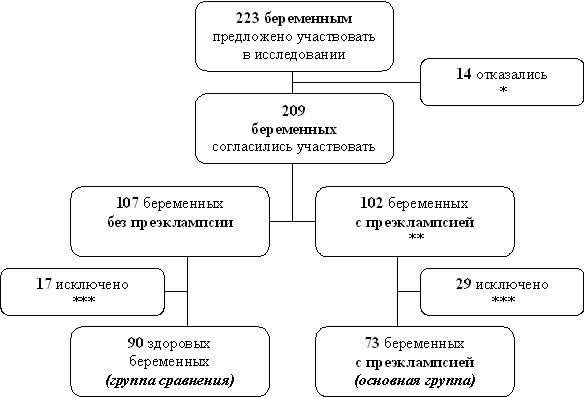 |
Рис. 1. Распределение пациенток в исследуемых группах * протокол информированного согласия пациентки на обследование; ** критерием включения в группу был диагноз преэклампсии верифицированный на основании международной статистической классификации болезней и проблем, связанных со здоровьем, 10-го пересмотра. Степень тяжести преэклампсии оценивалась по шкале Goecke в модификации Г. М. Савельевой; *** из наблюдения были исключены пациентки, имеющие пороки сердца, нарушения сердечного ритма, ишемическую болезнь сердца, хроническую артериальную гипертензию, кардиомиопатию, грубые нарушения гемореологических показателей, сахарный диабет, нейроинфекции, черепно-мозговые травмы и эпизоды синкопальных состояний в анамнезе. |
Методика проведения постурального теста: пациентка спокойно лежит не левом боку в течение 5 минут. Доступным способом измеряется артериальное давление на правом плече, результат измерения фиксируется. Манжету манометра оставляют на правой руке. Пациентка переворачивается на спину, и артериальное давление немедленно измеряют снова. Если диастолическое артериальное давление при повторном измерении увеличено более чем на 20 мм рт.ст. по сравнению с исходным, это указывает на высокий риск развития преэклампсии.
Артериальное давление измерено автоматическим сфигмоманометром монитора «Cardiocap II» фирмы «DATEX» с обычной манжетой на правой руке. Церебральная гемодинамика изучена с помощью метода транскраниальной допплерографии. Исследование выполнялось на ультразвуковом сканере Aloka SSD-4000. С целью исключения патологии, оказывающей потенциальное воздействие на фоновые показатели церебрального кровотока, проведено цветовое дуплексное сканирование брахиоцефальных артерий и артерий вертебробазилярного бассейна.
При ТДГ транстемпоральным доступом с обеих сторон измерены количественные параметры кровотока в M1 сегменте средней мозговой артерии: пиковая систолическая скорость кровотока (PSV), конечная диастолическая скорость (EDV), усредненная по времени средняя скорость (TAV), индекс стабильности потока (SFI), систолодиастолическое отношение (S/D), пульсационный индекс (PI) и индекс резистентности (RI). Перечисленные величины подсчитаны автоматически встроенной программой ультразвукового сканера.
Поскольку указанные выше линейные характеристики допплеровского спектра не позволили составить объективное представление об объеме перфузии мозга, был подсчитан ряд показателей, анализ которых помог уточнить состояние церебральной гемодинамики: индекс мозгового кровотока (ИМК), церебральное перфузионное давление (ЦПД), внутричерепное давление (ВЧД), индекс гидродинамического сопротивления (ИГС), коэффициент овершута (КО).
Достоверность различий средних значений установлена методом сравнения средних значений двух выборочных совокупностей с определением t-критерия Стьюдента и уровня значимости (p). Статистическая значимость результата (p) представляет собой оцененную меру уверенности в его "истинности", "репрезентативности выборки". Указанный показатель находится в убывающей зависимости от надежности результата. Более высокий p-уровень соответствует более низкому уровню доверия к найденной в выборке зависимости между переменными. Именно, p-уровень представляет собой вероятность ошибки, связанной с распространением наблюдаемого результата на всю популяцию. В медицинских исследованиях p-уровень 0,05 рассматривается как "приемлемая граница" уровня ошибки. Выборка однородная, распределение нормальное, подтверждено тестом Колмогорова – Смирнова. Равенство дисперсий в группах проверено при помощи критерия Левена. Для определения меры зависимости между переменными применена простая линейная корреляция Пирсона (r). Необходимые вычисления реализованы в прикладном пакете программ «STATISTICA 7.0»
Результаты исследования. Во время выполнения постурального теста нами определены показатели мозгового кровотока у пациенток с нормально протекающей беременностью и беременных с тяжелой преэклампсией, и установлена достоверность различий средних значений в исследуемых группах. При анализе данных, полученных при ТДГ средней мозговой артерии, выявлено, что у беременных основной группы наблюдается достоверное, симметричное с обеих сторон, снижение линейных показателей допплеровского спектра (табл. 1). У беременных с тяжелой преэклампсией во время постурального теста нами отмечено снижение линейной скорости кровотока, преимущественно, за счет пиковой систолической скорости (72,85 см/с против 73,76 см/с; p <0,05). Выявлено статистически достоверное изменение уровня цереброваскулярного сопротивления на основании снижения пульсационного индекса (0,71 против 0,73; p <0,01). Систолодиастолическое отношение, отражающее состояние сосудистой стенки, снизилось после выполнения постурального теста у беременных с тяжелой преэклампсией (1,94 против 1,91; p <0,01). Отмечено достоверное статистическое различие в ряде величин, отражающих внутричерепное давление, гидродинамическое сопротивление и цереброваскулярную реактивность. Постуральный тест в основной группе обследуемых женщин привел к повышению индекса гидродинамического сопротивления ( 2,45 мм рт. ст./см • с –1 против 2,34 мм рт ст./см • с –1 ; p <0,01). Внутричерепное давление также увеличилось ( 16,20 мм рт. ст. против 13,19 мм рт. ст.; p <0,005). Напротив, индекс мозгового кровотока (19,80 против 22,15; p <0,01) и индекс стабильности потока (0,59 против 0,60; p <0,05) оказались статистически достоверно ниже после завершения постурального теста. Статистических различий в группе сравнения не выявлено.
| Преэклампсия тяжелая (1) n=73 | Группа сравнения (2) n=90 | (p)* | (p) | |||
| До теста (1.1) | После теста (1.2) | До теста (2.1) | После теста (2.2) | 1.1-1.2 | 2.1-2.2 | |
| PSV, см/с | 73,76±1,11 | 72,85±1,15 | 103,79 ± 1,59 | 104,83 ± 1,75 | <0,001 | > 0,05 |
| EDV, см/с | 35,29 ± 0,39 | 34,69±0,43 | 48,28 ± 1,12 | 48,73 ± 1,09 | <0,001 | > 0,05 |
| TAV, см/с | 49,92 ± 0,40 | 48,50±0,42 | 67,81 ± 1,41 | 67,46 ± 1,38 | <0,001 | > 0,05 |
| S/D | 1,91 ± 0,02 | 1,94±0,02 | 2,06 ± 0,02 | 2,05 ± 0,02 | <0,01 | > 0,05 |
| PI | 0,73 ± 0,02 | 0,71±0,02 | 0,85 ± 0,02 | 0,84 ± 0,02 | <0,01 | > 0,05 |
| RI | 0,51 ± 0,01 | 0,49±0,01 | 0,53 ± 0,01 | 0,54 ± 0,01 | > 0,05 | > 0,05 |
| ЦПД, мм рт. ст. | 47,25 ± 1,21 | 48,30±1,22 | 50,52 ± 0,97 | 49,57 ± 0,99 | > 0,05 | > 0,05 |
| ВЧД, мм рт. ст. | 13,19 ± 1,68 | 16,20±1,45 | 10,54 ± 0,86 | 10,69 ± 0,74 | <0,005 | > 0,05 |
| ИГС, мм рт. ст./см • с –1 | 2,34 ± 0,02 | 2,45±0,02 | 1,26 ± 0,02 | 1,29 ± 0,03 | <0,001 | > 0,05 |
| ИМК, см/с | 22,15 ± 0,57 | 19,80±0,53 | 40,87 ± 1,11 | 40,20 ± 1,13 | <0,01 | > 0,05 |
| SFI | 0,60 ± 0,01 | 0,59±0,01 | 0,69 ± 0,02 | 0,69 ± 0,01 | <0,05 | > 0,05 |
| КО | 1,38 ± 0,02 | 1,31±0,03 | 1,04 ± 0,02 | 1,06 ± 0,04 | > 0,05 | > 0,05 |
| Примечание: * p – статистическая значимость (p-уровень). |
Согласно цели настоящего исследования, следующим этапом проведен корреляционный анализ между параметрами мозгового кровотока и показателями артериального давления. Обнаружена средняя обратная зависимость между показателями мозгового кровотока и средним артериальным давлением (PSV и САД: r =-0,41; EDV и САД: r =-0,43; TAV и САД: r =-0,44), что, вероятно, объясняется наличием собственной системы ауторегуляции кровообращения в головном мозге, блокирующей колебания артериального давления в определенных рамках регуляции.
Обсуждение результатов исследования
Наблюдаемые изменения церебральной гемодинамики, выявленные в ходе исследования в группе пациенток с преэклампсией весьма характерны для сосудистых сегментов, находящихся в состоянии вазодилатации. Нарушение перфузии мозга следует считать симметричным, поскольку не было выявлено достоверных различий между аналогичными величинами, измеренными с обеих сторон. Постуральный тест с поворотом вызывает изменения системного кровотока. Поворот с левого бока на спину приводит к увеличению артериального давления, как у здоровых беременных, так и у беременных с преэклампсией, однако в последней группе степень повышения давления сравнительно выше. Подобное изменение гемодинамики во время постурального теста у беременных основной группы привело к ауторегуляторной вазодилятации престенотических сегментов артерий и вазоконстрикции сосудов сопротивления (артериол) для поддержания постоянства мозгового кровотока. Вероятно, изменение тока крови указывает на пассивное расширение в области M1 сегмента средней мозговой артерии, что может отмечаться в случае комбинации повышенного артериального давления и сбоя в системе ауторегуляции. Становится очевидным, что мозговая ауторегуляция у беременных, страдающих преэклампсией, оказывается несостоятельной, поскольку не соблюдается закономерность реакции мозговой гемодинамики, состоящая в повышении скорости кровотока по магистральным артериям мозга в ответ на увеличение среднего артериального давления. Повышение показателя коэффициента овершута подтверждает предположение о предельно напряженном резерве вазодилатации. Полученные результаты следует интерпретировать как сбой компенсаторного механизма регуляции тонуса интракраниальных сосудов у беременных с тяжелой преэклампсией.
По-видимому, нарушения мозгового кровотока при постуральном тесте связаны с аорто-кавальной компрессией. Нам представляется, что в указанный процесс включаются и механизмы ауторегуляции мозгового кровообращения, вызывая дилатацию мозговых артерий для поддержания адекватной перфузии мозга на фоне низкого сердечного выброса. Но вместе с тем, предельно напряженный резерв вазодилатации, свидетельствующий о сбое системы ауторегуляции мозгового кровообращения у беременных с преэклампсией не способен компенсировать указанные нарушения, что приводит к расстройствам мозгового кровообращения.
По нашему мнению, при прогрессировании преэклампсии, указанные процессы ведут к увеличению внутричерепного давления, развитию вазогенного отека и формированию гипертонической энцефалопатии, что прямо и косвенно подтверждается итогами настоящего наблюдения. Между тем пассивному расширению артериол сопутствует снижение церебрального перфузионного давления. На фоне очерченных патологических процессов формируется феномен Кохера-Кушинга, направленный на восстановление церебрального перфузионного давления, за которым, предположительно, должно последовать дальнейшее прогрессивное повышение среднего артериального давления, усугубление артериальной гипертензии и формирование порочного круга. В том случае, когда внутричерепная гипертензия превышает компенсаторные возможности системы кровообращения, уровень мозгового кровотока и объем кровенаполнения головного мозга резко снижаются, развивается гипоксия и ишемия головного мозга, ауторегуляция нарушается или полностью утрачивается.
Таким образом, у пациенток с преэклампсией для достижения компенсации мозгового кровотока необходимо более сильное напряжение ауторегуляторных реакций периферического кровообращения. По-видимому, это может служить одним из объяснений биологической целесообразности периферической вазоконстрикции у беременных с тяжелой формой преэклампсии, так как существующие объяснения роста общего периферического сопротивления сосудов в зависимости только от волемического статуса выглядят механистически.
Выводы:
- Данные проведенного исследования свидетельствуют о нарушении перфузии мозга у беременных с тяжелой преэклампсией во время постурального теста в отличие от пациенток группы сравнения.
- Полученные результаты следует интерпретировать как сбой компенсаторного механизма регуляции тонуса интракраниальных сосудов у беременных с тяжелой преэклампсией.
- Выявленные статистически достоверные различия показателей мозгового кровотока у беременных с тяжелой преэклампсией и пациенток группы сравнения при проведении roll - over теста подчеркивают его исключительную ценность для диагностики преэклампсии.
Список литературы
- Венцковский Б. М. Гестозы. – М.: МИА. – 2005. – 312 с.
- Гестоз // Клинические рекомендации. Акушерство и гинекология / Под ред. В. И. Кулакова. – М.: ГЭОТАР-Медиа, 2005. – С. 136-171.
- Репина М. А. Преэклампсия и материнская смертность. - СПб.: Изд-во СПбМАПО, 2005. - 208 с.
- Савельева Г. М., Кулаков В. И., Серов В. Н. и др. Профилактика и терапия гестоза // Российский вестник акушера-гинеколога. – 2001. – Т. 1, № 3. – С. 66-72.
- Серов В. Н., Шифман Е. М., Молчанов И. В. Эклампсия – диагностика, анестезия и интенсивная терапия // Мат. Всероссийской междисциплинарной конференции. – Стамбул. – 2002. – С. 71-84.
- Шифман Е. М. Преэклампсия, эклампсия, HELLP -синдром. – Петрозаводск: Изд-во «ИнтелТек», 2002. – 432 с.
- Шифман Е.М., Гуменюк Е.Г., Ившин А.А. Диагностика поражений головного мозга у беременных с преэклампсией и эклампсией // Акушерство и гинекология. – 2004. – №6. – С.6-8.
- Шифман Е.М., Гуменюк Е.Г., Ившин А.А. Диагностика нарушений церебральной ар– териальной гемодинамики у беременных с тяжелой преэклампсией // Российский вестник акушера-гинеколога. – 2005. – №1. – С.4-8.

