САМАРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
П.Ю.Столяренко
ИСТОРИЯ ОБЕЗБОЛИВАНИЯ В СТОМАТОЛОГИИ (ЧАСТЬ 4)
Самара 2001
Содержание этой части
Краткая история развития анестезиологии (период с начала XX века)
История применения эндотрахеального наркоза в челюстно-лицевой хирургии
Развитие обезболивания в стоматологии с 1946 года до конца XX века
Послеоперационное обезболивание
Краткая история развития анестезиологии (период с начала XX века)
Первой была разработана методика ингаляционного наркоза, затем появилась местная анестезия, позже других стал развиваться внутривенный наркоз. В этом разделе остановимся на основных вехах развития анестезиологии после открытия первых ингаляционных анестетиков.
Ингаляционная анестезия. Несмотря на внедрение в практику других ингаляционных анестетиков (этилхлорид, этилен, дивиниловый эфир, циклопропан, трихлорэтилен, флуроксен и др.), эфир оставался наиболее распространенным ингаляционным анестетиком до начала 1960 г. Циклопропан, синтезированный в 1934 году, был единственным ингаляционным анестетиком, конкурировавшим с эфиром по безопасности и популярности. К сожалению, оба эти анестетика легко воспламеняются и поэтому постепенно были вытеснены невоспламеняющимися сильнодействующими фторсодержащими углеводородами: галотаном, фторотаном (синтезирован в 1951 г., применение начато в 1956 г.); метоксифлураном (синтезирован в 1951 г., применение начато Artusio и соавт. в 1960 г.); энфлюраном (синтезирован в 1963 г., применение начато в 1973 г.); изофлюраном (синтезирован в 1965 г., применение начато в 1981 г.); десфлюраном (синтезирован 1966 г.) и др.
Неингаляционная анестезия. История развития неингаляционного наркоза начинается с 1847 г. Н.И. Пирогов в работе «Практические и физиологические наблюдения над действием паров эфира на животный организм» посвятил две главы неингаляционному наркозу: одну прямокишечному, другую внутривенному и внутриартериальному.
Внутривенный наркоз эфиром не получил распространения из-за многих осложнений. Однако попытки достигнуть наркоза внутривенным введением наркотических веществ неоднократно повторялись. В 1872 г. Пьер-Сиприен Орэ ( Pierre - Cyprien Ore) вводил животным в вену хлоралгидрат и получил состояние наркоза. Через два года этот метод он применил у человека при лечении столбняка. В 1909 г. Буркхард (Burkhardt) вводил слабые растворы эфира и хлороформа. Им проведено 250 операций под таким обезболиванием без особых осложнений. Таким образом, идея Н.И. Пирогова о возможности достижения наркоза путем введения наркотических веществ непосредственно в кровь получила в дальнейшем всеобщее признание.
Новая эра в развитии внутривенного наркоза наступила тогда, когда для наркоза были предложены жидкие наркотические вещества с высокой точкой кипения, которые вследствие этого не переходили в сосудах в парообразное состояние.
 |
Рис. 92. Николай Павлович Кравков (1865–1924), крупнейший отечественный фармаколог. Предложил для внутривенного наркоза гедонал |
Начало современному внутривенному наркозу положил крупнейший русский фармаколог Н.П. Кравков (рис. 92), доказавший принципиальную возможность и целесообразность применения неингаляционного наркоза в чистом виде и в комбинации его с ингаляционным. В 1902 г. он предложил пользоваться для внутривенного наркоза гедоналом. Опыты по применению гедоналового внутривенного наркоза были выполнены в 1902 г. на собаках П.П. Лампсаковым и 7 декабря 1909 г. впервые в клинике С.П. Федоровым. В зарубежной литературе гедоналовый наркоз называется русским методом внутривенного наркоза (Жоров И. С., 1959).
Барбитураты были синтезированы в 1903 г. Фишером (Fisсher) и фон Мерингом (von Mering). Первым барбитуратом, примененным для вводного наркоза, оказался барбитал, но только после появления в 1927 г. гексобарбитала индукция анестезии барбитуратами получила широкое распространение. В 1932 г. синтезированы тиопентал-натрий Вольвилером (Volwiler) и Таберном (Tabern) и гексенал Веезе (Weese). Впервые в клинике наркоз тиопенталом был применен Джоном Ланди (John Lundy) и Ральфом Уотерсом (Ralph Waters) в 1934 г. и до сих пор остается наиболее часто используемым препаратом для вводного наркоза. В нашей стране в изучение и внедрение в практику барбитурового наркоза большой вклад внес Исаак Соломонович Жоров (рис. 93).
 |
Рис. 93. Исаак Соломонович Жоров (1898–1976). Корифей советской анестезиологии. Автор руководства по общему обезболиванию в хирургии, по которому училось не одно поколение анестезиологов |
Метогекситал впервые был применен в клинике В.К. Стелтингом (Stoelting V.K.) в 1957 г. и является еще одним барбитуратом, по сей день используемым для вводного наркоза. После того как в 1957 г. был синтезирован хлордиазепоксид, бензодиазепины - диазепам (1959 г.), лоразепам (1971 г.) и мидазолам (1976 г.) - стали широко использоваться для премедикации, индукции и потенцирования анестезии, а также для внутривенной седации. Кетамин был синтезирован в 1962 г. Стивенсом (Stevens), впервые применен в клинике в 1965 г. Корссеном (Corssen) и Домино (Domino), разрешен к широкому использованию в 1970 г. Кетамин стал первым неингаляционным анестетиком, введение которого сопровождалось лишь минимальным подавлением кровообращения и дыхания. В 1964 г. был синтезирован этомидат и разрешен к применению в 1972 г.
В 1976 г. синтезирован пропофол, в 1989 г. был разрешен к применению. Появление этого препарата имело огромное значение для амбулаторной анестезиологии в связи с кратковременностью его действия.
Миорелаксанты. Первые сведения о кураре проникли в Европу более 400 лет назад после возвращения экспедиции Колумба из Америки, где южноамериканские индейцы использовали его для смазывания наконечников стрел при стрельбе из лука или бамбуковых трубок (рис. 94).
 |
| Рис. 94. Индейцы на охоте на птиц выдувают отравленные кураре стрелы из бамбуковых трубок |
Как гласит предание, смертоносный яд готовили старейшие женщины племени. На костре в большом котле варились корни ядовитых растений вместе со смолянистыми соками, змеиным ядом, головами муравьев, хвостами скорпионов и др. Яд признавали годным для применения только тогда, когда одна из варивших этот состав старух теряла сознание и погибала (рис. 95).
 |
| Рис. 95. Приготовление "стрельного яда", в состав которого включалось кураре |
Такого рода пагубное действие, по мнению ряда исследователей, вряд ли можно отнести за счет кураре. По всей вероятности, усиленное вдыхание угара от примешанных к кураре неизвестных веществ оказывалось смертельным. К таким примесям, возможно, относились растения, подобные сумах - ядовитому дереву (Григорьев М.С., Аничков М.Н., 1957).
В 1857 г. Джон Сноу (John Snow) наблюдал, как во время наркоза хлороформом дыхание «... иногда выполнялось только диафрагмой, в то время как межреберные мышцы были парализованы». (Цит. по Д. Ворнеру, 1998.)
К 1935 г. Кинг (King) выделил из кураре его основной естественный алкалоид - тубокурарин. Впервые мышечный релаксант тубокурарин (интокострин) был использован в клинике 23 января 1942 г. в Монреальском Гомеопатическом госпитале доктором Гарольдом Гриффитом (Harold Griffith)
(рис. 96) и его помощником Энидом Джонсоном (Enid Jonson) при операции аппендэктомия под циклопропановым наркозом 20-летнему водопроводчику. Это стало вехой в развитии анестезиологии. Использование мышечных релаксантов значительно облегчало интубацию трахеи и позволяло проводить наркоз на поверхностном и более безопасном уровне.
 |
Рис. 96. Гарольд Гриффит (1894-1985). Президент канадской ассоциации анестезиологов (с 1943). Ввел в анестезиологическую практику мышечные релаксанты (кураре) |
Сукцинилхолин (дитилин) был синтезирован Бове (Bovet) в 1949 г. и разрешен к применению в клинике с 1951 г. Он стал препаратом выбора для обеспечения интубации и поддержания наркоза в челюстно-лицевой хирургии.
В нашей стране современный эндотрахеальный наркоз начали применять с 1946 г. В 1948 г. вышла первая отечественная монография, посвященная этому методу, - «Интратрахеальный наркоз в грудной хирургии» (Григорьев М.С., Аничков М.Н.). Пионерами применения миорелаксантов на фоне эндотрахеального наркоза в нашей стране были М.С. Григорьев и М.Н. Аничков. Ими написана первая отечественная монография о миорелаксантах «Кураре и курареподобные препараты в хирургии», изданная в 1957 г.
В 1961 г. Американское общество анестезиологов (ASA) приняло классификацию объективного статуса больного, используемую при предоперационном обследовании.
Ларингеальная маска (ЛМ). В настоящее время во многих странах широкое распространение получил новый метод оптимизации проходимости дыхательных путей во время общей анестезии с помощью ларингеальной маски (рис. 97).
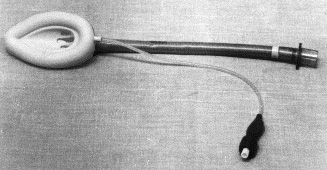 |
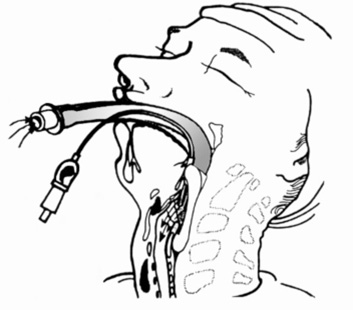
Рис. 97. Ларингеальная маска: А - основные элементы; 1 - коннектор; 2 - армированная трубка; 3 - эллипсовидная маска с раздувной манжетой; 4 - соединительная трубочка манжеты; 5 - контрольный баллончик; 6 - клапан; Б - у больного с синдромом Пьера Робена |
 |
Впервые тубус с блокирующей ротоглотку манжетой предложил в 1937 г. канадский анестезист Лич (Leech), но лишь в начале 80-х годов группа английских анестезиологов во главе с Арчибальдом Брайном (A. Brain) разработала современную концепцию применения ларингеальной маски (рис. 98).
 |
| Рис. 98. Арчибальд Брайн - создатель ларингеальной маски |
История создания и применения ларингеальной маски включает в себя три периода:
- Создание образцов-предшественников типа маски Гольдмана.
- Создание прототипов ЛМ (1981 - 1988 гг.):
- силиконовые;
- латексные;
- смешанные модели.
- Повсеместное распространение ЛМ (с 1988 г.).
Работая в 1981 г. в London Hospital Anaesthetics Unit доктор Брайн под руководством профессора Payne, изучая проблемы проходимости воздухоносных путей, сделал слепок ротоглотки трупа (рис. 99).
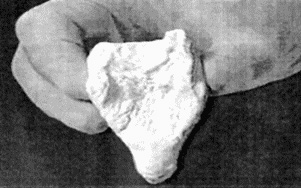 |
| Рис. 99. Слепок ротоглотки, полученнный А. Брайном |
На слепке было обнаружено пространство, находящееся вокруг и позади глотки, куда могли попадать инородные тела и давить на гортань. В этот период доктор Брайн работал в клинике хирургической стоматологии и для обеспечения проходимости дыхательных путей во время наркоза использовал воздуховод Мэйджила с присоединенной к нему стоматологической маской Гольдмана. Это была назальная маска одного размера с отсоединяющимся круговым надувным баллончиком. Баллончик, сформированный в форме эллипса, имел край для подсоединения ригидного компонента маски. Брайн обратил внимание на сходство величины и формы баллончика маски Гольдмана и полученного слепка ротоглотки. Это привело его к экспериментам в нерабочие часы и открытию, что если края баллончика свести вместе по средней линии, формируя длинную ось эллипса, то получится совершенно новая форма, похожая на надувную лодку с краями, формирующими дно. В то же время искривления, вызванные сведением краев маски Гольдмана, создавали большое сходство с фарингеальным слепком. При адаптации полученного образца и гортани трупа выявилось, что он очень хорошо сливается с грушевидной ямкой, в то время как лодкообразный нижний край баллончика плотно прилегает к треугольному контуру нижнего отдела глотки. Заключительным шагом этого рабочего этапа явилось подсоединение баллончика к трубке диаметром 10 мм и широкому краю маски с помощью акрилового клея. Баллончик опытного образца хорошо ложился в ротоглотке и его можно было легко сдувать и раздувать, как манжетку интубационной трубки. Этот образец легко стерилизовался в хлоргексидине и использовался у больных мужчин при операции грыжесечения в William Harvey Hospital, Ashfort, Kent в 1981 г.
В феврале 1983 г. ЛМ была впервые использована в случае неудачной интубации у больного массой тела 114 кг для проведения неотложной лапаротомии. Вентиляция проводилась в течение трех часов с пиком давления в воздухоносных путях 6 кРа. Осложнений не было. Это побудило Брайна провести в течение последующей недели 4 опыта на самом себе. ЛМ устанавливалась без медикаментозной подготовки и местной анестезии. Сохранялась хорошая проходимость дыхательных путей, болезненных ощущений не отмечалось. Так было установлено, что ЛМ может быть использована в трудных случаях и при правильной технике - атравматично.
В мае 1983 г. была проведена интубация трахеи «вслепую» через ЛМ, при этом трубка ЛМ составляла в диаметре 14 мм, а просвет интубационной трубки был 9 мм.
В связи с ростом коммерческого интереса в конце 1985 г. Dunlop по чертежам доктора Брайна сделала серию новых силиконовых масок в виде эллипса с перегородками в центральном отверстии. Этим самым предотвращалась обструкция гортани надгортанником. ЛМ стала лучше скользить, чем улучшилась ее установка. Появилась возможность выпускать воздух из баллончика до получения тонких его краев. Этим резко уменьшилась вероятность сталкивания баллончика ЛМ с надгортанником. Перестал использоваться металлический проводник и изменилась техника введения ЛМ. Она стала устанавливаться напрямую, без поворота на 180° и использования ларингоскопа.
В апреле 1987 г. был зарегистрирован 21 случай использования ЛМ у больных с трудной интубацией. В мае 1987 г. силиконовый прототип ЛМ был успешно применен постовой медицинской сестрой отделения интенсивной терапии в госпитале святого Андрея в лондонском районе Боу для реанимации больного с остановкой сердца и дыхания. До этого сестра никогда не использовала ЛМ, но методику ей объяснили на словах.
В октябре 1987 г. Брайном сконструирована назальная ЛМ и опробована у больного при удалении кисты языка. Идеей было сделать трубку разборной так, чтобы она могла бы быть удалена после установки.
ЛМ была введена в клиническую практику в 1988 г. и быстро получила распространение во всем мире, от госпиталей развитых стран до госпиталей Ганы, Камеруна и горного Непала. В США ЛМ применяется с 1992 г. и считается рутинной процедурой. J.Brimacombe, C.Verghese (1995) на ежегодном научном собрании австралийского анестезиологического колледжа в Тоунсвилле отразили опыт успешного использования ЛМ у 11 910 пациентов. В Германии первые предварительные исследования на 15 пациентах проведены в 1991 г. и были сдержанно оценены немецкими анестезиологами. Однако уже через 2 года ЛМ заняла прочное место во многих немецких клиниках.
В России внедрение ЛМ начато в 1995 г. (г. Новосибирск). Первый обзор по применению ЛМ опубликован в 1994 г. М.В. Лукьяновым, а краткое руководство В.П. Шевченко «Физиологические основы и проблемы использования ларингеальной маски» - в 1997 г. Авторами первых отечественных работ по применению ЛМ в челюстно-лицевой хирургии и стоматологии являются П.Ю. Столяренко(1999) и С.А. Рабинович с соавт. (1999).
История применения эндотрахеального наркоза в челюстно-лицевой хирургии
Уже первые попытки использовать ингаляционный наркоз при оперативных вмешательствах на лице и в полости рта встретили значительные трудности. Еще в 1847 г. Н.И. Пирогов писал, что при операциях, производимых во рту, трудно приладить надлежащим образом эфирный аппарат и очищать рот от крови и слюны. Наличие маски на лице, мешающей работе хирурга, опасности аспирации крови, слюны и рвотных масс побуждали хирургов изыскивать новые пути для введения наркотических веществ в трахею через трахеостому. Первое сообщение об этом принадлежит Н.И. Пирогову. Изучая на животных действие эфира на организм, он вводил эфир в трахею собак через трахеостому и получал достаточно глубокий наркоз. Результаты экспериментов были опубликованы Н.И. Пироговым в 1847 г. на русском и французском языках в работах: "Практические и физиологические наблюдения над действием паров эфира на животный организм", "Наблюдения над действием эфирных паров как болеутолительного средства в хирургических операциях" и "Recherches pratigues et physioloques sur l'etherisation".
В 1850 г. А. Бекетов, а в 1858 г. J. Snow повторили опыт Н.И. Пирогова. Они вводили животным через трахеостому пары хлороформа. При этом А. Бекетов рекомендовал такой способ ингаляции для применения у людей в тех случаях, когда операции подвергалась "местность ... прямо или последовательно затрудняющая применение хлороформа, как-то: некоторые операции на лице и глазах".
Однако в клинике эндотрахеальный метод наркоза впервые был применен в 1869 г. немецким хирургом Фридрихом Тренделенбургом (Trendelenburg) при резекции верхней челюсти (рис. 100).
 |
Рис. 100. Фридрих Тренделенбург (1844–1924). Выдающийся немецкий хирург, внесший вклад в развитие анестезиологии |
Наркоз проводился через трахеостому с помощью специальной трубки с надувной муфтой (рис. 101).
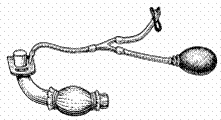 |
| Рис. 101. Трубка Тренделенбурга |
Надувная муфта предназначалась для закрытия пространства между введенной в трахею трубкой и стенками трахеи. К наружной части трубки присоединялась воронка, в которой находилась фланель, смоченная наркотическим веществом.
Как указывает Я.Л. Ясный (1962), в России впервые наркоз через трахеостому применил Р.В. Бутц в 1887 г. тоже при резекции верхней челюсти. Позднее этим методом пользовались А.П. Прокунин (1897), Н.Н. Теребинский, В.М. Минц (1907) и др.
Дальнейшее развитие методики эндотрахеального введения наркотических веществ связано с именами хирургов: сэра Уильяма Мак-Эвена (William MacEwen) в Шотландии, Джозефа О'Двайера (Joseph O'Dwyer) в США и Франца Кюна (Franz Kuhn) в Германии. По данным Howland и Lewis (1956), MacEwen в 1880 г. для удаления у больного злокачественной опухоли корня языка под хлороформным наркозом произвел интубацию трахеи через рот на ощупь металлической трубкой, затампонировал глотку и далее продолжил наркоз уже через эту трубку.
J. O'Dwyer в 1897 г. предложил при операциях в полости рта, носа и носоглотки производить интубацию трахеи специальной трубкой, через которую наркотическое вещество можно было вводить непосредственно в трахею. Интубационная трубка О'Двайера представляла алюминиевую канюлю, которая вставлялась в гортань и посредством гуттаперчевой трубки соединялась с воронкой Тренделенбурга (рис. 102). Однако, как отметил Д. Баталин (1913), эта система имела тот недостаток, что при операциях в полости рта гуттаперчевая трубка легко сдавливалась и доступ воздуха через нее затруднялся.
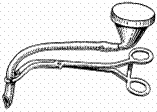 |
| Рис. 102. Трубка О'Двайера |
Более совершенным устройством для эндотрахеального наркоза был аппарат F. Kuhn, предложенный в 1901 г. Он состоял из гибкого металлического интубатора и воронки Тренделенбурга. Интубатор представлял собой трубку из металлических колец, соединенных при помощи резины так, чтобы трубка могла сгибаться, не закрывая при этом просвета. Составными частями интубатора являлись: рукоятка, крылья для фиксации трубки, сама трубка и клюв (рис. 103).
 |
Рис. 103. Франц Кюн (1866– 1929) и его интубатор |
Интубатор вводился в трахею через рот на ощупь при помощи изогнутого металлического мандрена. После введения интубатора в трахею мандрен удалялся и наружный конец интубатора присоединялся к воронке, в которой находилась уложенная слоями марля. На эту марлю наливали каплями наркотическое вещество (эфир или хлороформ). От воронки отходила гуттаперчевая трубка, служившая для контроля за дыханием больного. При интубации Kuhn рекомендовал применять трубки различных размеров в зависимости от возраста и пола больных. Перед введением интубатора он предлагал либо анестезировать слизистую оболочку гортани раствором кокаина, либо вводить больного в наркоз при помощи маски. При этом Kuhn указывал, что наркоз должен быть достаточно глубоким. После интубации производилась тампонада глотки марлевым бинтом. Kuhn успешно применил эндотрахеальный наркоз при 48 операциях в полости рта и носа. Продолжая совершенствовать методы интубации при эндотрахеальном наркозе, Kuhn в 1902 г. описал метод интубации через нос "вслепую".
Работы F. Kuhn положили начало более широкому применению эндотрахеального наркоза при операциях на лице и в полости рта. Д. Баталин (1913) сообщил, что за рубежом эндотрахеальный наркоз при операциях на лице и в полости рта в период с 1901 по 1913 г. применяли Dirck, Kohler, Sagebiel, Lotsch и др. Анализируя результаты применения эндотрахеального наркоза при операциях в полости рта, Kolle (1911) высоко оценивал метод как наиболее безопасный и удобный (цит. по И.Н. Муковозову, 1965).
Первая работа в России, посвященная применению эндотрахеального наркоза через интубационную трубку при вмешательствах на лице и в полости рта, принадлежит Д. Баталину. Она опубликована в 1913 г. в "Хирургическом архиве Вельяминова" под названием "К вопросу о пероральном тубаже гортани по способу Кuhn". В этой статье Д. Баталин привел собственные наблюдения по применению эндотрахеального наркоза в 1912 г. в клинике профессора В.М. Мыша (Томский университет) двум больным при резекции верхней челюсти и одному больному при операции по поводу рака миндалин (рис. 104).
 |
Рис. 104. Владимир Михайлович Мыш (1873–1950). Профессор факультетской хирургической клиники Томского университета, а затем Новосибирского медицинского института. Под его руководством впервые в России проведен эндотрахеальный наркоз с интубацией трахеи через рот |
В заключение Д. Баталин отмечал, что "впечатления, полученные от пероральной интубации по способу Kuhn, очень хорошие и в этом способе хирурги найдут одно из наиболее действенных средств к устранению опасностей, связанных с затеканием крови, слюны и рвотных масс в дыхательные пути". В этом же 1912 г. С.И. Спасокукоцкий (рис. 105) в своей клинике в Саратове применял эндотрахеальный наркоз с помощью аппарата Кuhn при операциях на лице и в полости рта в тех случаях, когда возникала опасность затекания крови в верхние дыхательные пути.
 |
Рис. 105. Сергей Иванович Спасокукоцкий (1870–1943). Академик, один из крупнейших советских хирургов |
Способ эндотрахеального введения наркотических веществ, который был разработан в основном для обеспечения операций в челюстно-лицевой области, с 1909 г. начинает внедряться и в грудную хирургию.
Однако при применении этого метода наркоза возникали значительные трудности, связанные с интубацией трахеи, которая осуществлялась в то время через рот на ощупь или через нос "вслепую". Положение изменилось после внедрения в практику ларингоскопа (Liliental, 1910; Jakson, 1913), при помощи которого интубацию стали производить под контролем зрения.
Интубация трахеи через нос под контролем прямой ларингоскопии была разработана Джилеспаем (Gillespie) в 1941 г. Этот вариант интубации нашел широкое использование в челюстно-лицевой хирургии и отделениях интенсивной терапии (рис. 106).
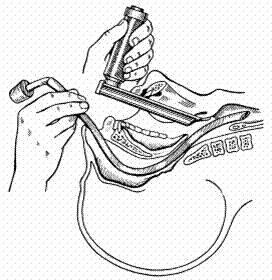 |
| Рис. 106. Схема интубации трахеи через нос под контролем прямой ларингоскопии |
Несмотря на облегчение техники интубации и некоторое усовершенствование наркозных аппаратов, этот способ наркоза долгое время в нашей стране оставался недоступным для широкого применения при операциях в челюстно-лицевой области. И.Н. Муковозов (1965) объясняет это следующими причинами. Во-первых, техника эндотрахеального наркоза все еще оставалась несовершенной, а надежных наркозных аппаратов и принадлежностей к ним было мало. Во-вторых, особенности иннервации челюстно-лицевой области давали возможность широко применять местную (проводниковую и инфильтрационную) анестезию при многих операциях в этой области. Все это привело к тому, что местное обезболивание в челюстно-лицевой хирургии и стоматологии стало господствующим.
Однако методы эндотрахеального введения наркотических веществ не были забыты. Они совершенствовались и при определенных, правда, весьма ограниченных показаниях, использовались в челюстно-лицевой области. Более широко применялся эндотрахеальный наркоз за рубежом - в Англии и Америке, особенно после создания Waters в 1923 г. новых наркозных аппаратов, работающих по закрытому способу с рециркуляцией газов и поглощением углекислоты. Этому также способствовали разработка более совершенной техники интубации и усовершенствование трубок для этой цели.
В 1925 г. на Международном конгрессе по пластической хирургии Айвэн Мэйджил (Ivan Magill) из клиники Gillis доложил о довольно широком применении эндотрахеального наркоза при пластических операциях в челюстно-лицевой области. Он несколько усовершенствовал технику интубации трахеи через нос "вслепую" и предложил изогнутые, более совершенные трубки. Flagg (1951), впервые применивший этот метод наркоза в 1927 г. в клинике, отмечает, что при операциях на лице и шее в течение последних 25 лет он стал почти обязательным. Это же сообщают и другие авторы. По данным J. Lundy (1941), эндотрахеальный наркоз в клинике Маyo с 1928 по 1940 г. был применен 12751 раз. Lundy указывает на особую ценность этого метода при операциях на голове и шее.
Эндотрахеальный наркоз применялся и во время второй мировой войны в лечебных учреждениях английских и американских армий при хирургической обработке ран челюстно-лицевой области. Так, Моwlem (1943) писал, что предварительная хирургическая обработка раненых в челюстно-лицевую область на главном перевязочном пункте должна в большинстве случаев проводиться под эндотрахеальным наркозом с тампонадой глотки. Эндотрахеальный наркоз при хирургической обработке у раненых с переломами нижней челюсти применяли Тhoma (1944) и Неnny (1951).
В нашей стране современный эндотрахеальный наркоз при операциях в челюстно-лицевой области впервые был применен в клинике челюстно-лицевой хирургии и стоматологии Военно-медицинской академии им. С.М. Кирова 31 августа 1949 г (Чуприна Ю.В., Александров Н.М.). До 1955 г. его применение носило эпизодический характер, так как наркоз проводился анестезиологами общехирургических клиник. С апреля 1955 г. проведением эндотрахеального наркоза стал специально заниматься сотрудник клиники Н.М. Александров (рис. 107), и наркоз стали применять более широко (Муковозов И.Н., 1965).
 |
Рис. 107. Никита Михайлович Александров (1923–1992). Первым в нашей стране применил эндотрахеальный наркоз в челюстно-лицевой хирургии. Генерал-майор медицинской службы. Главный стоматолог МО CCСP, начальник кафедры челюстно-лицевой хирургии и стоматологии ВМедА им. С.М. Кирова (до 1983 г.) |
Развитие обезболивания в стоматологии с 1946 года до конца XX века
Период 1946-1958 гг.
Несомненно, успехам челюстно-лицевой хирургии в значительной мере способствовало внедрение в хирургию новых методов обезболивания и элементов лечебно-охранительного и лечебно-стимулирующего режима; в частности, в литературе нашли отражение исследования, направленные на совершенствование местного обезболивания (Вайсблат С.Н., 1947-1962; Вейсбрем М.М., 1948; Даценко М.Ф. и Фетисов Н.В., 1959 и др.), местного потенцированного (Карленко С.Н., 1950; Кругляков И.О., 1951; Бернадский Ю.И., 1955-1969; Бажанов Н.Н., 1956-1962), эндотрахеального и масочного (Бердюк И.В., 1954; Александров Н.М., 1957; Митрофанов Г.Г., 1956; Муковозов И.Н., 1959-1965; Бизяев А.Ф., 1961-1967 и др.), а также гексеналового наркоза (Скопец Е.В., 1956). Особенно перспективным для использования в условиях челюстно-лицевых стационаров оказался метод потенцированного местного обезболивания с применением новых нейролептических препаратов, а в условиях поликлиники - местная анестезия, газовый наркоз закисью азота с кислородом, внутривенный наркоз.
В марте 1965 г. состоялся I Всероссийский съезд стоматологов в г. Калинине. Программным вопросом было "Обезболивание в стоматологии".
На V Всесоюзном съезде стоматологов (1968) Н.Н. Бажанов и В.Н. Александров в докладе "Задачи организации анестезиологической службы в стоматологии" отметили специфичность проведения общего обезболивания в стоматологической поликлинической практике, и проблемы, связанные с подготовкой анестезиологов для этой области медицины.
Во второй половине XX в. (60-90-е годы) вопросами обезболивания в стоматологии занимались Г. Адкина, Л.И. Алексеев, А.И. Маркин, Ю.И. Бернадский, Н.М. Александров, B.C. Стародубцев, Ю.С. Привалов, И.Н. Муковозов, П.М. Егоров, Н.Н. Бажанов, С.С. Ганина, А.Ф. Бизяев, Н.Г. Беляева, Е.В. Васманова, О.Ф. Конобевцев, С.Ф. Грицук, В.Ф. Рудько, В.Я. Рябцев, В.Н. Александров, В.К. Филатов, П.Ю. Столяренко, М.Г. Панин, А.С. Добронравов, Ю.В. Вовк, А.А. Несмеянов, Г.М. Иващенко, Н.И. Ивенский, В.П. Бережной, Н.K. Вячкилева, К.П. Шведов, А.В. Лепилин, И.А. Шугайлов, Е.Г. Шульгин, И.И. Левен, М.В. Лукьянов, Е.Н. Анисимова, А.Ж. Петрикас, С.А. Рабинович, Ю.В. Мишунин, Е. Lanz, R.Е. Walton, S.F. Malamed, Н. Еvers, Е. Glockmann, D. Schumann, R. Rahn, C.S. Reily, J.P. Rood, G.R. Seward, M. Simmons, J.Т. Jastak и многие другие (рис. 108-117).
 |
 |
|
| Рис. 108. Иван Николаевич Муковозов (1920–1992). Кандидат медицинских наук, подполковник медицинской службы. Работал в клинике челюстно-лицевой хирургии и стоматологии ВМедА им. С.М. Кирова. Автор двух монографий по наркозу в стоматологии и челюстно-лицевой хирургии (1965, 1972), по которым училось не одно поколение анестезиологов и стоматологов | Рис. 109. Николай Николаевич Бажанов. Родился в 1923 г. Академик РАМН, лауреат Государственной премии СССР, кавалер ордена СтАР "За большие заслуги перед стоматологией" I степени. Внес существенный вклад в решение проблемы обезболивания в амбулаторной стоматологической практике у больных, перенесших инфаркт миокарда, страдающих гипертонической болезнью, лекарственной непереносимостью, нервно-психическими заболеваниями | |
 |
 |
|
| Рис. 110. Владимир Федорович Рудько. Родился в 1919 г. Доктор медицинских наук, профессор кафедры хирургической стоматологии и челюстно-лицевой хирургии, академик хирургических наук Армении и международной академии им. Пьера Фошара (США). Единственный из россиян входит в состав 25 почетных стоматологов Мира. Награжден орденами Трудового Красного Знамени и "За большие заслуги перед стоматологией" I степени и 9 медалями. Под его руководством разработана и осуществлена программа целевых исследований «Борьба с болью в стоматологии». Результатом явилось внедрение в стоматологическую практику новых методик обезболивания при стоматологических операциях | Рис. 111. Всеволод Николаевич Александров (1933–1996). Доктор медицинских наук, профессор. Организатор и заведующий кафедрой анестезиологии и реаниматологии ММСИ им. Н.А. Семашко (1973–1995). Был инициатором и организатором широкого спектра исследований по обезболиванию при амбулаторных стоматологических вмешательствах. Разработал ряд методов общей анестезии. Автор более 200 научных публикаций и 18 изобретений | |
 |
 |
|
Рис. 112. Алексей Федорович Бизяев. Доктор медицинских наук, профессор кафедры факультетской хирургической стоматологии с курсом имплантологии МГМСУ. Научное направление исследований посвящено разработке метода комбинированного местного обезболивания, основанного на концепции биоэнергетической коррекции степени выраженности психоэмоционального стресса при стоматологических вмешательствах в условиях поликлиники. Автор нескольких монографий и разделов по обезболиванию в учебниках и справочнике по стоматологии |
Рис. 113. Стенли Ф. Маламед , доктор хирургической стоматологии, профессор анестезиологии и медицины. Стоматологический факультет Южнокалифорнийского университета. Лос-Анджелес, США. Автор капитального руководства по местной анестезии, выдержавшего 4 издания | |
 |
 |
|
| Рис. 114. Арнольд Жанович Петрикас. Родился в 1938 г. Заведующий кафедрой терапевтической стоматологии Тверской государственной медицинской академии, доктор медицинских наук, профессор, "Заслуженный врач РФ" (1997). Автор трех монографий, в т.ч. "Обезболивание зубов" (1997), и многих статей, касающихся различных аспектов анестезии при лечении зубов | Рис. 115. Игорь Александрович Шугайлов. Родился в 1948 г. Доктор медицинских наук, профессор, автор технологии объективной оценки болевой чувствительности человека и эффективности обезболивания в стоматологии. Основатель и заведующий кафедрой (1986–1997) анестезиологии и реаниматологии факультета усовершенствования стоматологов ММСИ, заведующий кафедрой стоматологии РМАПО МЗ РФ с 1997 г. и по настоящее время. Разработал серию карпульных инъекторов, которые прошли проверку у нас в стране, в Западной Европе, США, Новой Зеландии и получили высокую оценку специалистов | |
 |
 |
|
| Рис. 116. Дитер Шуман , профессор, доктор медицины и стоматологии. Родился в 1939 г. Челюстной-лицевой хирург. Основные работы по премедикации, регионарной и местной анестезии в челюстно-лицевой хирургии, Гeрмания | Рис. 117. Райнер Ранн. Родился в 1952 г. в Карлсруэ. Приват-доцент, доктор медицины и стоматологии. Основные работы по обезболиванию посвящены выбору местных анестетиков у пациентов с общесоматическими заболеваниями и факторами риска. Франкфурт-на-Майне, Германия |
Послеоперационное обезболивание
В 1806 г. 20-летний аптекарь из Патерборна Фридрих Вильгельм Адам Сертюрнер (Serturner F.) выделил активный компонент опия (рис. 118, 119). Болеутоляющие свойства опиумного мака были известны многие столетия. Сертюрнер первым назвал новый алкалоид "рrincinium somniferum", но в последующем изменил его на "морфин" в честь Морфея, греческого бога сна (Macht D.J., 1915).
 |
Рис. 118. Фридрих Вильгельм Адам Сертюрнер (1763–1841), немецкий химик и фармацевт. Образование получил самостоятельно, работал аптекарем в Гамелне. Основное направление - фармацевтическая химия. Впервые выделил активное вещество из опийного мака |
 |
| Рис. 119. Восточный мак. Опиум представляет собой сухой порошок, полученный из сока незрелых коробочек мака |
Изобретение шприца и игл позволило врачам готовить и вводить точно дозированные количества морфина, а в последующем местных анестетиков. Эти достижения и открытие мощных местно-анестезирующих свойств кокаина открыли дорогу все более обширным хирургическим вмешательствам (Madigan S.R., Raj P.P., 1992).
Ceorg Krile (Джордж Крайль) в самом начале 1890-х годов предположил, что преодоление послеоперационной боли окажет благоприятное влияние на результаты операции (рис. 120).
 |
Рис. 120. Джордж Крайль (1864–1943). Американский хирург, профессор (1900). Ему принадлежат десятки новаторских предложений в различных областях хирургии, в т.ч. оперативное лечение метастазов рака некоторых органов полости рта (операция Крайла). По проблеме обезболивания: предложил восстановление сердечной деятельности с помощью адреналина (1904), сочетание наркоза с местной анестезией (1914) |
Хороший обзор по вопросам возможных последствий неконтролируемой боли представлен Вrovn (1989).
На протяжении всей истории развития местной анестезии исследователи пытались найти способы пролонгации местно-анестезирующего эффекта (Sunada К., Furuya Н., 1993). (Цит. по С.Т. Сохову и соавт., 2000.) В целом было предложено более 60 способов удлинения и углубления анестезии, однако многие из них не нашли широкого применения.
Новокаин был первым из синтетических местных анестетиков, введенных в клиническую практику. Он обладает сравнительно слабым обезболивающим действием, которое проявляется медленно и длится недолго. Относительно малая активность и быстрый гидролиз в крови объясняют слабую токсичность новокаина. Однако парааминобензойная кислота, образующаяся при гидролизе, вызывает аллергические реакции, особенно при повторном введении.
Лидокаин был первым из препаратов группы амидов, широко применяемых в клинике. Бупивакаин был первым из местных анестетиков, сочетающих в себе способность вызывать быстрое и длительное обезболивание при четком разграничении сенсорной и двигательной блокады. Обезболивающее действие этидокаина развивается быстрее, чем у бупивакаина. Наиболее совершенным из местных анестетиков длительного действия является ропивакаин (наропин).
Чрескожная электронейростимуляция (ЧЭНС). Электростимуляцию для обезболивания и лечения различных заболеваний, как указывалось ранее, использовали еще в древности. Электричество применяли для лечения болей уже в античные времена. В 46 г. н.э. римский врач Скрибоний Ларгин использовал электрических угрей для лечения подагры, головных болей и других болезней (Кеllaway Р., 1946; Кane K., Тaub А., 1975). Больной орган пациента помещали в ванну с водой, где плавала эта рыба. В некоторых случаях пациенты теряли сознание, но боли проходили или ослабевали.
В ХVII и ХVIII веках возрос интерес к электричеству и его связи с биологией. Благодаря исследованиям Жильборта, фон Гуерика, Грея, Гальвани, Вольта было установлено, что электричество можно производить, хранить и передавать (Becker R.O., Маrino А.А., 1982). Многие врачи и шарлатаны начали использовать электричество для лечения различных болезней. Книга под названием "Электрическая медицина" была опубликована Иоганом Шнеффером в 1752 г.
С середины XIX века в США начали производить ручные стимуляторы. Они приобрели наибольшую популярность в 1910-1940 годах и продавались в большинстве магазинов. Однако пределы технических возможностей и прогресс фармакотерапии снизили интерес к электростимуляции (Katz N., 1998).
В 1965 г. R. Melzack и P. Wall предложили свою теорию "ворот боли". Они выдвинули гипотезу, что афферентная активность больших миелинизированных волокон (А) блокирует центральную трансмиссию ноцицептивных импульсов по малым миелинизированным волокнам (А) и немиелинизированным волокнам (С-волокна), закрывая таким способом "ворота" трансмиссии болевых импульсов. Эта теория дала новый толчок для изучения нервной стимуляции и её роли при анальгезии.
В 1967 г. P. Wall и W. Sweet при воздействии электростимулятором на подглазничный нерв у здоровых лиц отметили снижение болевой чувствительности в его области.
А. Нуmes и сотр. в 1973 г. первыми сообщили о применении ЧЭНС при острых послеоперационных болях. После работ этих авторов ЧЭНС стали применять во многих лечебных учреждениях всего мира в борьбе с хронической и послеоперационной болью.
ЧЭНС - это один из неинвазивных и безопасных методов анальгезии. Несмотря на обезболивающий эффект, подтвержденный клиническими и лабораторными наблюдениями, до сих пор не получено данных, подтверждающих прямую причинную связь между анальгезией и проводимой стимуляцией. Тем не менее ЧЭНС может стать ценным методом в определенных клинических ситуациях (Katz N., 1998).
Криоанальгезия . Заключается в воздействии низких температур на нервы с целью обезболивания. Самый обычный криозонд вызывает замораживание при выпускании под повышенным давлением закиси азота через узкое отверстие на верхушке зонда (рис. 121).
 |
| Рис. 121. Аппарат для криоанальгезии с криозондами. (Ил. по Ф. Ферранте, Т.Р. ВейдБонкору, 1998.) |
Замораживание происходит в результате расходования тепла на испарение закиси азота или углекислого газа. М. Маiwand и сотр. (1986) показали, что оптимальная блокада обеспечивается при охлаждении каждого нерва в течение не менее 30 с. Однократный цикл замораживания вместо двух 30-секундных циклов создает анальгезию сроком на 1 месяц и снижает частоту расстройств чувствительности. Однако даже при однократном цикле замораживания все же возможно повреждение нерва, хотя сохранение эндотелия обеспечивает со временем прорастание нейронов.
Акупунктура . Уже 4000 лет назад в Китае было известно, что введение игл в определенные точки тела вызывает анальгезию. Согласно китайской философии Чи, жизненная сила циркулирует в теле по путям, называемым меридианами. Повреждение и заболевание могут блокировать эту циркуляцию, вызывая боль и расстройства. Полагают, что акупунктура снимает такие блоки и восстанавливает баланс энергии человека. Традиционно акупунктурные точки стимулируются путем введения тонких игл, которые затем вращаются вручную или стимулируются с помощью тепла (моксинагревание) или электричества. Чтобы акупунктурная анальгезия была эффективной, пациент должен испытывать чувство тяжелого онемения (называемого те-чи), распространяющегося от акупунктурной точки.
Можно считать, что акупунктура продуцирует высокоинтенсивную низкочастотную стимуляцию. Полагают, что она вызывает выброс энкефалинов и эндорфинов, которые ответственны за наблюдаемые анальгетический и седативный эффекты.
В стоматологии чаще используют блок тройничного нерва и его ветвей при лечении больных невралгией тройничного нерва.
В 1883 г. Тирш (Thiersch) предложил неврэкзерез, а в 1903 г. Шлессер (Schlosser C.) - алкоголизацию нервов.
В 1931 г. удалось добиться продления действия местной анестезии получением тетракаина (введением заместителя в ароматическое кольцо прокаина). Но вещество оказалось в 10 раз токсичнее, чем прокаин, и поэтому в сегодняшней стоматологии применяется только для поверхностной анестезии.
Одним из путей повышения эффективности местной проводниковой анестезии в челюстно-лицевой хирургии является продленная проводниковая блокада (ППБ) ветвей тройничного нерва. Метод предложен П.Ю. Столяренко в 1987 г. Сущность его заключается в подведении ко 2-й или 3-й ветви тройничного нерва местного анестетика внеротовым доступом через тонкий пластиковый катетер (рис. 122).
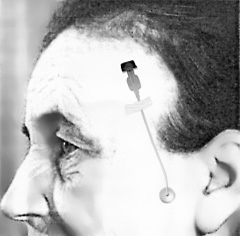 |
Рис. 122. Вид больной с катетером для продленной проводниковой блокады 3-й ветви тройничного нерва |
Это позволило усовершенствовать методики комбинированного обезболивания во время операций, а также исключить в послеоперационном периоде назначение опиатов, угнетающих дыхание и кашлевой рефлекс, усиливающих посленаркозную депрессию и возможность возникновения ятрогенной наркозависимости. Применение катетера, обеспечивающего повторное введение болюсных доз или постоянную инфузию местного анестетика, G. Smith (1998) считает наиболее эффективным способом пролонгации обезболивания.
В 80-е годы уходящего века появился метод создания лекарственных веществ направленного действия за счет сочетания известных препаратов с особыми магнитными носителями, способными обеспечивать их адресную доставку к органам. Экспериментально-клиническая разработка магнитоуправляемого местного анестетика феррокаина позволила кумулировать анестетики в биологически активных тканях под действием внешнего магнитного поля и начать клиническое применение в амбулаторной стоматологии (Сохов С.Т., 1997).

