двухмесячный научно-образовательный журнал
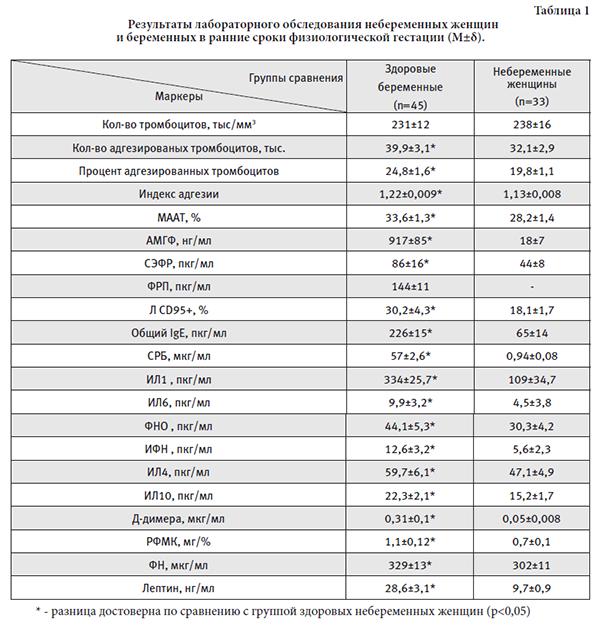
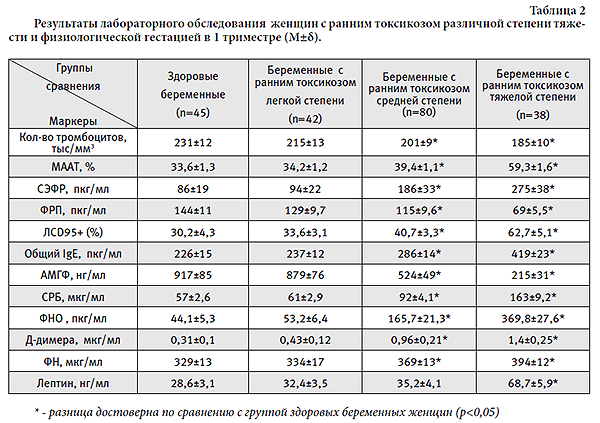
"Тольяттинский медицинский консилиум" 2016г. № 1-2Значение факторов физиологического повреждения, эмбриоплацентарной дисфункции и синдромов гестационной дезадаптации в формировании гетерогенных вариантов течения беременности в I триместреЮ.В. Тезиков1, И.С. Липатов1, О.А. Кутузова2, А.В. Приходько1, Н.А. Фролова1, Т.А. Тезикова2, О.В. Бренерова3 The value of the factors of physiological damage, embriofetal dysfunction and syndromes of gestational maladjustment in the formation of heterogeneous variants of pregnancy in the first trimesterYu.V. Tesikov, I.S. Lipatov, O.A. Kutuzova, A.V. Prichodko, N.A. Frolova, T.A. Tesikova, O.V. Brenerova РезюмеЦель исследования - выделение клинико-патогенетических вариантов раннего токсикоза беременных с учетом клинических проявлений и маркеров ведущих патогенетических синдромов гестационной дезадаптации. В 1 триместре гестации обследованы 45 здоровых беременных женщин и 160 беременных с ранним токсикозом различной степени тяжести. Группу сравнения составили 33 здоровые небеременные женщины. Обследование включало оценку клинической симптоматики, определение маркеров воспалительной реакции, энергетического баланса репродуктивной системы, функциональной активности эндометрия, сосудисто-эндотелиальных и гемостазиологических нарушений, биохимических показателей крови. Исследование позволило количественно объективизировать факторы «физиологического повреждения» и «механизмы гестационной адаптации» при физиологической гестации, выделить эмбриоплацентарную дисфункцию в качестве основного звена дезадаптации в ранние сроки беременности. Преобладание патогенетических механизмов формирования раннего токсикоза предопределило выделение 4 клинико-патогенетических вариантов течения данного осложнения гестации. Ключевые слова: физиологическая беременность, ранний токсикоз, эмбриоплацентарная дисфункция, вегетативный дисбаланс, лептин, цитокины, факторы роста, апоптоз ВведениеДля понимания механизмов осложненного течения беременности необходимо четкое представление о формировании физиологической гестации, «норме беременности» на новом этапе развития акушерской науки [1-4]. Оценка гомеорезиса при беременности актуализирована в связи с необходимостью уточнения границ физиологической гестации, являющейся непрерывным компенсаторно-приспособительным процессом, и патологических состояний, угрожающих неблагоприятными гестационными и перинатальными исходами [5-9]. Формирование нового сосудистого русла во время беременности тесно связано с гемохориальным типом плацентации, что и обуславливает альтерацию в области плодного яйца и соответствующую реакцию организма беременной [10-14]. Существует точка зрения, что альтерация в рамках физиологического процесса (факторы повреждения - нидация, умеренное воспаление децидуальной оболочки, повреждение и перестройка маточно-плацентарных сосудов, плацентация, недостаток кислорода в тканях эмбриоплацентарного комплекса и оксидативный стресс, медленный маточно-эмбриональный ток крови с активацией коагуляционного потенциала, повышение регуляторных уровней аутоантител и реагинов, гестационный сдвиг метаболизма и др.) компенсируется механизмами гестационной адаптации [15-19]. Однако, соотношение этих процессов, их значение для формирования и течения беременности до настоящего времени не ясны. Анализ литературы последних лет показал, что причина манифестации раннего токсикоза до настоящего времени не определена. Ранний токсикоз по данным статистики осложняет беременность на ранних сроках у 40-60% женщин [20-24]. В большинстве наблюдений нарушения в организме беременной мало выражены и не требуют лечения. У подавляющего числа беременных рвота или другие проявления раннего токсикоза диагностируются между 4-й и 6-й неделями гестации. Общепризнано, что к факторам, предрасполагающим к развитию токсикоза относятся хронические заболевания желудочно-кишечного тракта, хронические заболевания печени, астенический синдром, нарушение функции щитовидной железы, нервно-психические заболевания, юный возраст беременной (до 18 лет), трофобластические заболевания в анамнезе, сахарный диабет, бронхиальная астма и др. [25, 26]. Основной этап становления эмбрио(фето) плацентарной системы приходится на время реализации раннего токсикоза у беременных [27]. До настоящего времени имеют место несколько теорий развития раннего токсикоза: токсическая рвоту беременных связывают с отравлением токсичными продуктами обмена веществ; иммуногенетическая теория - сенсибилизация материнского организма антигенами плода при гистосовместимости; нервно-психическая теория - отрицательные эмоции, страх перед беременностью и родами; нервно-рефлекторная - нарушение взаимоотношений деятельности центральной нервной системы и внутренних органов [28]. Согласно доминирующим взглядам акушеров-гинекологов, ранний токсикоз беременных рассматривается как проявление нарушений нейроэндокринной регуляции всех видов обмена вследствие частичного или полного голодания и обезвоживания [29]. Современные представления о формировании ранних сроков беременности предопределяют, что ранний токсикоз клинически проявляется не только диспепсическими расстройствами и рвотой беременных. Ранний токсикоз - это гетерогенное осложнение первой половины беременности, методологию диагностики и лечения которого определяет риск развития поздних осложнений беременности [30, 31, 32]. Осложнения первой половины беременности являются зеркалом более глубоких и специфических для гестации нарушений на этапе инвазии цитотрофобласта первой волны и предиктором тяжелых гестационных осложнений второй половины беременности (плацентарной недостаточности, преждевременных родов, преэклампсии и др.) [15, 19, 21]. Согласно научным работам ряда авторов, в развитии эмбриоплацентарной дисфункции важная роль отводится синдромам системного воспалительного ответа, эндотелиально-гемостазиологической дисфункции, функциональной недостаточности эндометрия, метаболических нарушений, вегетативного дисбаланса [3, 15, 29]. Механизмы дезадаптации организма беременной к развитию гестации отражаются как на плодном яйце, в том числе и на ранней плаценте, так и реализуются через полисистемную и полиорганную дисфункцию и недостаточность (системный воспалительный ответ, активация сосудистотромбоцитарного звена гемостаза, иммунопатологические реакции, аллергизация, метаболические и нейровегетативные нарушения) [9, 10, 21]. В качестве компенсаторно-приспособительной реакции, на ранних этапах развития тяжелых осложнений гестации, активируется индуцированный трофобластом апоптоз иммуннокомпетентных клеток, для повышения активности защитных механизмов синтезируются белки острой фазы воспаления, повышаются регуляторные уровни реагинов и др. [6, 14, 16]. Отсутствие единых взглядов на патогенез раннего токсикоза ведет к применению традиционного симптоматического лечения клинических проявлений данного осложнения. Недооценка степени повреждающих факторов срыва физиологической адаптации беременной ведет к отсутствию прогнозирования и профилактики поздних осложнений, непосредственно развивающихся на фоне раннего токсикоза. Выделение клиникопатогенетических вариантов дезадаптации на ранних сроках позволит дифференцированно проводить диагностику и лечение, причем, с учетом характера патогенетических нарушений, лечение преобразуется из симптоматического в патогенетическое. Выделение клинико-патогенетических вариантов патологического течения ранних сроков гестации позволит формировать группу высокого риска развития поздних осложнений беременности и снизить число репродуктивных потерь, улучшить качество перинатальных исходов. Цель исследования - выделение клинико-патогенетических вариантов раннего токсикоза беременных с учетом клинических проявлений и маркеров ведущих патогенетических синдромов гестационной дезадаптации. Пациент и методыДля выявления направленности изменений гомеостаза в ранние сроки физиологической беременности обследованы 45 здоровых беременных женщин в период от 7 до 12 нед. гестации (1 группа) и 33 здоровые небеременные женщины (2 группа сравнения). Средний возраст в 1 группе составил 26±1,5 лет, во 2 - 25±1,8 лет (p>0,05). Все женщины 1 группы были первобеременными. Для изучения патогенеза раннего токсикоза и выделения клинико-патогенетических вариантов гестационной дезадаптации беременных на ранних сроках проведено исследование 160 беременных женщин с ранним токсикозом различной степени тяжести. Критерии включения: срок беременности – 1 триместр. Критерии исключения: наследственные заболевания, тяжелая экстрагенитальная патология, острые инфекционно-воспалительные заболевания половых органов, аномалии развития плода. Для оценки течения беременности женщины были разделены на три группы: 1a группу составили 42 беременные с ранним токсикозом легкой степени; 1б группу – 80 беременных с ранним токсикозом средней степени тяжести; 1с - 38 беременных с тяжелым течением раннего токсикоза. Средний возраст в группах сравнения составил 24,5±2,1, 26±1,9, 27±2, 2 лет (p>0,05) соответственно 1а, 1б, 1с группам. Во всех группах соотношение перво- и повторнобеременных было одинаковым. У всех беременных проводился углубленный анализ клинической симптоматики в сопоставлении с результатами лабораторно-инструментального обследования. Обследование женщин групп сравнения включало определение в крови содержания маркеров воспалительной реакции - ИЛ1β, ИЛ6, ФНОα («лиганд смерти» системы Fas/APO-1/CD95), ИФНγ, белка острой фазы воспаления – С-реактивный белок (СРБ), противовоспалительных цитокинов - ИЛ4 и ИЛ10; маркера энергетического баланса репродуктивной системы – лептина; маркера функциональной активности эндометрия - альфа-2-микроглобулина фертильности (АМГФ); маркеров сосудисто-эндотелиальных и гемостазиологических нарушений - сосудисто-эндотелиального фактора роста (СЭФР), фактора роста плаценты (ФРП), лимфоцитов с фенотипом CD95+ (Л CD95+ или FasR, рецептор системы Fas/APO-1/ CD95), общего иммуноглобулина Е (IgE), фибронектина (ФН), Д-димера, РФМК, количество, адгезивные (количество и процент адгезированных тромбоцитов, индекс адгезии) и агрегационные свойства тромбоцитов (максимальная амплитуда агрегации тромбоцитов – МААТ); биохимических показателей крови (общий белок, белковые фракции, глюкоза, АлАТ, АсАТ, протромбиновый индекс, билирубин, кетоновые тела, липидный спектр, остаточный азот, ТЩФ). Уровни ИЛ1β, ИЛ6, ФНОα, ИФНγ, ИЛ4, ИЛ10, лептина, СРБ, общего IgЕ, СЭФР, ФРП, АМГФ в сыворотке крови, плазменную концентрацию ФН определяли методом иммуноферментного анализа с применением наборов реагентов (ООО «Протеиновый контур»; DSL (USA); «Вектор-Бест»; «Дитатех-Э»; «R&D systems»; «Pharmacia diagnostika»; «АМГФ-Фертитест»; ИФА-ФН (ЗАО «НВО-Иммунотех»)). Идентификация Л CD95+ осуществлялась стандартным методом иммунофлуоресцентного анализа с использованием моноклональных АТ к АГ лимфоцитов человека, меченых FITS Fab-фрагментами антимышиных иммуноглобулинов производства «МедБиоСпектор» (Россия). Для иммунофенотипирования лимфоцитов использовался метод лазерной проточной цитометрии. Относительное количество Л CD95+ определялось на проточном цитометре Becton Dickinson FACS Calibur с помощью компьютерной программы Cell Quest Pro. Уровень Д-димера определялся методом ELISA (ЗАО «Биохиммак»), РФМК с применением РФМК-теста (ООО «Технология-Стандарт»). Подсчет количества тромбоцитов проводился на гематологическом анализаторе «МЕК 5103» (CELLTAC, Япония). Тромбоцитарное звено гемостаза изучали путем определения адгезивных свойств тромбоцитов по ЛИПК (Одесская Т.А. с соавт., 1971) и их агрегационных свойств на лазерном агрегометре (BIOLA Ltd., модель 230 LA). Биохимические исследования проводились на биохимическом анализаторе Stat Fax 4500+. Для оценки эмбриоплацентарной системы применялась ультразвуковая система GE Voluson S6 (GE Healthcare, США). Для определения исходного вегетативного тонуса, отражающего направленность функционирования вегетативной нервной системы в период относительного покоя, использовали анализ субъективных и объективных симптомов по таблицам А.М. Вейна (2003). Нормой считали количество ваготонических признаков не более 6, а симпатикотонических – не более 2, при увеличении количества пороговых значений делали заключение об исходном вегетативном тонусе по ваготоническому или симпатикотоническому типу. Кроме того, определяли интегративные показатели – индекс Кердо, коэффициент Хильдебранта, проводили клиноортостатическую пробу. Результаты их обсуждениеРезультаты лабораторного тестирования выявили различия между женщинами с физиологической гестацией и здоровыми небеременными женщинами по содержанию в сыворотке крови провоспалительных цитокинов (увеличение ИЛ1β в 3 раза, ИЛ6 – в 2,2 раза, ИФНγ – в 1,7 раза, ФНОα – в 1,4 раза), СРБ – повышение концентрации в десятки раз (57±2,6 мкг/мл и 0,94±0,08 мкг/мл соответственно) – таблица 1. Это свидетельствует в пользу активации первичного иммунного ответа в ранние сроки физиологической беременности в виде неспецифической воспалительной реакции на альтерацию децидуальной оболочки в процессе имплантации плодного яйца, инвазию цитотрофобласта, повреждение спиральных артерий с формированием гемохориального типа плацентации [6, 8, 16]. Данные отклонения гомеостаза сдерживаются от реализации системного воспалительного ответа повышением уровня противовоспалительных цитокинов и перестройкой иммунного ответа матери в сторону Th2-доминирования [12]. Проведенный анализ содержания противовоспалительных цитокинов показал их достоверное (p<0,05) повышение: ИЛ4 в 1,3 раза, ИЛ10 в 1,4 раза по сравнению с группой небеременных. Кроме того, в поддержании физиологического развития гестации важная роль принадлежит сбалансированному влиянию факторов роста и запрограммированной клеточной гибели [27, 28]. Благодаря процессу апоптоза, происходит элиминация активированных клонов лимфоцитов, поддержание механизма материнской иммунотолерантности и фетопротекции в период гестации [9, 20]. Выявленные в группе здоровых беременных изменения содержания Активированные эндотелиоциты высвобождают в больших количествах тканевый фактор – ФН, что увеличивает коагуляционный потенциал крови. Содержание ФН в группе здоровых беременных составило 329±13 мкг/ мл, что отличается от небеременных 302±11 мкг/мл. Однако, с ранних сроков гестации в формирующейся плаценте включается комплекс противосвертывающих факторов (аннексин V, простациклин и др.), что при физиологическом процессе сдерживает гиперкоагуляционный потенциал [1, 16, 29]. В выявленную закономерность укладываются и результаты по функциональной активности тромбоцитов: в ранние сроки беременности в ответ на «физиологическую альтерацию» сосудов в маточно-эмбриональной области происходит активация тромбоцитарного звена (достоверное увеличение адгезированных тромбоцитов, процента адгезированных тромбоцитов, индекса адгезии, МААТ, p<0,05). Согласно известным механизмам формирования и течения беременности, результатам данного этапа исследования, при физиологической гестации имеют место факторы «физиологического повреждения» (альтерация эндометрия и вскрытие спиральных артерий с образованием гемохориального типа плацентации, умеренное воспаление, активация иммунного ответа, оксидативный стресс и др.) и «механизмы гестационной адаптации» (повышение уровня трофоадаптивных гормонов, противосвертывающих и антиоксидантных факторов, локальная и системная супрессия, иммунный ответ по Th2 пути, апоптоз активированных лимфоцитов, стабильный просвет спиральных артерий и др.), равновесие которых выработалось и закрепилось в процессе филогенеза вынашивания беременности. Нарушение равновесия между «механизмами адаптации» и «физиологическим повреждением» ведет к морфофункциональным изменениям в системе «мать-плодное яйцо» с развитием «эмбриоплацентарной дисфункции / недостаточности» [6, 8, 15, 16]. Результаты лабораторного обследования выявили различия между женщинами с физиологической гестацией (1 группа) и беременными с ранним токсикозом различной степени тяжести (1а, 1б, 1с) по содержанию в крови маркеров гестационной дезадаптации (таблица 2). Проанализировав полученные результаты, можно отметить, что клинические проявления раннего токсикоза различной степени тяжести являются отражением срыва механизмов гестационной адаптации, что соотносится с повышением уровня маркеров неспецифической воспалительной реакции (увеличение провоспалительных цитокинов, белков острой фазы воспаления, активация сосудистого эндотелия, коагуляционного потенциала крови). Также характерной особенностью является значимая корреляционная взаимосвязь между повышением маркеров системного воспалительного ответа, содержания сосудистоэндотелиального фактора роста, снижением уровня фактора роста плаценты, уменьшением общего количества тромбоцитов, повышением максимальной агрегации тромбоцитов, увеличением уровня Д-димера (раннего маркера фибринообразования и фибринолиза), увеличением содержания фибронектина (маркера сосудистого эндотелия и состояния гемостаза), повышением уровня лептина (маркера метаболических нарушений) и клиническими проявлениями раннего токсикоза (k от 0,71 до 0,93). Следует отметить, что чем выраженнее отклонения маркеров гестационной дезадаптации от физиологической «нормы беременности», тем ярче клиническая картина и выше степень тяжести раннего токсикоза. Кроме того, было выявлено, что при идентичных изменениях маркеров гестационной дезадаптации клинические проявления у беременных на ранних сроках имеют как общие, так и отличающиеся друг от друга симптомы. Это позволило предложить дифференцированный поход к диагностике, а, соответственно, и к лечению раннего токсикоза, по сути – выделение различных вариантов течения раннего токсикоза, что может быть перспективным в отношении новой клинико-патогенетической классификации данного осложнения беременности. Так, отмечена достоверная корреляционная связь между маркерами эмбрио(фето)плацентарной дисфункции, повышением уровня лептина, понижением уровня глюкозы и клиническими проявлениями в виде потери массы тела, снижения или отсутствия аппетита, нарушения вкусовых пристрастий, а также повышения печеночных проб (АлАТ, АсАТ), гипопротеинемии, снижения гемоглобина в периферической крови, появления симптомов анемии. Все перечисленные маркеры были объединены в клинико-патогенетический вариант раннего токсикоза с преимущественным нарушением метаболических процессов. Данный вариант течения раннего токсикоза составил 46, 9% (75 наблюдений). У 23,8% (38 наблюдений) беременных, наряду с наличием маркеров гестационной дезадаптации (умеренное повышение маркеров воспалительного ответа, умеренное снижение факторов роста, контролирующих ангиогенез в эмбриоплацентарном комплексе), отмечали такие симптомы как усталость, сонливость, психоэмоциональная неустойчивость, снижение артериального давления, лабильность частоты сердечных сокращений, парестезии и судороги в конечностях, извращение вкуса, гиперосмия, отсутствие аппетита, коллаптоидные реакции, достоверное снижение индекса Кердо, значительное преобладание парасимпатической системы при балльной оценке состояния вегетативной системы. Этот комплекс проявлений составил основу клинико-патогенетического варианта с преобладанием нейровегетативных нарушений. Третья группа симптомов суммировалась из следующих параметров: воспалительные заболевания органов репродуктивной системы, наличие хронической урогенитальной инфекции, указание на акушерские и гинекологические манипуляции, дисбиоз влагалища, клинические проявления угрозы прерывания беременности, нарастание маркеров системного воспалительного ответа, эндотелиально-гемостазиологической дисфункции, тромбоцитопении, агрегационной активности тромбоцитов, наследственные тромбофилии. Перечисленные маркеры стали основой клинико-патогенетического варианта с развитием гестационного эндотелиоза, то есть с проявлениями эндотелиально-гемостазиологической дисфункции. Четвертая группа беременных объединила особо тяжелые формы раннего токсикоза - бронхиальная астма беременных, герпетиформное импетиго, острая жировая атрофия печени, дерматозы беременных, тетания беременных, остеомаляция беременных (менее 1-2% [2, 5, 26]). На наш взгляд, выделение данных клинико-патогенетических вариантов позволит осуществлять индивидуальное наблюдение и выбирать методы коррекции осложнений ранних сроков с учетом не только клинических проявлений, но и маркеров патогенетических нарушений, дополняя традиционные методы диагностики и лечения персонифицированными подходами. Выводы
Литература
|