Anaesthesiology,
2008; 109:318–38
Temperature Monitoring and Perioperative Thermoregulation
Daniel I. Sessler, M.D.
Мониторинг температуры и терморегуляция в периоперационном периоде.
Часть 1.
Большинство доступных в современной медицине термометров позволяют достаточно точно измерять температуру, независимо от того, температура какой ткани определяется.
Сложность состоит в отсутствии абсолютно неинвазивных и удобных для использования достоверных мест измерения температуры, особенно у пациентов, которые ведутся без использования общей анестезии. Тем не менее, у большинства пациентов корректное измерение температуры возможно. Температура тела должна обязательно контролироваться при продолжительности общей анестезии более 30 минут, и у пациентов, которым выполняются «большие» операции с использованием нейроаксиальной анестезии. В обычных условиях центральная температура тела жестко контролируется. Все препараты, используемые для общей анестезии, приводят к существенному снижению центральной температуры тела, четко связанному с дозой, что в свою очередь приводит к запуску механизмов защиты от переохлаждения – артерио-венозное шунтирования, вазоконстрикции и дрожи. Обусловленное использованием анестетиков нарушение нормальных механизмов терморегуляции, приводящее к перераспределению тепла между центральными и периферическими отделами тела, является главной причиной гипотермии у большинства пациентов. Нейроаксиальная анестезия также приводит к повреждению нормальных механизмов терморегуляции, хотя и в меньшей степени, чем общая анестезия. Продолжительная эпидуральная анальгезия связана с гипертермией, причина которой на сегодняшний день остается неясной.
В предыдущих статьях я рассмотрел вопросы терморегуляции у хирургических пациентов1, осложнения, связанные с периоперационными колебаниями температуры2, этиологию и лечение послеоперационной дрожи3. В работе Heier and Caldwell4 сделан обзор влияния гипотермии на чувствительность организма к миорелаксантам. Более того, появилась отдельная монография, посвященная приобретающей все более важное звучание теме терапевтической гипотермии5. В данной статье я с запозданием остановлюсь на вопросах мониторинга температуры и влияния общей и нейроаксиальной анестезии на контроль терморегуляции.
Хирургическое вмешательство как правило бывает сопряжено с пребыванием пациента в холодном помещении, вливанием холодных растворов, испарением из зон операционных разрезов. Впрочем, сами по себе эти факторы обычно не приводят к гипотермии; наоборот, действующие в организме механизмы терморегуляции должны эффективно поддерживать центральную температуру тела постоянной при воздействии соизмеримых стрессовых факторов. То, что развитие гипотермии у предварительно «несогретых» хирургических пациентов возникает практически всегда, является следствием сбоя в работе отлаженных механизмов терморегуляции. Таким образом, понимание особенностей влияния анестетиков на существующие механизмы терморегуляция является ключом к решению проблемы периоперационных колебаний температуры; так как именно непосредственное действие анестетиков (в гораздо большей степени, чем холод в операционной) является причиной большинства температурных нарушений, с которыми мы сталкиваемся у хирургических пациентов.
В своей статье я сначала коротко расскажу о мониторинге температуры и механизмах терморегуляции, а затем перейду к обсуждению влияния общей и нейроаксиальной анестезии на поддержание температуры.
Мониторинг температуры
Температура тела неоднородна: обычно температура в глубине грудной и брюшной полостей, а также в центральной нервной системе (т.н. центральная температура) на 2-4°С градуса выше температуры конечностей; а температура большей части поверхности кожи еще холодней. В отличие от центральной температуры, постоянство которой строго поддерживается, температура кожи значительно меняется при изменениях окружающей среды; температура же периферических тканей (в основном речь идет о конечностях) зависит и от температуры окружающей среды в данный конкретный момент и в предшествующий период, и от величины центральной температуры, и от терморегуляторных сосудо-двигательных реакций. Центральная температура, хотя и не может ни в коей мере являться всеобъемлющей характеристикой содержания и распределения тепла в организме, является оптимальным индикатором температурного статуса человеческого организма.
Мониторинг центральной температуры (а именно, температуры в барабанной перепонке, легочной артерии, дистальном отделе пищевода или в носоглотке) используется для контроля интраоперационной гипотермии, предотвращения перегревания и способствует выявлению злокачественной гипертермии. Поскольку измерение температуры в вышеперечисленных местах не всегда доступно и удобно, в клинической практике также используют ряд других «околоцентральных» мест. К подобным «околоцентральным» местам относятся полость рта, подмышечная область, мочевой пузырь, прямая кишка и поверхность кожи. Каждый из этих вариантов имеет свои ограничения, но может быть использован в клинике при соответствующих обстоятельствах.
До сих пор точно не установлено, какая степень точности измерения температуры необходима в клинической деятельности. Хорошая практическая рекомендация, подтвердившая свою эффективность при проведении многих исследований, предлагает считать допустимой суммарную погрешность измерения (погрешность термометра + погрешность «околоцентральности» места измерения) не более 0,5°С. Одной из основ данной рекомендации являются данные, указывающие, что именно 0,5°С - это то минимально значимое изменение температуры, которое может приводить к осложнениям, связанным с гипотермией6.
Температуры мышц и поверхности кожи могут быть использованы для оценки сосудодвигательных реакций7 и убеждают в ценности периферического нейро-мышечного мониторинга4. Температура мышц также используется для определения температуры периферических отделов и регионального распределения тепла тела8-10. Для оценки влияния различных анестетиков на механизмы терморегуляции11 и оценки средней температуры тела (СТТ)12 необходимо производить измерение величин, как центральной температуры тела, так и средней температуры поверхности кожи.
Термометры
Ртутно-стеклянные термометры очень медленны и громоздки; кроме того, пролившаяся ртуть токсична; поэтому они практически исчезли из клинической практики, хотя остаются весьма полезными для лабораторной калибровки других типов термометров. Наиболее распространенными видами электронных термометров являются термисторы и термопары. Термисторы – это чувствительные к изменениям температуры полупроводники; работа термопар основана на возникновении очень слабого электрического тока между двумя разными соединенными металлами. Оба типа устройств достаточно точны для целей клинической практики и достаточно дешевы, чтобы их использовать как одноразовые. Однако, сигналы, получаемые от этих типов термометров, по своей сути нелинейные и поэтому их необходимо линеаризовать при помощи калиброванных компенсирующих устройств.
Другим популярным типом термометров в последние 10 лет стали инфракрасные датчики. Их принцип работы заключается в регистрации инфракрасного излучения, испускаемого всеми поверхностями, имеющими температуру выше абсолютного нуля. Соответственно, при использовании данного типа датчика нет необходимости прикасаться к поверхности исследуемого места (что весьма ценно, например, при измерении температуры расплавленной лавы и металлов). Эти термометры точны и относительно недороги. Модели, используемые в клинической практике, позволяют измерять температуру поверхности кожи с точностью до десятой доли градуса. Если же регистрировать инфракрасное излучение, излучаемое барабанной перепонкой, то результаты этого измерения являются фактически значением центральной температурой13,14. Однако, все доступные на практике датчики слишком велики для того, чтобы их можно было продвинуть больше чем на несколько миллиметров вглубь ушного канала и реально не «видят » достаточно близко к барабанной перепонке. При стандартном использовании, т.е. при ориентации на ушной канал15 или височную артерию16, инфракрасные системы недостаточно точны для нужд клинической практики (рис.1). С учетом описанных недостатков, нельзя признать удачной завоеванную ими популярность.
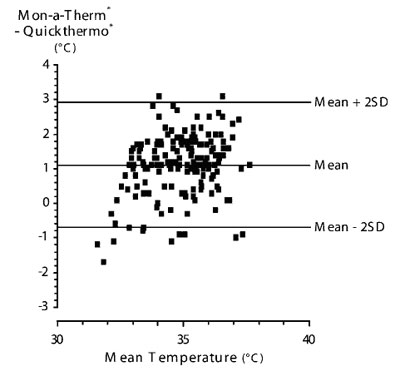 |
| Рис.1. Различия между температурой барабанной перепонки, измеренной при помощи термопары (Mon-a-therm, Сент-Луис, штат Миссури) и температурой в ушном канале, измеренной при помощи инфракрасного термометра Quickthermo (Mie. Япония). Средняя разница между значением центральной температуры и показаниями инфракрасного датчика составила 1,1°С. В этом исследовании также проверялась достоверность измерений, производимых тремя другими вариантами инфракрасных термометров; во всех случаях измерения оказались недостаточно точными для нужд клинической практики. Данные Immamura et al.15; публикуется с разрешения Wiley - Blackwell Publishing Ltd. средняя температура, среднее, среднее + 2 SD , среднее -2 SD ( SD - среднеквадратическое отклонение) |
Очень интересным методом измерения центральной температуры с поверхности кожи представляется использование системы, предложенной Fox et al .17,18 и усовершенствованной Togawa et al .19 Суть методики состоит в соединении нагревателя и термального потокового датчика (что фактически можно представить как два термометра, разделенные известным термоизолятором). Нагреватель при помощи сервопривода доводится до состояния, когда поток становится нулевым. В этот момент, тепло тепла и температура кожи должны быть равны по определению, иначе был бы поток тепла наружу. Сообразно этой же логике в этот момент отсутствует поток тепла и с поверхности кожи в более глубоко лежащие ткани; иначе тепло бы аккумулировалось, что противоречит второму закону термодинамики. На самом деле эта логика не совсем точна, так как игнорируются связанные с током крови поперечные потоки тепла. На практике такие термометры с достаточной точностью определяют температуру тканей, залегающих примерно на глубине 1 см от поверхности кожи. Во многих частях тела, в частности в области груди и лба, сантиметр является достаточной глубиной для измерения ориентировочной центральной температуры (рис.2). К несчастью, эти во всех остальных отношениях замечательные термометры пока не доступны ни Европе, ни в Соединенных Штатах.
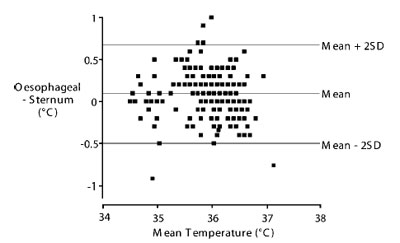 |
| Рис.2. Сравнение Bland и Altman температуры дистального отдела пищевода и «глубокой стернальной» темрературы. По вертикальной оси – разница между пищеводной и глубокой стернальной температурами. Средняя температура по горизонтальной оси соответствует среднему значению между пищеводной и глубокой стернальной температурами в каждый момент измерения. Среднее отклонение составило 0,1°С, среднеквадратическое отклонение – 0,3°С. Данные Matsukawa et al.20, публикуется с разрешения. средняя температура, среднее, среднее + 2 SD , среднее -2 SD ( SD - среднеквадратическое отклонение) |
Когда необходим мониторинг температуры?
Мониторинг центральной температуры рационален в процессе большинства общих анестезий, как для выявления злокачественной гипертермии, так и для количественной оценки гипертермии и гипотермии. Злокачественная гипертермия лучше всего выявляется по тахикардии и увеличению парциального давления углекислого газа в конечном выдыхаемом объеме, несоразмерному минутной вентиляции21. Хотя увеличение центральной температуры и не является первым признаком острой злокачественной гирертермии; тем не менее, это безусловно помогает подтвердить диагноз. Более распространенной, чем злокачественная гипертермия, является интраоперационная гипертермия другой этиологии, включая чрезмерное согревание, инфекционную лихорадку, попадание крови в IV мозговой желудочек и переливание несовместимой крови. Так как причины гипертермии очень серьезны, любая периоперационная гипертермия требует диагностического внимания,
Несомненно, наиболее известным видом нарушения температуры в периоперационном периоде является непредумышленная гипотермия (по «невнимательности (небрежности)»). Проспективные рандомизированные исследования показали, что даже незначительная гипотермия приводит к многочисленным неблагоприятным последствиям у различных групп пациентов. Среди осложнений, обусловленных гипотермией, необходимо отметить: патологические изменения миокарда22 за счет активации симпатической нервной системы23, инфекцию операционной раны24,25, коагулопатию6, 26-33, рост аллогенных трансфузий6,24,26,27,31,33-37, отрицательный азотный баланс38, медленное заживление раны24, замедленное восстановление после наркоза39, увеличение сроков госпитализации24, дрожь40 и субъективно ощущаемый дискомфорт пациента41.
Главной причиной развития гипотермии у большинства пациентов при проведении общей анестезии является внутреннее перераспределение тепла между центральными и периферическими отделами тела, что обычно приводит к снижению центральной температуры на 0,5-1,5°С в течение первых 30 минут от начала общей анестезии. Гипотермия развивается вследствие внутреннего перераспределения тепла и действия целого ряда других факторов, значимость которых у каждого конкретного пациента трудно предсказать9. При этом нарушения центральной температуры в первые 30 минут наркоза трудно интерпретировать, и ее измерение, как правило, не требуется. Однако, необходимо следить за температурой тела у большинства пациентов при длительности общей анестезии более 30 минут, и у всех пациентов при продолжительности операции более 1 часа. Измерение температуры тела (и поддержание нормотермии) сейчас фактически является стандартом при длительной общей анестезии, особенно при больших операциях, когда риск гипотермии реален.
Гипотермия, происходящая главным образом вследствие перераспределения тепла между центром и периферией, часто встречается и при эпидуральной и спинальной анестезии, и может быть не менее серьезной42. Так как при нейроаксиальной анестезии нарушаются поведенческие терморегуляторные реакции (а именно, чувство холода у пациента),43 и пациенты, и врачи зачастую не замечают развившуюся гипотермию (рис.3)42. Поэтому следует измерять центральную температуру во время регионарной анестезии у пациентов с высокой вероятностью развития гипотермии, включая тех, кому выполняются полостные операции, – хотя пока мониторинг температуры при нейроаксиальной анестезии как правило не проводится44,45.
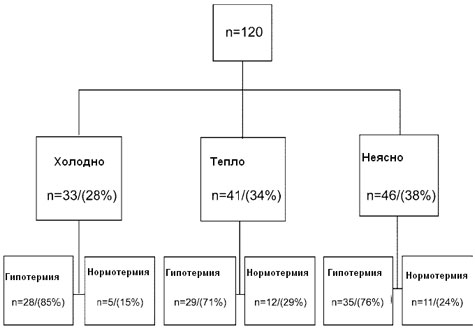 |
| Рис.3. Все пациенты были разделены на группы на основании «впечатления» анестезиолога об их термальном статусе. По «впечатлению» анестезиолога количество гипотермичных (<36°С)пациентов и пациентов с нормальной температурой (вероятность=0,36) было примерно равным. На самом деле такого рода оценка не является достоверной. Данные Arkilic et al.42, публикуется с разрешения. |
Где осуществлять мониторинг?
Центральный температурный «отсек» представлен тканями с высокой перфузией, в которых температура очень однородна и достаточно высока по сравнению с другими частями тела. Измерение центральной температуры можно произвести в легочной артерии, дистальном отделе пищевода, барабанной перепонке и носоглотке46,47. Даже во время быстрых нарушений температуры (например, сердечно-легочное шунтирование) эти участки тела остаются надежными зонами мониторинга температуры – хотя и могут возникать временные различия между ними.
Температурные датчики, встроенные в пищеводные стетоскопы, для достижения должной точности необходимо располагать в зонах наибольшей слышимости сердечных шумов, или даже еще более дистально48. Современные термопары для барабанной перепонки очень мягкие и податливые. Поэтому шансы перфорации перепонки если и есть, то минимальные, хотя возможно протолкнуть кусочек ушной серы к барабанной перепонке. Введение барабанных датчиков совсем не так элементарно, как кажется на первый взгляд, особенно у пациентов, находящихся в сознании; так как ушной канал непрямой и протяженный (длина его составляет несколько сантиметров). Сложность состоит в том, что тот, кто вводит датчик, может принять очередной изгиб ушного канала за барабанную перепонку, и, соответственно, расположить датчик в неправильном месте. Если датчик расположен правильно, полезно закрыть вход в ушной канал ватой для исключения охлаждения термопары потоками воздуха. Носоглоточные датчики для измерения центральной температуры нужно вводить как минимум на несколько сантиметров дальше, чем ноздри; показания носоглоточных датчиков, скорее всего, доказательны только у пациентов, у которых нет носового дыхания.
Центральную температуру можно с приемлемой точностью измерить и на основании значения температуры в ротовой полости, в подмышечной области и в мочевом пузыре; за исключением случаев чрезвычайных отклонений температуры46,47. Каждая из этих локализаций может быть подвержена помехам, поэтому клиницистам следует быть рациональным в выборе конкретного места измерения и типа термометра у каждого отдельного пациента. Например, температура ротовой полости может быть некорректной у пациентов, которые дышат через рот или недавно принимали внутрь горячие или холодные жидкости. Подмышечная температура в принципе может быть достаточно точна49, но предпочтительно, чтобы датчик был установлен точно над подмышечной артерией, а рука пациента прижата к боковой поверхности тела. Разница в технике измерения может объяснять разницу в точности50.
Температура поверхности кожи значительно ниже центральной температуры51; температура кожи лба, например, обычно на 2°С холоднее центральной. Это может показаться удивительным, но даже интенсивная вазодилятация при потоотделении и интенсивная вазоконстрикция при дрожи очень мало влияют на лобно-центральный градиент температуры (рис.4)52.
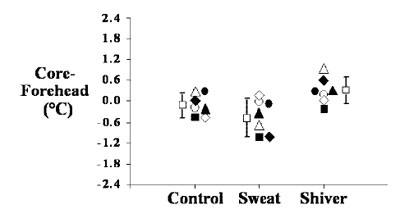 |
| Рис.4. Разница между температурой барабанной перепонки (=центральной) и температурой поверхности кожи лба в течение термонейтрального периода составила 0,1°С +-0,3°С. Эта разница осталась без существенных изменений при вазодилятации, связанной с потоотделением, и вазоконстрикции, связанной с дрожью. Результаты представлены в виде «среднее значение плюс-минус среднеквадратическое отклонение». Данные Ikeda et al.52; публикуется с разрешения. По горизонтальной оси слева направо: контрольная группа, потение дрожь. По вертикальной оси : центральная-лобная |
Температура кожи определяется соотношением между продукцией тепла, подкожными тканями и потерей тепла в окружающую среду. Отдача тепла с поверхности кожи, происходящая в основном за счет радиации и конвекции, зависит от температуры окружающей среды. Несмотря на то, что различные виды отдачи тепла кожей описываются при помощи разных уравнений, причем в большинстве случаев эти зависимости носят совсем нелинейный характер, в целом потеря тепла кожей в пределах незначительных колебаний температуры окружающей среды приблизительно может быть описана как линейный процесс. Колебания температуры окружающей среды в 1-2°С, с которыми обычно приходится иметь дело в операционной, таким образом, мало влияют на лобно-центральный градиент (рис.5)52. Следовательно, температура кожи лба может быть на удивление точным источником измерения центральной температуры с учетом поправки в +2°С.
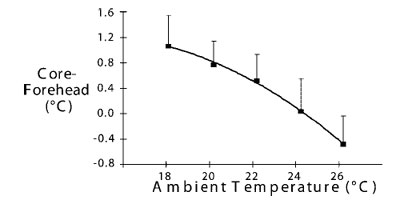 |
| Рис.5. Разница между температурой барабанной перепонки (центральной) и температурой поверхности кожи лба (?Т) при темпретуре окружающей среды (Tambient) от 18 до 26°С. Температура кожи увеличивалась с интервалом в 2°С. Полученные данные соответствовали регрессии второго порядка: ?Т = -0,58 + 0,29х(Tambient) - 0,01х(Tambient) 2 , r2=0,999. Таким образом, изменение температуры воздуха на 1°С, начиная с 22°С, приводило к изменению температуры кожи примерно на 0,16°С. Результаты представлены в виде «среднее значение плюс-минус среднеквадратическое отклонение». Горизонтальные строки ошибки (колебания температуры окружающей среды) не нанесены, так как величина колебаний была меньше, чем размеры разметки. Данные Ikeda et al.52, публикуется с разрешения. центральная-лобная, температура окружающей среды. |
Необычным вариантом контроля кожной температуры являются термометры для височных артерий. Это инфракрасные термометры для поверхности кожи, которые измеряют температуру с частотой приблизительно 10 Гц и определяют наивысшую температуру по мере сканирования кожи лба с захватом области височных артерий. Идея состоит в том, что температура крови в височных артериях это практически и есть центральная температура; и, поэтому, соответствующая температура кожи тоже приближается к центральной температуре. Хотя эта теория звучит очень привлекательно, эти устройства слишком неточны для клинической практики16,53.
Явным недостатком идеи измерения температуры кожи является ее неспособность достоверно подтверждать клинические признаки злокачественной гипертермии (тахикардию и гиперкапнию), что подтверждено при проведении исследования на свиньях (рис.6)54; исследования же такого рода на человеке не проводились. Ректальная температура обычно достаточно хорошо коррелирует с центральной46,47, но не возрастает ожидаемым образом при злокачественных гипертермических кризисах54 и при других документировано подтвержденных ситуациях, включая тепловой удар55,56. Следовательно, ректальная и кожная температуры должны использоваться со значительной осторожностью.
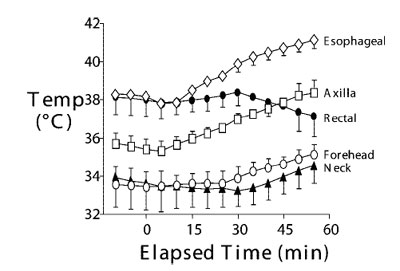 |
| Рис.6. При опытах по изучению злокачественной гипертермии у свиней аксиальная и пищеводная температуры коррелировали хорошо; между лобной и шейной температурами убедительной корреляции не было. Ректальная температура также оказалась ненадежной в своевременном определении начала злокачественной гипертермии. Нулевая отметка времени установлена на момент, когда парциальное давление кислорода в выдыхаемом воздухе составляло 70 мм рт.ст. Данные указывают, что температура кожи лба и шеи не может служить достоверным подтверждением других клинических признаков злокачественной гипертермии. Подходящими местами измерения центральной температуры являются: дистальный отдел пищевода, легочная артерия, носоглотка и барабанная перепонка. За исключением случаев легочно-сердечного шунтирования, приемлемыми местами измерения температуры тела также можно считать: полость рта, подмышечную область и мочевой пузырь. Результаты представлены в виде «среднее значение плюс-минус среднеквадратическое отклонение». Данные Iaizzo et al.54; публикуется с разрешения с изменениями. По горизонтальной оси: продолжительность, По вертикальной: температура, сверху вниз: пищеводная, подмышечная, ректальная, лобная, шейная |
Четыре области мониторирования центральной температуры (а именно барабанная перепонка, носоглотка, легочная артерия и пищевод) остаются информативными даже при сердечно-легочном шунтировании крови. В отличие от этого, ректальная температура запаздывает относительно температур измеренных в центральных зонах. Вследствие этого, ректальную температуру считают «промежуточной» температурой у пациентов с управляемой гипотермией. Температура мочевого пузыря во время операций на сердце может быть такой же, как ректальная (т.е. «промежуточной»), если темп диуреза низкий, а может быть равной температуре в легочной артерии (т.е. центральной), если темп диуреза высокий67. Адекватность согревания лучше всего оценивать как с учетом центральной, так и «промежуточной» температур.
Средняя температура кожи . Средняя температура кожи – это взвешенная по площади средняя температура поверхности кожи. Несмотря на то, что средняя температура кожи и не является столь же важным показателем, как центральная температура, она может быть ценной по крайней мере по трем причинам: (1) отдача тепла кожей зависит от средней температуры кожи и от температуры окружающей среды; (2) работа центрального механизма терморегуляции определяется совокупностью центральной и средней кожной температур; (3) совокупность центральной и средней кожной температур может быть использована для оценки СТТ и, соответственно, количества тепла в организме пациента.
Неудивительно, что точность измерения средней температуры кожи растет с увеличением количества участков измерения. Поэтому, при исследованиях терморегуляции стараются производить измерения в 15, или даже больше, участках. Так, более чем в 100 исследованиях использовались следующие участки и области регионарного «взвешивания»; голова – 6%, плечи – 9%, предплечья – 6%, руки – 2,5%, пальцы рук – 2%, спина – 19%, грудь – 9,5%, живот – 9,5%, медиальная сторона бедер – 6%, латеральная сторона бедер – 6%, задняя поверхность бедер – 7%, голени спереди – 7,5%, голени сзади – 4%, стопы – 4%, пальцы ног – 2% 58 . Столь значительное количество областей измерения обеспечивает высокую точность результата даже в условиях регионарных термальных манипуляций (активное согревание или охлаждение) и при различной термоизоляции в разных участках.
Когда действия, направленные на коррекцию температьуры (изоляция, согревание или охлаждение), в разной степени затрагивают разные участки тела, можно пользоваться упрощенными формулами без существенной потери точности. Формула с использованием всего четырех компонентов была предложена Ramanathan59 в 1964 году и используется до сих пор: средняя температура кожи (СТТ) = 0,3(грудь + плечи) + 0,2(бедро + голень).
Средняя температура тела . Изменения средней температуры тела в динамике по времени определяются путем интеграции разницы между метаболической продукцией тепла (потребление кислорода) и отдачей тепла кожей (измеряемой датчиками теплового потока). СТТ может быть также приблизительно определена как взвешенная по массе сумма регионального распределения температуры, что в свою очередь может быть определено путем интеграции радиального распределения температуры60. Однако, методика этого исследования инвазивна, а подсчеты трудоемки. Поэтому, ее использование ограничивается контролируемыми лабораторными исследованиями, выполняющимися при наличии соответствующего оборудования61.
В 1935 году, Burton62 очень находчиво предложил рассчитывать СТТ по формуле: СТТ = α x Т центр + (1-α) x Т кожи . Общий вид уравнения основан на идее о том, что все центральные участки относительно гомогенны, тогда как температура периферийных участков уменьшается по параболе по мере перехода от центральной температуры к температуре кожи. Численное значение специального коэффициента α, описывающего вклад центральной температуры в среднюю температуру тела, было в последствии выведено путем одновременного измерения количества тепла тела калориметром, центральной температуры и средней температуры кожи. Коэффициент ? получился равным 0,64, а формула приняла вид: СТТ=0,64 х Т центр + 0,36 х Т кожи.
Аналогичным подходом воспользовались и другие исследователи включая Hardy и Dubois63, предложивших коэффициент α равный 0,7 для нейтральной температуры окружающей среды; Stolwijk и Hardy64, предложившие коэффициент, равный 0,7 для высокой температуре окружающей среды и Snellen65, описавший коэффициент равный 0,8 для интенсивной мышечной работы при высокой температуре воздуха. Впоследствии, Colin et al.66 продемонстрировали в весьма изящном исследовании, что коэффициент, предложенный Burton , действительно «работает» при нейтральной температуре воздуха, а при чрезмерно высоких температурах воздуха должен быть увеличен до 0,79.
Принимая во внимание все данные о распределении тепла в теле, которые необходимо учесть для расчета СТТ на основе центральной и кожной температур, было бы удивительным предположить, что этот расчет можно произвести, воспользовавшись простой формулой. Но, тем не менее, это так. Даже во время сердечно-легочного шунтирования, формула Colin et al.66 позволяет оценивать СТТ достаточно хорошо (рис.7).
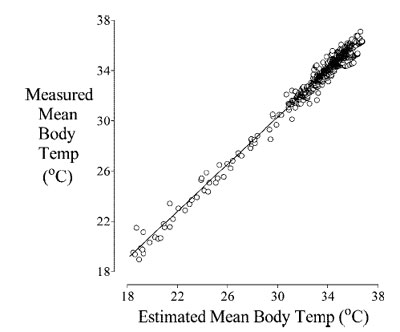 |
| Рис.7. Линейная регрессия, полученная при анализе 913 пар измерений, выполненных у 44 человек, участвовавших в 4 исследованиях теплового баланса. Средняя температура тела (СТТ) рассчитывалась из центральной температуры и средней температуры кожи и сравнивалась с цифрами, полученными путем опытного измерения. Выявлена убедительная связь между практически измеренной и рассчитанной СТТ: СТТ рассчитанная =0,94хСТТ измеренная +2,15, r2=0,98. Данные Lenhardt и Sessler12; публикуется с разрешения. По вертикальный оси – измеренная Т тела, по горизонтальной – ожидаемая средняя температура тела. |
Нормальная терморегуляция
Нормальная регуляция температуры тела
Температура тела в норме поддерживается достаточно жестко, гораздо жестче, чем частота сердечных сокращений сердца и величина артериального давления. Система контроля температуры достаточно сложная и состоит из двух параллельно работающих систем позитивной и негативной обратной связи, при работе которых задействованы в той или иной степени практически все отделы вегетативной нервной системы.
Уже в 1912 году физиологи выяснили, что главным звеном в терморегуляции у млекопитающих является гипоталамус, на основании данных о нарушении терморегуляции при травме или разрушении гипоталамуса. (У птиц за эту функцию отвечает спинной мозг). Замечательно, что потребовалось почти полвека для понимания важности значения тепловых сигналов, происходящих из кожи, в терморегуляции. Сейчас известно, что тепловая информация поступает в гипоталамус от различных органов и тканей; при этом на пути от периферии к центру эта информация частично обрабатывается67. Таким образом, терморегуляция основана на множественных повторяющихся сигналах, поступающих практически от всех тканей. Переработка терморегуляторной информации происходит в три этапа: центростремительная температурная чувствительность, центральная регуляция и центробежные ответные реакции.
Входящие сигналы. Практически все физиологические процессы в какой-то степени зависят от температуры; при нарушениях температуры заметно активируются или угнетаются специфические клетки. Предполагается, что эти клетки и есть температурные рецепторы, их называют тепло- и холодочувствительные клетки. Холодовые рецепторы активируются при охлаждении ткани, тепловые – при нагревании.
Кожные терморецепторы, вследствие их широкой доступности, изучены больше всего (подробнее см. монографию Henzel68). Человеческая кожа феноменально чувствительна к температуре: так, кожа лба способна уловить возрастание температуры на 0,003°С. У различных участков кожи температурная чувствительность и, что еще важнее, способность влиять на терморегуляторные ответные реакции неодинаковы. Кожа лица примерно в 5 раз чувствительнее кожи других областей. Более того, различия в чувствительности разных областей кожи до некоторой степени зависят от типа воздействия – тепло или холод. Кожа значительно более чувствительна к быстрым изменениям температуры, чем к тем, которые проистекают медленно.
Холодовые сигналы от кожи первично передаются через Аδ нервные волокна, тогда как тепловые проходят по безмиелиновым С-волокнам69. До недавнего времени было практически ничего неизвестно о том, как именно Аδ- и С-нервные волокна «чувствуют» температуру. Впрочем, теперь появилось мнение, что главными термочувствительными элементами и в коже, и в узлах задних корешков являются ваниллоидные(В) и ментоловые(М) рецепторы, действующие по механизму транзиторного рецепторного потенциала (ТРП). Это целая «семья» рецепторов, замечательных своей необыкновенно высокой температурной чувствительностью, их подробное описание появилось совсем недавно. Большинство изменяет свою активность больше, чем в 10 раз, в диапазоне изменения температуры в 10°С (Q10>10). ТРПВ1-4 рецепторы активируются теплом, тогда как ТРПМ8 и ТРПА1 рецепторы – холодом70,71.
Большинство восходящих температурных сигналов проходят по спиноталамическим трактам в передних столбах спинного мозга, тем не менее нельзя сказать, что существует отдельный выделенный канал для прохождения температурных импульсов. Недавно, например, был описан центростремительный соматосенсорный проводящий путь по латеральным парабрахиальным нейронам, передающий сигналы напрямую в предзрительный терморегуляторный центр72. Соответственно, для прекращения термогуляторных ответных реакций должен быть разрушен весь передний отдел спинного мозга. Гипоталамус, другие отделы головного мозга, спинной мозг, глубоколежащие ткани грудной и брюшной полостей и поверхность кожи ответственны каждый примерно за 20% входящих температурных импульсов к центральной регуляторной системе73,74. Таким образом, хотя гипоталамус и является главным и наиболее точным терморегулятором, его собственную температуру нельзя считать самой важной.
Центральный контроль . Простейшей моделью терморегуляции является схема «заданная величина», согласно которой все температурные ответные реакции включаются и выключаются синхронно с изменением температуры гипоталамуса. Эту модель нельзя считать адекватной, так как (1) на самом деле ответные реакции могут возникать при изменении температуры практически любой части тела, (2) ответные реакции не возникают синхронно или при аналогичных температурах, (3) в модели отсутствует понятие «нулевой зоны», в которой терморегуляторных реакций не возникает, (4) эта модель не в состоянии объяснить термоадаптацию и ряд других существующих явлений.
Общепринятая модель терморегуляции
Здесь мы изложим несколько более сложную, но значительно более полезную схему. Как и в других ситуациях, когда приходится прибегать к схемам, данную модель следует рассматривать лишь как своего рода каркас, позволяющий выработать подход к анализу терморегуляторных реакций; не следует воспринимать данную схему как подробный реальный механизм осуществления терморегуляторных реакций в теле человека. Согласно этой модели температурные сигналы от различных тканей человеческого организма интегрируются на различных уровнях (включая спинной мозг и ствол мозга); при этом наиболее центром координации является гипоталамус. Вклад отдельных импульсов координируется на основе взвешенного среднего.
Регуляция температуры центральными структурами происходит путем сравнения интегрированных температурных сигналов от поверхности кожи, нервной трубки (спинного мозга и ствола мозга) и глубоких тканей с пороговыми значениями (пусковыми, или триггерными центральными температурами) для каждой отдельной терморегуляторной реакции.
Центральные контролирующие действия имеют определенную структуру: интеграция входящих сигналов осуществляется на различных уровнях нервной трубки; у млекопитающих главная роль принадлежит гипоталамусу; при этом центр вегетативной регуляции расположен в переднем гипоталамусе; а центр поведенческой регуляции – в заднем гипоталамусе. Подобная иерархическая система, по-видимому, сформировалась в процессе эволюции системы терморегуляции путем ассимиляции ранее существовавших механизмов67. Так, например, мышцы, появившиеся в процессе эволюции для поддержания позы и передвижения, были приспособлены для дрожи; аналогично, терморегуляторную вазомоцию можно рассматривать как боковую ветвь развития системы контроля гемодинамики. Вероятно, некоторые терморегуляторные реакции осуществляются, не поднимаясь выше уровня спинного мозга74. Так, у пациентов и животных с высоким пересечением спинного мозга терморегуляция становится значительно хуже; но пойкилотермными их назвать нельзя.
Угол наклона графика, отражающего взаимосвязь интенсивности ответной реакции и центральной температуры, показывает прирост терморегуляторной реакции. Максимальной интенсивностью реакции называют такую, при которой дальнейшее изменение центральной температуры уже не вызывает увеличения интенсивности реакции.. На рис.8, например, показана зависимость возникновения потоотделения от температуры, измеренной в дистальном отделе пищевода, в процессе согревания поверхности тела.
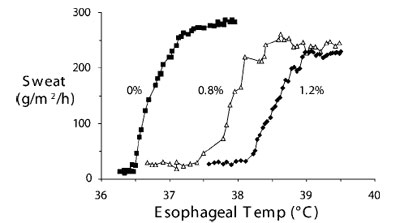 |
| Рис.8. Особенности потоотделения у «среднестатистических» мужчин добровольцев демонстрируют наличие порогового значения, прироста и максимальной интенсивности во время гипертермии без использования анестезии (концентрация изофлюрана в выдыхаемом воздухе - 0%), и на фоне анестезии при концентрации изофлюрана в выдыхаемом воздухе соответственно 0,8% и 1,2%. Пороговые значения существенно увеличивались при анестезии; а прирост и уровень максимального потоотделения были практически одинаковыми во всех группах. Данные Washington et al.75; публикуется с разрешения. По вертикальной оси: потоотделение (г/м2/ч), По горизонтальной оси: пищеводная температура |
Так, пока дистальная пищеводная температура не достигнет порогового значения – 36,5°С, происходит только базовая незаметная отдача воды кожей без анестезии. Потоотделение быстро растет при увеличении центральной температуры на 0,5°С (=прирост реакции), в дальнейшем, достигнув максимума, интенсивность потоотделения остается неизменной, несмотря на дальнейшее возрастание гипертермии (=максимальная интенсивность реакции). Хотя пороговое значение для возникновения прироста меняется в зависимости от концентрации изофлюрана, скорость прироста и максимальная интенсивность остаются схожими в процессе анестезии75.
Контроль вегетативных реакций приблизительно на 80% определяется импульсами, поступающими от центральных структур76,77; и остается практически неизменным во время анестезии (рис.9). Добрая половина импульсов, определяющих поведенческие реакции, напротив, происходит с поверхности кожи78.
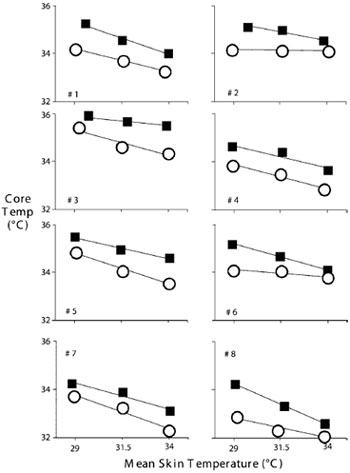 |
| Рис.9. Индивидуальная средняя температура кожи и центральная температура при пороге вазоконстрикции (обозначено квадратами) и пороге дрожи (обозначено кружками) у 8 добровольцев. Продемонстрирована линейная зависимость между средней кожной и центральной температурами при пороге вазоконстрикции и пороге дрожи у каждого исследуемого (линии): r2=0,98±0,02 для вазоконстрикции и 0,96±0,04 для дрожи .Относительный вклад кожной и центральной температур отличался от исследуемого у исследуемому, но в среднем вклад температуры кожи составил 21±8% в вазоконстрикцию и 18±10% в дрожь. Данные Lenhardt et al.89, публикуется с разрешения. По горизонтальной оси: средняя температура кожи, по вертикальной оси: центральная температура |
Очевидно, что человеческий организм в состоянии оценить величину собственной температуры тела с высокой точностью; тем не менее существует не конкретное значение, а некий межпороговый диапазон (набор температур), в пределах которого компенсаторные вегетатативные реакции не возникают. Диапазон температуры, которая организмом воспринимается как правильная центральная температура, определяется рядом обстоятельств (а именно, время суток, фаза менструального цикла). Нормальная центральная температура тела у людей находится в диапазоне от 36,5°С до 37,5°С; Значение центральной температуры меньше 36°С и больше 38°С, как правило, свидетельствует либо о нарушении терморегуляции, либо о чрезвычайно неблагоприятной температуре окружающей среды, при которой терморегуляционные защитные механизмы оказываются неэффективными.
Работа механизмов по поддержанию правильной схемы температуры усложняется параллельной активностью других реактивных механизмов (а именно, контроль сосудистого объема) а также факторами, зависящими от времени. В центре внимания физиологов остаются проблемы приспособления человека к выживанию к таких условиям окружающей среды, которые в норме должны запускать абсолютно противоположные механизмы компенсации. Например, тепловой удар, как правило, сопряжен с обезвоживанием в условиях очень горячей окружающей среды. Обезвоживание как таковое в принципе должно запускать механизмы, позволяющие удерживать жидкость, а гипертермия должна вызывать потоотделение. На самом деле тепловой удар обычно потому и развивается, что организм не может одновременно эффективно решить эти две задачи.
Большинство моделей терморегуляции (включая и описанную выше) недостаточно учитывают скорость изменения центральной и периферической температур. Поэтому эти модели должны применяться при динамичном развитии событий с особой осторожностью. Аналогично, существуют ситуации, когда терморегуляторные реакции определяются не только моментальными сигналами о текущей температуре, но и обусловлены предшествующими особенностями нарушений терморегуляции. Каково соотношение влияния на терморегуляторные реакции факторов, зависящих от температуры, и факторов, обусловленных временем, остается неясным.
Пороговые значения . Каким образом у человека определяются абсолютные пороговые значения температур, не вполне ясно; похоже, что при этом задействованы тормозящие постсинаптические потенциалы в гипоталамических нейронах79, работа которых регулируется адреналином, допамином, 5-гидрокситриптамином, ацетилхолином, простагландином Е и нейропептидами. Пороговые значения меняются в течение дня в диапазоне 0,5-1°С и у женщин, и у мужчин (циркадный ритм)80, и приблизительно в пределах 0,5°С у женщин в течение менструального цикла81. На величины пороговых значений также могут влиять физическая нагрузка, характер питания, наличие инфекции, гипо- и гипертиреоидизм, прием лекарственных препаратов (в том числе спирт, седативные препараты и никотин), а также холодовая и тепловая адаптация. Но влияние всех этих факторов очень мало по сравнению с глубокими нарушениями, вызываемыми общей анестезией.
Межпороговый диапазон (диапазон значений центральной температуры, при котором не запускаются регулирующие вегетативные реакции) ограничен порогом потоотделения сверху и порогом вазоконстрикции снизу. В пределах этого диапазона величина центральной температуры распознается правильно, но колебания температуры не запускают механизмы терморегуляции. С позиции целесообразности принесение в «жертву» небольшой доли терморегуляции выглядит весьма благоразумно: энергия и питательные вещества не тратятся активно для противодействия незначительным изменениям окружающей среды.
У человека внутрипороговый диапазон обычно составляет всего 0,2-0,4°С82, и это и есть диапазон нормальной температуры тела. По непонятным причинам температурный контроль в момент низшей точки циркадного ритма (примерно в 3 часа ночи) в два раза «свободнее», чем в другое время. (рис.10)80.
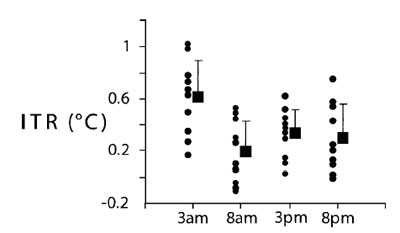 |
| Рис.10. Межипороговый диапазон (МПД - ITR ) от потоотделения до вазоконстрикции в разные моменты дня. Результаты представлены в виде «среднее значение плюс-минус среднеквадратическое отклонение». Пороговые значения в три часа ночи значительно отличаются от результатов, полученных в любое другое время суток. Данные Tayefeh et al.80 (стр.403, рис.2) публикуется с разрешения |
У некоторых животных (верблюды, пустынные крысы) межпороговой диапазон очень широкий; колебания центральной температуры в течение дня могут достигать 10°С; это связано с наличием системы консервации энергии и питательных веществ,которая позволяет поддерживать температуру в рамках межпорогового диапазона без активного участия вегетативной нервной системы и без испарения жидкости. Но это по большому счету исключение из правил; большинство млекопитающих весьма жестко контролируют свою центральную температуру.
Оба порога – и потоотделения, и вазоконстрикции, у женщин на 0,3-0,5°С выше, чем у мужчин, даже во время фолликулярной фазы менструального цикла (т.е. в его первые 10 дней)75. Разница еще более выражена во время лютеиновой фазы83. Центральный механизм терморегуляции вполне работоспособен даже у незначительно недоношенных детей84; но, по-видимому, не полностью сформирован у глубоко недоношенных детей (весом меньше килограмма). Пороговое значение для дрожи сохраняется даже у некоторых людей в возрасте почти 90 лет, хотя это происходит и не у всех; у лиц же младше 80 лет терморегуляция практически не меняется.85
Центробежные ответные реакции . Некоторые терморегуляторные реакции весьма редко, если вообще когда-либо, активируются чем-то, кроме изменений температуры. К таким реакциям относятся потоотделение и метаболизм бурого жира. В других случаях система терморегуляции ассимилирует исполнительные механизмы, эволюционно появившиеся для других целей: это дрожь (мышечная активность для поддержания позы и направленного движения) и сосудодвигательная реакция ( контроль давления крови и осмотического статуса). Приспособление ранее созданных механизмов для нужд терморегуляции вполне согласуется с иерархической моделью терморегуляции, предложенной Satinoff67, и отчасти объясняет, почему контроль терморегуляции столь широко расходуется.
Нарушения температуры (определяемые как отклонения температуры тела от специфического порогового значения) запускают исполнительные механизмы, которые фактически содействуют соответствующему увеличению отдачи тепла в окружающую среду или увеличению метаболической продукции тепла. У каждой ответной реакции есть свой собственный порог и свой диапазон «прироста». Система контроля при этом способна к активации реакций в определенном целесообразном порядке (т.е.вазоконстрикция предшествует дрожи, более энергозатратному механизму) и в той степени, которая реально необходима для поддержания центральной температуры.
Поведенческая регуляция . Поведенческая регуляция (преднамеренное воздействие на обмен тепла с окружающей средой) является наиболее мощным исполнительным терморегуляторным механизмом. Это то новшество, которое позволяет людям существовать и в самых холодных, и в самых жарких местах на Земле. У животных поведенческий механизм регуляции температуры тоже известен. Наиболее поразительна поведенческая регуляция у рептилий и амфибий. Эти животные, которых зачастую называют «холоднокровными», на самом деле очень здорово умеют регулировать свою температуру и даже способны к поведенческой «лихорадке»86. Если их поместить в среду, диапазон температуры которой совместим с их существованием, «холоднокровные» сумеют пристроиться так, чтобы поддерживать центральную температуру в пределах нескольких градусов от «нормальной». Любопытно, что оптимальной для большинства рептилий является температура приблизительно такая же, как и у млекопитающих, около 37°С. Аналогичным образом поступают рыбы87. Один исследователь даже смог «надрессировать» свою золотую рыбку поддерживать нужную температуру воды (а, следовательно, и своего тела) путем нажатия кнопки88. Даже бактерии при предоставлении такой возможности будут стремиться расположиться там, где есть возможность поддерживать оптимальную температуру.
Активное поведенческое изменение отдачи тепла в окружающую среду как правило не требуется, если температура окружающей среды приемлема. В этом заключается эволюционное достижение - поддержания практически постоянной центральной температуры (вероятно необходимой для оптимального функционирования ферментов) без использования поведенческих реакций, которые могут угрожать выживанию. Тем не менее, если вегетативных реакций терморегуляции оказывается недостаточно для поддержания центральной температуры, принципиальными для выживания становятся поведенческие механизмы. Поведенческое приспособление очень разнообразно; из наиболее распространенных вариантов можно отметить столь простые действия как уход с прямого солнца в тень, выбор одежды по погоде, использование кондиционеров и отопления. Поведенческие реакции требуют сознательного ощущения температуры тела. Интересно, что человек плохо ощущает изменения центральной температуры; и напротив, очень чутко чувствует даже минутные колебания температуры поверхности кожи. Таким образом, поведенческая терморегуляция приблизительно наполовину обусловлена температурой кожи78, тогда как в работе вегетативных терморегуляторных механизмов доля информации, поставляемая кожей, составляет всего лишь 10-20%76,89.
Сосудо-двигательные реакции . Отдача метаболического тепла преимущественно производится через поверхность кожи, и сужение сосудов кожи, наиболее часто используемый исполнительный механизм вегетативной терморегуляции, уменьшает потерю тепла. В суммарном кожном токе крови можно выделить питающую (в основном капилляры) и терморегуляторную (в основном артериовенозные шунты) составляющие90. Шунты обычно имеют диаметр 100 μm; это означает, что один шунт может передать в 10000 раз больше крови, чем соответствующей длины капилляр 10 μm в диаметре. Артериовенозные шунты могут быть открытыми и закрытыми, что собственно означает большой возможный диапазон «прироста» при использовании данного механизма терморегуляции. Порядка 10% сердечного выброса проходит через артериовенозные шунты; соответственно, «закрытие» шунтов увеличивает артериальное давление приблизительно на 15 мм рт ст91.
Артериовенозные шунты располагаются только в дистальных отделах (пальцы рук, пальца ног, нос и т.д.) Эти специализированные терморегуляторные сосуды являются α-адренергическими; их сужение происходит под действием норадреналина, выделяющегося симпатическими нервными окончаниями. Похоже, что циркулирующие в крови вещества не оказывают прямого влияния на артериовенозные шунты, хотя гормоны (такие как ангиотензин) могут способствовать ответу на полученный симпатический стимул. Большинство сосудов при локальной гипотермии сужаются, но артериоввенозные шунты относительно устойчивы к местным температурным изменениям и, скорей всего, контролируются исключительно центральным терморегуляторным статусом. При термонейтральной окружающей среде (т.е.температура воздуха соответствует температуре тела в пределах межпорогового диапазона) и в денервированной конечности артериовенозные шунты полностью открыты. Впрочем, при обычной температуре окружающей среды тонизирующая симпатическая симуляция поддерживает кровоток в шунтах на минимальном уровне.
« Несократительный» термогенез . Под несократительным термогенезом понимают увеличение метаболической продукции тепла, несвязанное с работой мышц. Такое увеличение преимущественно происходит в специализированной жировой ткани - буром жире, располагающемся в основном между лопатками и около почек. Бурый жир имеет коричневый оттенок за счет чрезвычайно высокого содержания митохондрий. При стимуляции бурый жир обладаем самой высокой метаболической активностью в человеческом организме (до 0,5 Вт/г). Обычно, митохондриальный метаболизм приводит к образованию протона, который секретируется за пределы саркоплазматической сети. Протонный трансмембранный градиент в свою очередь активирует калий-натриевую АТФ-азу, приводя к образованию АТФ из АДФ. При высвобождении норадреналина из симпатических нервных окончаний митохондриальное дыхание в бурой аденозин- трифосфатазной ткани происходит обычным образом. При этом продукции АТФ препятствует специальный «расщепляющий белок», который позволяет протонам вернуться в саркоплазматическую сеть без использования калий-натриевой АТФазы92.
Несократительный термогенез является основным механизмом защиты от холода у мелких млекопитающих (мыши, крысы); он может с легкостью приводить к удвоению, а то и утроению метаболической продукции тепла (оцениваемой по потреблению организмом кислорода) без выполнения какой-либо механической работы. Недрожательный термогенез может удваивать продукцию тепла и у младенцев93. Интенсивность недрожательного термогенеза является линейной функцией от разницы между величиной средней температурой тела (СТТ) и ее пороговым значением.
Несократительный термогенез имеет важное значение только у маленьких животных и у младенцев; при относительно крупных размерах биологического организма (>50кг) этот механизм или не имеет реального практического значения, или не работает вообще. У взрослых людей такой термогенез слабо развит и мало участвует в поддержании температуры тела
Дрожь . Длительная дрожь увеличивает метаболическую продукцию тепла у взрослых на 50-100%. Это увеличение очень мало в сравнении с увеличением, происходящим вследствие физической нагрузки (при физической нагрузке увеличение продукции тепла может быть пятикратным, по крайней мере, кратковременно), и поэтому является на удивление малоэффективным. Дрожь это беспорядочное сотрясение, которое выглядит на электромиограмме как случайные накладывающиеся зубцы деполяризации миофибрилл. На эти быстрые и явно хаотические всплески местной активности накладываются более структурированные волнообразные циклы изменения активности (4-10 колебаний в минуту). Причем, эти медленные волновые изменения активности происходят синхронно во всех мышцах тела95. Дрожание не встречается у новорожденных младенцев и скорей всего недостаточно эффективно у детей первых лет жизни. Так как температурный порог дрожи на целый градус меньше порога вазоконстрикции82, похоже, что это «последняя надежда» среди способов борьбы с переохлаждением.
Потоотделение . Потоотделение контролируется постганглионарными холинергическими нервными волокнами. Это активный процесс, который может быть выключен посредством нервной блокады или введением атропина97. Даже у нетренированных людей потоотделение может достигать до 1 л/ч, а спортсмены могут «потеть» в два раза интенсивнее. Потоотделение является единственным механизмом отдачи тепла, работающим при температуре окружающей среды большей, чем центральная температура тела. К счастью, этот механизм работает очень эффективно: Вместе с одним граммом пота «уходит» 0,58 ккал. Если окружающий человека воздух сухой и есть конвекция, величина теплоотдачи путем потоотделения может во много раз превышать значение базального метаболизма, который в грубом приближении составляет ккал/кгхчас. Конечно, пот, который образуется скапливается на коже в виде капелек и не испаряется, никак не способствует тепловому балансу и лишь содействует обезвоживанию.
При физической нагрузке мышечный кровоток резко увеличивается, и давление крови можно поддержать только за счет вазоконстрикции в других сосудистых сетях. Более того, при физической нагрузке образуется столько тепла, что для его эффективной отдачи практически при любой погоде требуется усиление капиллярного кровотока и потоотделения (1 л/ч или даже больше). При этом механизмы терморегуляции вступают в «борьбу» с потребностью мышц в увеличении кровотока. Так что неудивительно, что максимальный капиллярный кровоток и интенсивность потоотделения могут повреждаться при снижении ОЦК и сердечно-сосудистой недостаточности. Учитывая серьезное стрессовое действие физической нагрузки на сердечно-сосудистую систему и терморегуляторную компенсацию возникающего при этом увеличения метаболической продукции тепла, поразительно, как вообще удается человеку вести себя энергично при высокой температуре окружающей среды и сохранять приемлемый уровень артериального давления.
В противоположность кровотоку в шунтах, капиллярный кровоток минимален и при обычных температуре окружающей среды, и при термонейтральном окружении. При тепловом стрессе активная дилятация прекапиллярных артериол приводит к резкому возрастанию капиллярного кровотока. Эта дилятация безусловно связана с прекращением симпатической стимуляции, но, похоже, что в возникновении дилятации какую-то роль играет и какое-то химическое вещество, продуцируемое потовыми железами; что это за вещество, еще предстоит определиться, возможно, это окись азота или нейропептид Y98. Так как активная вазодилатация требует сохранной функции потовых желез, она также значительно угнетается при нарушении нервной передачи. При серьезном тепловом стрессе кровоток в поверхностном слое кожи толщиной 1 мм может достигать 7,5 л/мин – то есть столько же, сколько составляет весь сердечный выброс в покое99. Пороговое значение для активной вазодилатации аналогично пороговому значению потоотделения, но обычно максимальная кожная вазодилатация запаздывает и наступает после достижения максимальной активности потоотделения.
Стратегия активации ответных реакций . В идеальном варианте все потенциальные терморегуляторные реакции доступны и используются в определенном порядке в зависимости от порогового значения и диапазона ответных приростов. Однако при определенных обстоятельствах один или несколько ответных механизмов могут оказаться недейственными. Например, социальные обычаи могут ограничивать свободу произвольного передвижения или возможность искать более теплое или прохладное место. Наличие в организме миорелаксанта может препятствовать дрожи, а вазодилататора – ваконстрикции. В таких ситуациях механизмы, оставшиеся рабочими, пытаются справиться с ситуацией своими силами и компенсировать недостающие механизмы в пределах своих возможностей. Как правило, при этом центральную температуру удается удержать, но сокращаются границы возможности приспособления к состоянию окружающей среды.
Список литературы
- Sessler DI: Perioperative heat balance. ANESTHESIOLOGY 2000; 92:578–96
- Sessler DI: Complications and treatment of mild hypothermia. ANESTHESIOLOGY2001; 95:531–43
- De Witte J, Sessler DI: Perioperative shivering: Physiology and pharmacology. ANESTHESIOLOGY 2002; 96:467–84
- Heier T, Caldwell JE: Impact of hypothermia on the response to neuromuscularblocking drugs. ANESTHESIOLOGY 2006; 104:1070–80
- Mayer SA, Sessler DI: Therapeutic Hypothermia. New York , Marcel Dekker, 2004
- Winkler M, Akc.a O, Birkenberg B, Hetz H, Scheck T, Arkilic CF, Kabon B, Marker E, Grubl A, Czepan R, Greher M, Goll V, Gottsauner-Wolf F, Kurz A, Sessler DI: Aggressive warming reduces blood loss during hip arthroplasty.Anesth Analg 2000; 91:978–84
- Rubinstein EH, Sessler DI: Skin-surface temperature gradients correlate with fingertip blood flow in humans. ANESTHESIOLOGY 1990; 73:541–5
- Matsukawa T, Sessler DI, Christensen R, Ozaki M, Schroeder M: Heat flowand distribution during epidural anesthesia. ANESTHESIOLOGY 1995; 83:961–7
- Matsukawa T, Sessler DI, Sessler AM, Schroeder M, Ozaki M, Kurz A, Cheng C: Heat flow and distribution during induction of general anesthesia. ANESTHESIOLOGY 1995; 82:662–73
- Kurz A, Sessler DI, Christensen R, Dechert M: Heat balance and distribution during the core-temperature plateau in anesthetized humans. ANESTHESIOLOGY 1995; 83:491–9
- Wadhwa A, Sengupta P, Durrani J, Akca O, Lenhardt R, Sessler DI, Doufas AG: Magnesium sulphate only slightly reduces the shivering threshold in humans. Br J Anaesth 2005; 94:756–62
- Lenhardt R, Sessler DI: Estimation of mean body temperature from mean skin and core temperature. ANESTHESIOLOGY 2006; 105:1117–21
- Lopez M, Ozaki M, Sessler DI, Valdes M: Mild core hyperthermia does not alter electroencephalographic responses during epidural/enflurane anesthesia in humans. J Clin Anesth 1993; 5:425–30
- Matsukawa T, Kashimoto S, Miyaji T, Hanagata K, Iriki M, Kumazawa T: A new infrared tympanic thermometer in surgery and anesthesia. J Anesth 1993; 7:33–9
- Imamura M, Matsukawa T, Ozaki M, Sessler DI, Nishiyama T, Kumazawa T: The accuracy and precision of four infrared aural canal thermometers during cardiac surgery. Acta Anaesthesiol Scand 1998; 42:1222–6
- Suleman MI, Doufas AG, Akc.a O, Ducharme M, Sessler DI: Insufficiency in a new temporal-artery thermometer for adult and pediatric patients. Anesth Analg 2002; 95:67–71
- Fox RH, Solman AJ: A new technique for monitoring the deep body temperature in man from the intact skin surface. J Physiol 1970; 212:8–10
- Fox RH, Solman AJ, Isaacs R, Fry AJ, MacDonald IC: A new method for monitoring deep body temperature from the skin surface. Clin Sci 1973; 44:81–6
- Togawa T, Nemoto T, Yamazaki T, Kobayashi T: A modified internal temperature measurement device. Med Biol Eng 1976; 14:361–4
- Matsukawa T, Sessler DI, Ozaki M, Kumazawa T: Comparison of distal oesophageal temperature with “deep” and tracheal temperatures. Can J Anaesth 1997; 44:433–8
- Baudendistel L, Goudsouzian N, Cote. C, Strafford M: End-tidal CO2 monitoring: Its use in the diagnosis and management of malignant hyperthermia. Anaesthesia 1984; 39:1000–3
- Frank SM, Fleisher LA, Breslow MJ, Higgins MS, Olson KF, Kelly S, Beattie C: Perioperative maintenance of normothermia reduces the incidence of morbid cardiac events: A randomized clinical trial. JAMA 1997; 277:1127–34
- Frank SM, Higgins MS, Fleisher LA, Sitzmann JV, Raff H, Breslow MJ: Adrenergic, respiratory, and cardiovascular effects of core cooling in humans.Am J Physiol 1997; 272:R557–62
- Kurz A, Sessler DI, Lenhardt RA: Study of wound infections and temperature group: Perioperative normothermia to reduce the incidence of surgicalwound infection and shorten hospitalization. N Engl J Med 1996; 334:1209–15
- Melling AC, Ali B, Scott EM, Leaper DJ: Effects of preoperative warming on the incidence of wound infection after clean surgery: A randomised controlledtrial. Lancet 2001; 358:876–80
- Schmied H, Kurz A, Sessler DI, Kozek S, Reiter A: Mild intraoperativehypothermia increases blood loss and allogeneic transfusion requirements during total hip arthroplasty. Lancet 1996; 347:289–92
- Widman J, Hammarqvist F, Sellden E: Amino acid infusion induces thermogenesis and reduces blood loss during hip arthroplasty under spinal anesthesia. Anesth Analg 2002; 95:1757–62
- Sellden E: Peri-operative amino acid administration and the metabolic response to surgery. Proc Nutr Soc 2002; 61:337–43
- Nesher N, Zisman E, Wolf T, Sharony R, Bolotin G, David M, Uretzky G, Pizov R: Strict thermoregulation attenuates myocardial injury during coronary artery bypass graft surgery as reflected by reduced levels of cardiac-specifictroponin I. Anesth Analg 2003; 96:328–35
- Vassiliades T Jr, Nielsen J, Lonquist J: Evaluation of a new temperature management system during off-pump coronary artery bypass. Interactive Cardiovasc Thorac Surg 2003; 141:1–5
- Hofer CK, Worn M, Tavakoli R, Sander L, Maloigne M, Klaghofer R, Zollinger A: Influence of body core temperature on blood loss and transfusion requirements during off-pump coronary artery bypass grafting: A comparison of3 warming systems. J Thorac Cardiovasc Surg 2005; 129:838–43
- Persson K, Lundberg J: Perioperative hypothermia and postoperative opioid requirements. Eur J Anaesthesiol 2001; 18:679–86
- Johansson T, Lisander B, Ivarsson I: Mild hypothermia does not increase blood loss during total hip arthroplasty. Acta Anaesthesiol Scand 1999; 43: 1005–10
- Bock M, Muller J, Bach A, Bohrer H, Martin E, Motsch J: Effects of preinduction and intraoperative warming during major laparotomy. Br J Anaesth 1998; 80:159–63
- Hohn L, Schweizer A, Kalangos A, Morel DR, Bednarkiewicz M, Licker M: Benefits of intraoperative skin surface warming in cardiac surgical patients. Br JAnaesth 1998; 80:318–23
- Nathan HJ, Polis T: The management of temperature during hypothermic cardiopulmonary bypass, II: Effect of prolonged hypothermia. Can J Anaesth 1995; 42:672–6
- Smith CE, Desai R, Glorioso V, Cooper A, Pinchak AC, Hagen KF: Preventing hypothermia: Convective and intravenous fluid warming versus convective warming alone. J Clin Anesth 1998; 10:380–5
- Carli F, Emery PW, Freemantle CAJ: Effect of peroperative normothermia on postoperative protein metabolism in elderly patients undergoing hip arthroplasty. Br J Anaesth 1989; 63:276–82
- Lenhardt R, Marker E, Goll V, Tschernich H, Kurz A, Sessler DI, Narzt E, Lackner F: Mild intraoperative hypothermia prolongs postanesthetic recovery. ANESTHESIOLOGY 1997; 87:1318–23
- Just B, Delva E, Camus Y, Lienhart A: Oxygen uptake during recovery following naloxone. ANESTHESIOLOGY 1992; 76:60–4
- Sessler DI, Rubinstein EH, Moayeri A: Physiological responses to mild perianesthetic hypothermia in humans. ANESTHESIOLOGY 1991; 75:594–610
- Arkilic CF, Akc.a O, Taguchi A, Sessler DI, Kurz A: Temperature monitoring and management during neuraxial anesthesia: An observational study. Anesth Analg 2000; 91:662–6
- Sessler DI, Ponte J: Shivering during epidural anesthesia. ANESTHESIOLOGY 1990; 72:816–21
- Frank SM, Nguyen JM, Garcia C, Barnes RA: Temperature monitoring practices during regional anesthesia. Anesth Analg 1999; 88:373–7
- Torossian A: Survey on intraoperative temperature management in Europe . Eur J Anaesthesiol 2007; 24:668–75
- Bissonnette B, Sessler DI, LaFlamme P: Intraoperative temperature monitoring sites in infants and children and the effect of inspired gas warming on esophageal temperature. Anesth Analg 1989; 69:192–6
- Cork RC, Vaughan RW, Humphrey LS: Precision and accuracy of intraoperative temperature monitoring. Anesth Analg 1983; 62:211–4
- Kaufman RD : Relationship between esophageal temperature gradient and heart and lung sounds heard by esophageal stethoscope. Anesth Analg 1987; 66:1046–8
- Lodha R, Mukerji N, Sinha N, Pandey RM, Jain Y: Is axillary temperature an appropriate surrogate for core temperature? Indian J Pediatr 2000; 67:571–4
- Ogren JM: The inaccuracy of axillary temperatures measured with an electronic thermometer. Am J Dis Child 1990; 144:109–11
- Burgess GE III, Cooper JR, Marino RJ, Peuler MJ: Continuous monitoring of skin temperature using a liquid-crystal thermometer during anesthesia. South Med J 1978; 71:516–8
- Ikeda T, Sessler DI, Marder D, Xiong J: The influence of thermoregulatory vasomotion and ambient temperature variation on the accuracy of core-temperature estimates by cutaneous liquid-crystal thermometers. ANESTHESIOLOGY 1997; 86:603–12
- Greenes DS, Fleisher GR: Accuracy of a noninvasive temporal artery thermometer for use in infants. Arch Pediatr Adolesc Med 2001; 155:376–81
- Iaizzo PA, Kehler CH, Zink RS, Belani KG, Sessler DI: Thermal response in acute porcine malignant hyperthermia. Anesth Analg 1996; 82:803–9
- Ash CJ, Cook JR, McMurry TA, Auner CR: The use of rectal temperature to monitor heat stroke. MO Med 1992; 89:283–8
- Buck SH, Zaritsky AL: Occult core hyperthermia complicating cardiogenic shock. Pediatrics 1989; 83:782–4
- Horrow JC, Rosenberg H: Does urinary catheter temperature reflect core temperature during cardiac surgery? ANESTHESIOLOGY 1988; 69:986–9
- Sessler DI, Schroeder M: Heat loss in humans covered with cotton hospital blankets. Anesth Analg 1993; 77:73–7
- Ramanathan NL: A new weighting system for mean surface temperature of the human body. J Appl Physiol 1964; 19:531–3
- Belani K, Sessler DI, Sessler AM, Schroeder M, McGuire J, Washington D, Moayeri A: Leg heat content continues to decrease during the core temperature plateau in humans. ANESTHESIOLOGY 1993; 78:856–63
- Taguchi A, Ratnaraj J, Kabon B, Sharma N, Lenhardt R, Sessler DI, Kurz A: Effects of a circulating-water garment and forced-air warming on body heat content and core temperature. ANESTHESIOLOGY 2004; 100:1058–64
- Burton AC: Human calorimetry: The average temperature of the tissues of the body. J Nutr 1935; 9:261–80
- Hardy JD, DuBois EF: Basal metabolism, radiation, convection, and evaporation at temperatures from 22° to 35°C . J Nutr 1938; 15:477–92
- Stolwijk JAJ, Hardy JD: Partitional calorimetric studies of responses of man to thermal transients. J Appl Physiol 1966; 21:967–77
- Snellen JW: Mean body temperature and the control of sweating. Acta Physiol Neerl 1966; 14:99–174
- Colin J, Timbal J, Houdas Y, Boutelier C, Guieu JD: Computation of mean body temperature from rectal and skin temperatures. J Appl Physiol 1971; 31:484–9
- Satinoff E: Neural organization and evolution of thermal regulation in mammals: Several hierarchically arranged integrating systems may have evolved to achieve precise thermoregulation. Science 1978; 201:16–22
- Hensel H: Thermoreception and Temperature Regulation. London , Academic Press, 1981
- Poulos DA: Central processing of cutaneous temperature information. FedProc 1981; 40:2825–9
- Brauchi S, Orta G, Salazar M, Rosenmann E, Latorre R: A hot-sensing cold receptor: C-terminal domain determines thermosensation in transient receptor potential channels. J Neurosci 2006; 26:4835–40
- Moqrich A, Hwang SW, Earley TJ, Petrus MJ, Murray AN, Spencer KS, Andahazy M, Story GM, Patapoutian A: Impaired thermosensation in mice lacking TRPV3, a heat and camphor sensor in the skin. Science 2005; 307:1468–72
- Nakamura K, Morrison SF: A thermosensory pathway that controls body temperature. Nat Neurosci 2008; 11:62–71
- Jessen C, Feistkorn G: Some characteristics of core temperature signals in the conscious goat. Am J Physiol 1984; 247:R456–64
- Simon E: Temperature regulation: The spinal cord as a site of extrahypothalamic thermoregulatory functions. Rev Physiol Biochem Pharmacol 1974;71:1–76
- Washington D, Sessler DI, Moayeri A, Merrifield B, Prager M, McGuire J, Belani K, Hudson S, Schroeder M: Thermoregulatory responses to hyperthermiaduring isoflurane anesthesia in humans. J Appl Physiol 1993; 74:82–7
- Cheng C, Matsukawa T, Sessler DI, Kurz A, Merrifield B, Lin H, Olofsson P: Increasing mean skin temperature linearly reduces the core-temperature thresholds for vasoconstriction and shivering in humans. ANESTHESIOLOGY 1995; 82:1160–8
- Wyss CR, Brengelmann GL, Johnson JM, Rowell LB, Silverstein D: Altered control of skin blood flow at high skin and core temperatures. J Appl Physiol 1975; 38:839–45
- Frank S, Raja SN, Bulcao C, Goldstein D: Relative contribution of core and cutaneous temperatures to thermal comfort, autonomic, and metabolic responsesin humans. J Appl Physiol 1999; 86:1588–93
- Curras MC, Kelso SR, Boulant JA: Intracellular analysis of inherent and synaptic activity in hypothalamic thermosensitive neurones in the rat. J Physiol 1991; 440:257–71
- Tayefeh F, Plattner O, Sessler DI, Ikeda T, Marder D: Circadian changes in the sweating-to-vasoconstriction interthreshold range. Pflugers Arch 1998; 435:402–6
- Lee KA: Circadian temperature rhythms in relation to menstrual cycle phase. J Biol Rhythms 1988; 3:255–63
- Lopez M, Sessler DI, Walter K, Emerick T, Ozaki M: Rate and gender dependence of the sweating, vasoconstriction, and shivering thresholds in humans. ANESTHESIOLOGY 1994; 80:780–8
- Hessemer V, Bru.ck K: Influence of menstrual cycle on thermoregulatory, metabolic, and heart rate responses to exercise at night. J Appl Physiol 1985; 59:1911–7
- Mestyan J, Jarai I, Bata G, Fekete M: The significance of facial skin temperature in the chemical heat regulation of premature infants. Biol Neonate 1964; 7:243–54
- Vassilieff N, Rosencher N, Sessler DI, Conseiller C: The shivering threshold during spinal anesthesia is reduced in the elderly. ANESTHESIOLOGY 1995; 83: 1162–6
- Bernheim HA, Kluger MJ: Fever and antipyresis in the lizard Dipsosaurus dorsalis. Am J Physiol 1976; 231:198–203
- Rausch RN, Crawshaw LI, Wallace HL: Effects of hypoxia, anoxia, and endogenous ethanol on thermoregulation in goldfish, Carassius auratus. Am J Physiol Regul Integr Comp Physiol 2000; 278:R545–55
- Rozin PN, Mayer J: Thermal reinforcement and thermoregulatory behavior in the goldfish, Carassius auratus. Science 1961; 134:942–3
- Lenhardt R, Greif R, Sessler DI, Laciny S, Rajek A, Bastanmehr H: Relative contribution of skin and core temperatures to vasoconstriction and shivering thresholds during isoflurane anesthesia. ANESTHESIOLOGY 1999; 91:422–9
- Hales JRS: Skin arteriovenous anastomoses: Their control and role in thermoregulation, Cardiovascular Shunts: Phylogenetic, Ontogenetic and Clinical Aspects. Edited by Johansen K, Burggren W. Copenhagen, Munksgaard, 1985, pp 433–51
- Greif R, Laciny S, Rajek A, Doufas AG, Sessler DI: Blood pressure response to thermoregulatory vasoconstriction during isoflurane and desflurane anesthesia. Acta Anaesthesiol Scand 2003; 47:847–52
- Nedergaard J, Cannon B: The uncoupling protein thermogenin and mitochondrial thermogenesis. New Comp Biochem 1992; 23:385–420
- Dawkins MJR, Scopes JW: Non-shivering thermogenesis and brown adipose tissue in the human new-born infant. Nature 1965; 206:201–2
- Jessen K: An assessment of human regulatory nonshivering thermogenesis. Acta Anaesthesiol Scand 1980; 24:138–43
- Israel DJ, Pozos RS: Synchronized slow-amplitude modulations in the electromyograms of shivering muscles. J Appl Physiol 1989; 66:2358–63
- Hemingway A, Price WM: The autonomic nervous system and regulation of body temperature. ANESTHESIOLOGY 1968; 29:693–701
- Boudet J, Qing W, Boyer-Chammard A, Del Franco G, Bergougnan JL, Rosen P, Meyer P: Dose-response effects of atropine in human volunteers. Fund Clin Pharmacol 1991; 5:635–40
- Kellogg DL Jr: In vivo mechanisms of cutaneous vasodilation and vasoconstriction in humans during thermoregulatory challenges. J Appl Physiol 2006; 100:1709–18
- Detry J-MR, Brengelmann GL, Rowell LB, Wyss C: Skin and muscle components of forearm blood flow in directly heated resting man. J Appl Physiol 1972; 32:506–11
- Greif R, Laciny S, Rajek AM, Larson MD, Bjorksten AR, Doufas AG, Bakhshandeh M, Mokhtarani M, Sessler DI: Neither nalbuphine nor atropine posses special antishivering activity. Anesth Analg 2001; 93:620–7
- Gronert GA, Theye RA, Milde JH, Tinker JH: Catecholamine stimulation of myocardial oxygen consumption in porcine malignant hyperthermia. ANESTHESIOLOGY 1978; 49:330–7
- Davatelis G, Wolpe SD, Sherry B, Dayer JM, Chicheportiche R, Cerami A: Macrophage inflammatory protein-1: A prostaglandin-independent endogenous pyrogen. Science 1989; 243:1066–8
- Fabricio AS, Rae GA, D'Orleans-Juste P, Souza GE: Endothelin-1 as a central mediator of LPS-induced fever in rats. Brain Res 2005; 1066:92–100
- Blatteis C, Sehic E: Fever: How may circulating pyrogens signal the brain? News Physiol Sci 1997; 12:1–9
- Alheim K, Bartfai T: The interleukin-1 system: Receptors, ligands, and ICE in the brain and their involvement in the fever response. Ann N Y Acad Sci 1998; 840:51–8
- Chu EK , Ribeiro SP, Slutsky AS : Heat stress increases survival rates in lipopolysaccharide-stimulated rats. Crit Care Med 1997; 25:1727–32
- Negishi C, Lenhardt R, Sessler DI, De Witte J, Ikeda T, Kurz A, Lobo E: Desflurane reduces the febrile response to administration of interleukin-2. ANESTHESIOLOGY 1998; 88:1162–9
- Negishi C, Kim J-S, Lenhardt R, Sessler DI, Ozaki M, Vuong K, Bastanmehr H, Bjorksten AR : Alfentanil reduces the febrile response to interleukin- 2 in humans. Crit Care Med 2000; 28:1295–300
- Kurz A, Go JC, Sessler DI, Kaer K, Larson M, Bjorksten AR : Alfentanil slightly increases the sweating threshold and markedly reduces the vasoconstriction and shivering thresholds. ANESTHESIOLOGY 1995; 83:293–9
- Kotani N, Kushikata T, Matsukawa T, Sessler DI, Muraoka M, Hashimoto H, Ishihara H, Matsuki A: A rapid increase in foot tissue temperature predicts cardiovascular collapse during anaphylactic and anaphylactoid reactions. ANESTHESIOLOGY 1997; 87:559–68
- Rosenberg J, Pentel P, Pond S, Benowitz N, Olson K: Hyperthermia associated with drug intoxication. Crit Care Med 1986; 14:964–9
- Frank SM, Kluger MJ, Kunkel SL: Elevated thermostatic setpoint in postoperative patients. ANESTHESIOLOGY 2000; 93:1426–31
- Pernerstorfer T, Schmid R, Bieglmayer C, Eichler HG, Kapiotis S, Jilma B: Acetaminophen has greater antipyretic efficacy than aspirin in endotoxemia: A randomized, double-blind, placebo-controlled trial. Clin Pharmacol Ther 1999; 66:51–7
- 114. Lenhardt R, Negishi C, Sessler DI, Vuong K, Bastanmehr H, Kim J-S, Bjorksten AR : The effects of physical treatment on induced fever in humans. Am J Med 1999; 106:550–5
- Mayer S, Commichau C, Scarmeas N, Presciutti M, Bates J, Copeland D: Clinical trial of an air-circulating cooling blanket for fever control in critically ill neurologic patients. Neurology 2001; 56:292–8
- Diringer MN: Treatment of fever in the neurologic intensive care unit with a catheter-based heat exchange system. Crit Care Med 2004; 32:559–64
- Dae MW, Gao DW, Sessler DI, Chair K, Stillson CA : Effect of endovascular cooling on myocardial temperature, infarct size, and cardiac output in humansized pigs. Am J Physiol Heart Circ Physiol 2002; 282:H1584–91
- Doufas AG, Akc.a O, Barry A, Petrusca DA, Suleman MI, Morioka N, Guarnaschelli JJ, Sessler DI: Initial experience with a novel heat-exchanging catheter in neurosurgical patients. Anesth Analg 2002; 95:1752–6
- Manthous CA, Hall JB, Olson D, Singh M, Chatila W, Pohlman A, Kushner R, Schmidt GA , Wood LD: Effect of cooling on oxygen consumption in febrilecritically ill patients. Am J Resp Crit Care Med 1995; 151:10–4
- Matsukawa T, Kurz A, Sessler DI, Bjorksten AR, Merrifield B, Cheng C: Propofol linearly reduces the vasoconstriction and shivering thresholds. ANESTHESIOLOGY 1995; 82:1169–80
- Talke P, Tayefeh F, Sessler DI, Jeffrey R, Noursalehi M, Richardson C: Dexmedetomidine does not alter the sweating threshold, but comparably and linearly reduces the vasoconstriction and shivering thresholds. ANESTHESIOLOGY 1997; 87:835–41
- Annadata RS, Sessler DI, Tayefeh F, Kurz A, Dechert M: Desflurane slightly increases the sweating threshold, but produces marked, non-linear decreases decreases in the vasoconstriction and shivering thresholds. ANESTHESIOLOGY 1995; 83:1205–11
- Xiong J, Kurz A, Sessler DI, Plattner O, Christensen R, Dechert M, Ikeda T: Isoflurane produces marked and non-linear decreases in the vasoconstriction and shivering thresholds. ANESTHESIOLOGY 1996; 85:240–5
- Kurz A, Xiong J, Sessler DI, Dechert M, Noyes K, Belani K: Desflurane reduces the gain of thermoregulatory arterio-venous shunt vasoconstriction in humans. ANESTHESIOLOGY 1995; 83:1212–9
- Ikeda T, Kim J-S, Sessler DI, Negishi C, Turakhia M, Jeffrey R: Isoflurane alters shivering patterns and reduces maximum shivering intensity. ANESTHESIOLOGY 1998; 88:866–73
- Alfonsi P, Adam F, Passard A, Guignard B, Sessler DI, Chauvin M: Nefopam, a nonsedative benzoxazocine analgesic, selectively reduces the shivering threshold. ANESTHESIOLOGY 2004; 100:37–43
- Kurz A, Ikeda T, Sessler DI, Larson M, Bjorksten AR , Dechert M, Christensen R: Meperidine decreases the shivering threshold twice as much as the vasoconstriction threshold. ANESTHESIOLOGY 1997; 86:1046–54
- Doufas AG, Lin CM, Suleman MI, Liem EB, Lenhardt R, Morioka N, Akc.a O, Shah YM, Bjorksten AR , Sessler DI: Dexmedetomidine and meperidine additively reduce the shivering threshold in humans. Stroke 2003; 34:1218–23
- Roy JD, Girard M, Drolet P: Intrathecal meperidine decreases shivering during cesarean delivery under spinal anesthesia. Anesth Analg 2004; 98:230–4
- Sessler DI, Olofsson CI, Rubinstein EH, Beebe JJ: The thermoregulatory threshold in humans during halothane anesthesia. ANESTHESIOLOGY 1988; 68:836–42
- Washington DE , Sessler DI, McGuire J, Hynson J, Schroeder M, Moayeri A: Painful stimulation minimally increases the thermoregulatory threshold for vasoconstriction during enflurane anesthesia in humans. ANESTHESIOLOGY 1992; 77:286–90
- Sessler DI, Olofsson CI, Rubinstein EH: The thermoregulatory threshold in humans during nitrous oxide-fentanyl anesthesia. ANESTHESIOLOGY 1988; 69: 357–64
- Delaunay L, Bonnet F, Liu N, Beydon L, Catoire P, Sessler DI: Clonidine comparably decreases the thermoregulatory thresholds for vasoconstriction and shivering in humans. ANESTHESIOLOGY 1993; 79:470–4
- Delaunay L, Herail T, Sessler DI, Lienhart A, Bonnet F: Clonidine increases the sweating threshold, but does not reduce the gain of sweating. Anesth Analg 1996; 83:844–8
- Ozaki M, Sessler DI, Suzuki H, Ozaki K, Tsunoda C, Atarashi K: Nitrous oxide decreases the threshold for vasoconstriction less than sevoflurane or isoflurane. Anesth Analg 1995; 80:1212–6
- Imamura M, Matsukawa T, Ozaki M, Sessler DI, Nishiyama T, Kumazawa T: Nitrous oxide decreases the shivering threshold less than isoflurane in rabbits. Br J Anaesth 2003; 90:88–90
- Kurz A, Sessler DI, Annadata R, Dechert M, Christensen R: Midazolam minimally impairs thermoregulatory control. Anesth Analg 1995; 81:393–8
- Matsukawa T, Hanagata K, Ozaki M, Iwashita H, Koshimizu M, Kumazawa T: I.M. midazolam as premedication produces a concentration dependent decrease in core temperature in male volunteers. Br J Anaesth 1997; 78:396–9
- Zbinden AM, Maggiorini M, Petersen-Felix S, Lauber R, Thomson DA, Minder CE: Anesthetic depth defined using multiple noxious stimuli during isoflurane/oxygen anesthesia, I: Motor reactions. ANESTHESIOLOGY 1994; 80:253–60
- Hodgson PS, Liu SS, Gras TW: Does epidural anesthesia have general anesthetic effects? A prospective, randomized, double-blind, placebo-controlled trial. ANESTHESIOLOGY 1999; 91:1687–92
- Nakajima Y, Takamata A, Matsukawa T, Sessler DI, Kitamura Y, Ueno H, Tanaka Y, Mizobe T: Effect of amino acid infusion on central thermoregulatory control in humans. ANESTHESIOLOGY 2004; 100:634–9
- Mizobe T, Nakajima Y, Ueno H, Sessler DI: Fructose administration increases intraoperative core temperature by augmenting both metabolic rate and the vasoconstriction threshold. ANESTHESIOLOGY 2006; 104:1124–30
- Nakajima Y, Mizobe T, Takamata A, Tanaka Y: Baroreflex modulation of peripheral vasoconstriction during progressive hypothermia in anesthetized humans. Am J Physiol Regul Integr Comp Physiol 2000; 279:R1430–6
- Nakajima Y, Takamata A, Ito T, Sessler DI, Kitamura Y, Shimosato G, Taniguchi S, Matsuyama H, Tanaka Y, Mizobe T: Upright posture reduces thermogenesis and augments core hypothermia. Anesth Analg 2002; 94:1646–51
- Lopez M, Ozaki M, Sessler DI, Valdes M: Physiological responses to hyperthermia during epidural anesthesia and combined epidural/enflurane anesthesia in women. ANESTHESIOLOGY 1993; 78:1046–54
- Sessler DI, Hynson J, McGuire J, Moayeri A, Heier T: Thermoregulatory vasoconstriction during isoflurane anesthesia minimally decreases heat loss. ANESTHESIOLOGY 1992; 76:670–5
- Ikeda T, Sessler DI, Tayefeh F, Negishi C, Turakhia M, Marder D, Bjorksten AR, Larson MD: Meperidine and alfentanil do not reduce the gain or maximum intensity of shivering. ANESTHESIOLOGY 1998; 88:858–65
- Passias TC, Mekjavic IB, Eiken O: The effect of 30% nitrous oxide on thermoregulatory responses in humans during hypothermia. ANESTHESIOLOGY 1992; 76:550–9
- Bissonnette B, Sessler DI: The thermoregulatory threshold in infants and children anesthetized with isoflurane and caudal bupivacaine. ANESTHESIOLOGY 1990; 73:1114–8
- Bissonnette B, Sessler DI: Thermoregulatory thresholds for vasoconstric- tion in pediatric patients anesthetized with halothane or halothane and caudal bupivacaine. ANESTHESIOLOGY 1992; 76:387–92
- Kurz A, Plattner O, Sessler DI, Huemer G, Redl G, Lackner F: The threshold for thermoregulatory vasoconstriction during nitrous oxide/isoflurane anesthesia is lower in elderly than young patients. ANESTHESIOLOGY 1993; 79:465–9
- Ozaki M, Sessler DI, Suzuki H, Ozaki K, Atarashi K, Negishi C: The threshold for thermoregulatory vasoconstriction during nitrous oxide/sevoflurane anesthesia is reduced in elderly patients. Anesth Analg 1997; 84:1029–33
- Hynson JM, Sessler DI, Moayeri A, McGuire J: Absence of nonshivering thermogenesis in anesthetized humans. ANESTHESIOLOGY 1993; 79:695–703
- Dicker A, Ohlson KB, Johnson L, Cannon B, Lindahl SG, Nedergaard J: Halothane selectively inhibits nonshivering thermogenesis. ANESTHESIOLOGY 1995; 82:491–501
- Plattner O, Semsroth M, Sessler DI, Papousek A, Klasen C, Wagner O: Lack of nonshivering thermogenesis in infants anesthetized with fentanyl and propofol. ANESTHESIOLOGY 1997; 86:772–7
- Ozaki M, Kurz A, Sessler DI, Lenhardt R, Schroeder M, Moayeri A, Noyes KM, Rotheneder E: Thermoregulatory thresholds during spinal and epidural anesthesia. ANESTHESIOLOGY 1994; 81:282–8
- Kurz A, Sessler DI, Schroeder M, Kurz M: Thermoregulatory response thresholds during spinal anesthesia. Anesth Analg 1993; 77:721–6
- Leslie K, Sessler DI: Reduction in the shivering threshold is proportional to spinal block height. ANESTHESIOLOGY 1996; 84:1327–31
- Glosten B, Sessler DI, Ostman LG, Faure EAM, Thisted RA: Intravenous lidocaine does not cause tremor or alter thermoregulation. Reg Anesth 1991; 16:218–22
- Hynson J, Sessler DI, Glosten B, McGuire J: Thermal balance and tremor patterns during epidural anesthesia. ANESTHESIOLOGY 1991; 74:680–90
- Leslie K, Sessler DI, Bjorksten A, Ozaki M, Matsukawa T, Schroeder M, Lin S: Propofol causes a dose-dependent decrease in the thermoregulatory threshold for vasoconstriction, but has little effect on sweating. ANESTHESIOLOGY 1994; 81:353–60
- Glosten B, Sessler DI, Faure EAM, Stoen R, Thisted RA, Karl L: Central temperature changes are poorly perceived during epidural anesthesia. ANESTHESIOLOGY 1992; 77:10–6
- Emerick TH, Ozaki M, Sessler DI, Walters K, Schroeder M: Epidural anesthesia increases apparent leg temperature and decreases the shivering threshold. ANESTHESIOLOGY 1994; 81:289–98
- Kim J-S, Ikeda T, Sessler D, Turakhia M, Jeffrey R: Epidural anesthesia reduces the gain and maximum intensity of shivering. ANESTHESIOLOGY 1998; 88:851–7
- Ponte J, Collett BJ, Walmsley A: Anaesthetic temperature and shivering in epidural anaesthesia. Acta Anaesthesiol Scand 1986; 30:584–7
- Ponte J, Sessler DI: Extradurals and shivering: Effects of cold and warm extradural saline injections in volunteers. Br J Anaesth 1990; 64:731–3
- Harris MM, Lawson D, Cooper CM, Ellis J: Treatment of shivering after epidural lidocaine. Reg Anesth 1989; 14:13–8
- Horn E-P, Sessler DI, Standl T, Schroeder F, Bartz H-J, Beyer J-C, Schulte am Esch J: Non-thermoregulatory shivering in patients recovering from isoflurane or desflurane anesthesia. ANESTHESIOLOGY 1998; 89:878–86
- Panzer O, Ghazanfari N, Sessler DI, Yu.cel Y, Greher M, Akc.a A, DonnerA, Germann P, Kurz A: Shivering and shivering-like tremor during labor with and without epidural analgesia. ANESTHESIOLOGY 1999; 90:1609–16
- Horn E-P, Schroeder F, Wilhelm S, Sessler DI, Standl T, von dem Busche K, Schulte am Esch J: Postoperative pain facilitates non-thermoregulatory tremor. ANESTHESIOLOGY 1999; 91:979–84
- Sharkey A, Lipton JM, Murphy MT , Giesecke AH: Inhibition of postanesthetic shivering with radiant heat. ANESTHESIOLOGY 1987; 66:249–52
- Brownbridge P: Shivering related to epidural blockade with bupivacaine in labour, and the influence of epidural pethidine. Anaesth Intensive Care 1986; 14:412–7
- Joris J, Banache M, Bonnet F, Sessler DI, Lamy M: Clonidine and ketanserin both are effective treatments for postanesthetic shivering. ANESTHESIOLOGY 1993; 79:532–9
- Kizilirmak S, Karakas SE, Akc.a O, Ozkan T, Yavru A, Pembeci K, Sessler DI: Magnesium sulphate stops postanesthetic shivering. Proc N Y Acad Sci 1997; 813:799–806
- Goetzl L, Rivers J, Zighelboim I, Wali A, Badell M, Suresh MS: Intrapartum epidural analgesia and maternal temperature regulation. Obstet Gynecol 2007; 109:687–90
- Fusi L, Maresh MJA, Steer PJ, Beard RW: Maternal pyrexia associated with the use of epidural analgesia in labour. Lancet 1989; 1:1250–2
- Philip J, Alexander JM, Sharma SK, Leveno KJ, McIntire DD, Wiley J: Epidural analgesia during labor and maternal fever. ANESTHESIOLOGY 1999; 90: 1271–5
- Vinson DC, Thomas R, Kiser T: Association between epidural analgesia during labor and fever. J Fam Pract 1993; 36:617–22
- Macaulay JH, Mrcog KB, Steer PJ: Epidural analgesia in labor and fetal hyperthermia. Obstet Gynecol 1992; 80:665–9
- Lieberman E, Lang JM, Frigoletto F, Richardson DK, Ringer SA, Cohen A: Epidural analgesia, intrapartum fever, and neonatal sepsis evaluation. Pediatrics 1997; 99:415–9
- Lieberman E, Cohen A, Lang J, Frigoletto F, Goetzl L: Maternal intrapartum temperature elevation as a risk factor for cesarean delivery and assisted vaginal delivery. Am J Public Health 1999; 89:506–10
- Bredtmann RD , Herden HN, Teichmann W, Moecke HP, Kniesel B, Baetgen R, Techklenburg A: Epidural analgesia in colonic surgery: Results of a randomized prospective study. Br J Surg 1990; 77:638–42
- Churgay CA, Smith MA, Blok B: Maternal fever during labor: What does it mean? J Am Board Fam Pract 1994; 7:14–24
- Dashe JS, Rogers BB, McIntire DD, Leveno KJ: Epidural analgesia and intrapartum fever: Placental findings. Obstet Gynecol 1999; 93:341–4
- Goetzl L, Zighelboim I, Badell M, Rivers J, Mastrangelo MA, Tweardy D, Suresh MS: Maternal corticosteroids to prevent intrauterine exposure to hyperthermia and inflammation: A randomized, double-blind, placebo-controlled trial. Am J Obstet Gynecol 2006; 195:1031–7
- Goetzl L, Rivers J, Evans T, Citron DR , Richardson BE, Lieberman E, Suresh MS: Prophylactic acetaminophen does not prevent epidural fever in nulliparous women: A double-blind placebo-controlled trial. J Perinatol 2004; 24:471–5
- Reilly DR, Oppenheimer LW: Fever in term labour. J Obstet Gynaecol Can 2005; 27:218–23
- Lieberman E, O'Donoghue C: Unintended effects of epidural analgesia during labor: A systematic review. Am J Obstet Gynecol 2002; 186:S31–68
- Negishi C, Lenhardt R, Ozaki M, Ettinger K, Bastanmehr H, Bjorksten AR, Sessler DI: Opioids inhibit febrile responses in humans, whereas epidural analgesia does not: An explanation for hyperthermia during epidural analgesia. ANESTHESIOLOGY 2001; 94:218–22
- Gross JB, Cohen AP, Lang JM, Frigoletto FD, Lieberman ES: Differences in systemic opioid use do not explain increased fever incidence in parturients receiving epidural analgesia. ANESTHESIOLOGY 2002; 97:157–61

